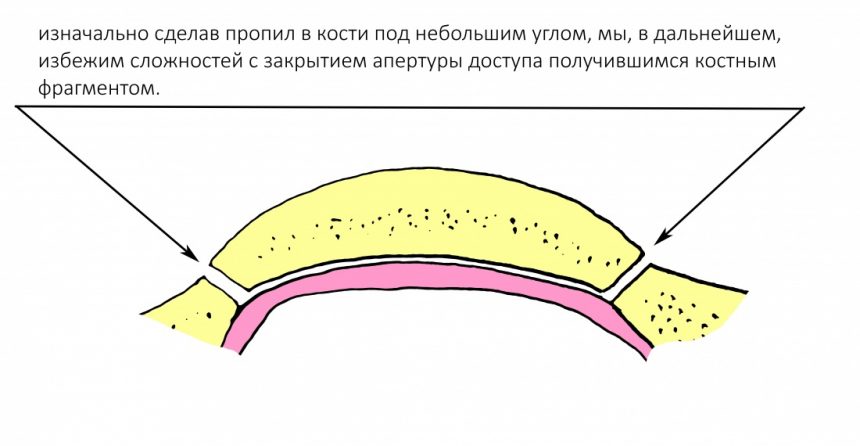
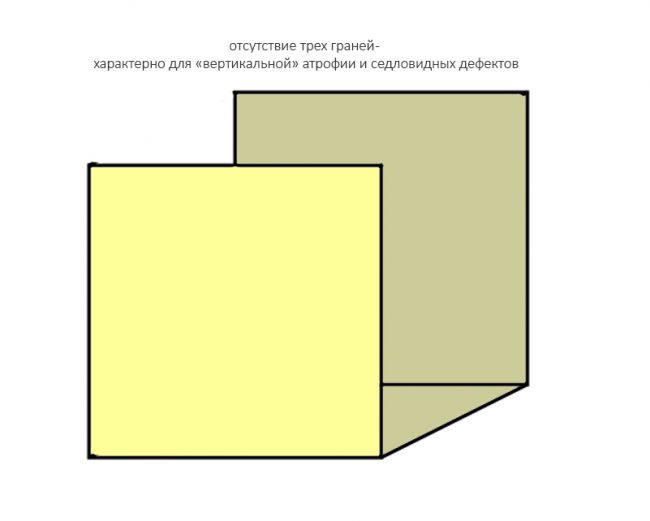
Вообще, сегодня я планировал опубликовать статью о том, как не переплатить в стоматологической клинике, но тут в КЛИНИКУ ИН вернулась наша давняя пациентка Зинаида, и я решил, что публикация под рабочим названием «Пчелы против меда» подождет. Мы поговорим об остеопластике, сочетаемой с имплантацией, долгосрочных результатах наращивания костной ткани и методах их оценки. Заодно узнаешь, почему я перестал участвовать в тематических аквадискотеках и сидеть в стоматологических пабликах и на форумах.
Традиционно, я предлагаю тебе вспомнить всё, что написано об остеопластике с одновременной имплантацией до этого момента:
Основная цель имплантологического лечения… — публикация 2014 года, где я впервые показываю один из клинических случаев сочетания имплантации и остеопластики. Да, мы проводили подобное лечение во временя, когда ты еще не знал, что такое имплант и чем он отличается от имплантата.
Не усложняйте! Остеопластика — это не так уж и страшно. — публикация из эпохи, когда наращивание костной ткани казалось чем-то очень страшным и опасным. Интересно, что в те времена мы делали больше подобных операций, чем делаем сейчас. 2015 год.
Имплантация, расщепление альвеолярного гребня и немного НКР — статья аж 10-летней давности, первая из публикаций, посвященных имплантации, проводимой с одновременной остеопластикой.
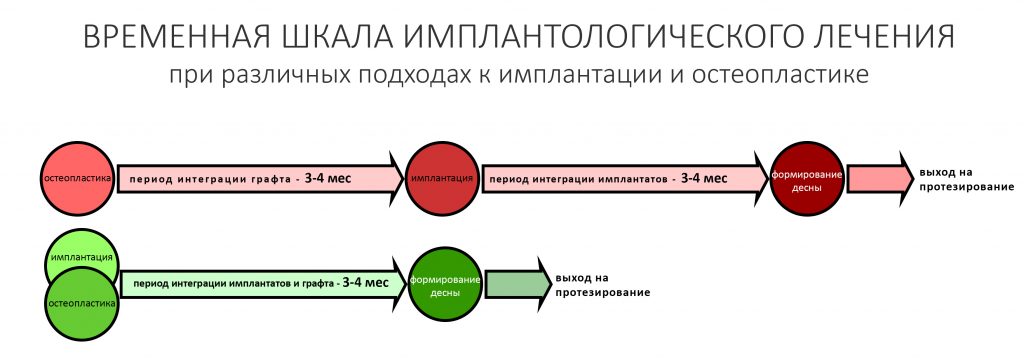
Имплантация и остеопластика (наращивание костной ткани): вместе или врозь? Часть I — статья 2016 года, в которой описан метод из сегодняшней статьи. С имплантатами Nobel Biocare, между прочим.
Имплантация и остеопластика: вместе или врозь? Часть II, плюс Ankylos, плюс Geistlich — эпичная хирургическая работа, эпичный клинический случай аж 2013 года, от воспоминаний о которых у меня до сих пор дергается левый глаз.
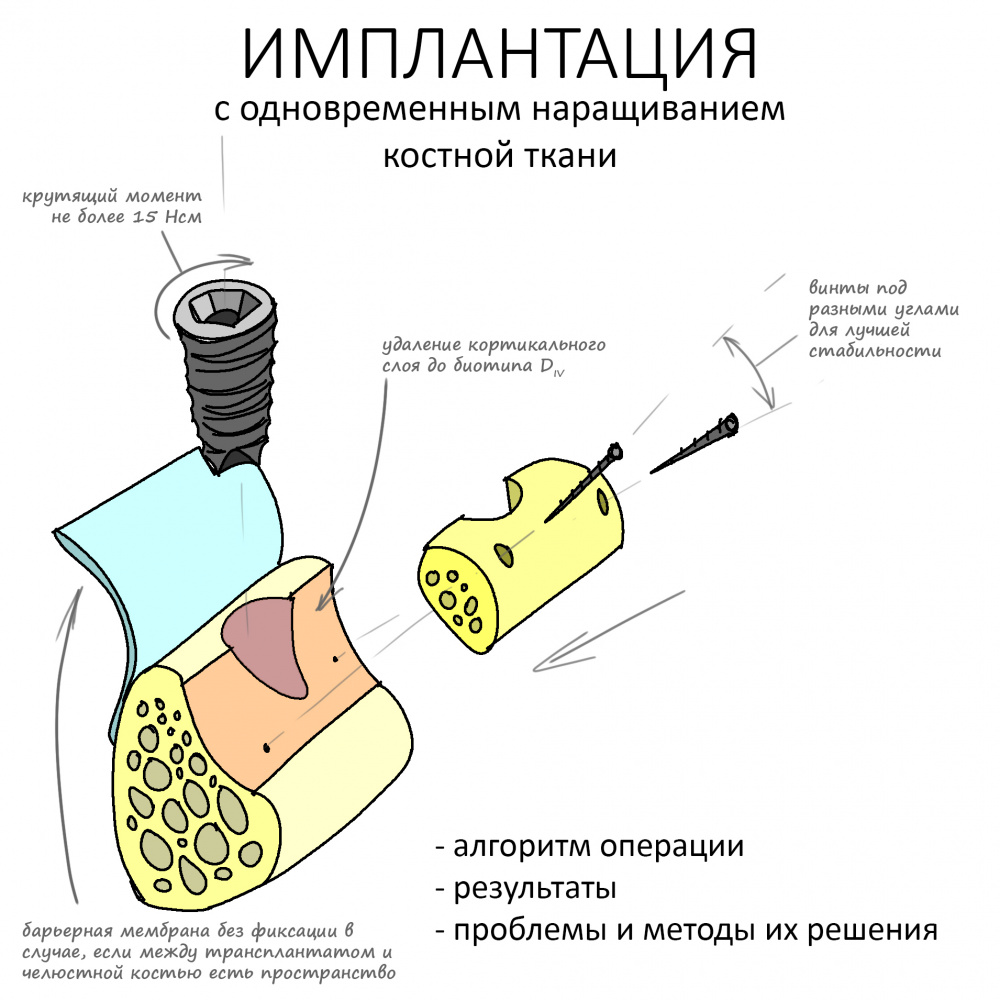
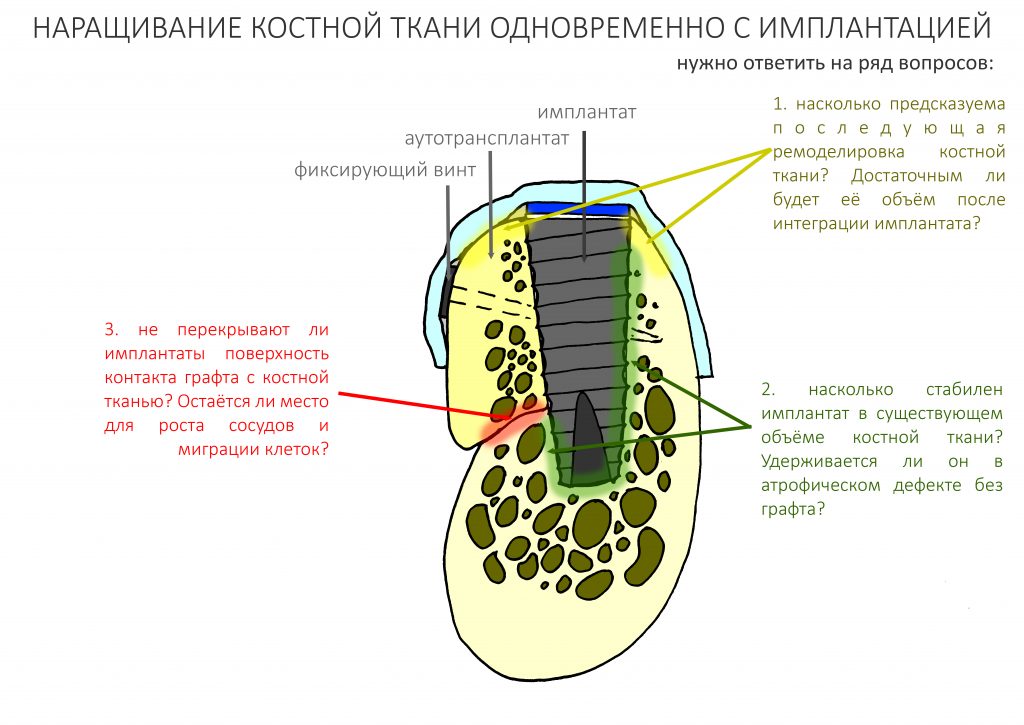
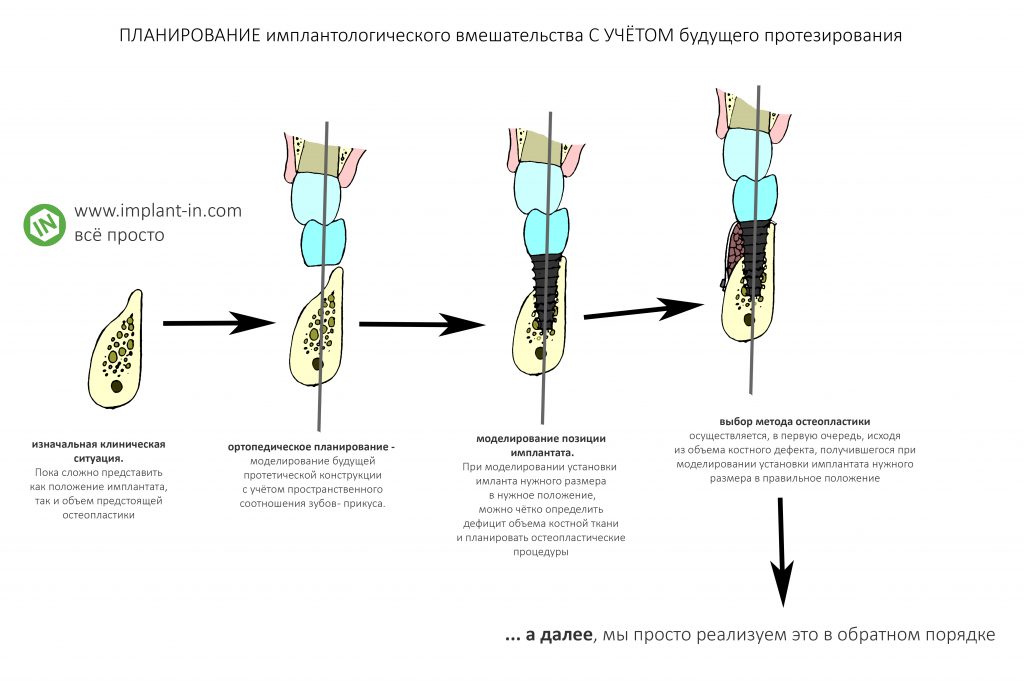
Имплантация с одновременным наращиванием костной ткани. Планирование и принятие решений — первая подробная и логически структурированная часть руководства по методике. Специально для врачей, 2022 год.
Имплантация с одновременным наращиванием костной ткани. Алгоритм операции, результаты, проблемы и методы их решения — вторая часть руководства, 2022 год. По сути, обобщение всего моего опыта в этом направлении.
Еще почитай что-нибудь с меткой «остеопластика» на этом сайте или 2026.implant-in.com. В жизни пригодится.
Как видишь, моя компетенция в этих вопросах легко подтверждается историей моих же публикаций. Я провожу такие операции больше пятнадцати лет, столько же наблюдаю результаты и лечу осложнения, если они вдруг случаются. Если ты хочешь стать имплантологом и научиться делать что-то подобное — без проблем. Переходи на эту страницу, внимательно прочитай условия и приезжай на стажировку.
Ну, и книги. Про книги не забудь — их можно купить в моем интернет-магазине последиплом.рф. Первый том «Базовые принципы» — это то, что должен знать каждый имплантолог. Второй том «Немедленная имплантация» — это движение вперед, когда к твоим навыкам отсроченной имплантации добавляется новая методика, установка имплантата в лунку только что удаленного зуба.
Цена любой из книг — всего 4 000 рублей. Это дешевле, чем сходить на однодневные курсы.
Еще взамен уничтоженного канала, у нас появилась целая группа в Телеграм, где есть отдельная тема для врачей (стоматологов и не только). Там можно спрашивать, отвечать, комментировать, спорить и даже материться. Я буду рад, если ты на неё подпишешься.
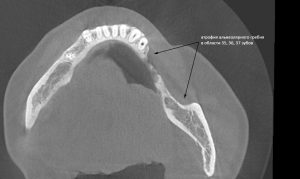
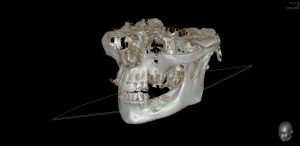
Вернемся к Зинаиде. Мы познакомились с ней в 2013 году, она гражданин соседнего и до сих пор дружественного государства. Как обычно бывает в таких случаях, Зинаида прислала данные КЛКТ, после мы созвонились и обсудили всё по телефону. Договорились следовать в рамках инструкций с этой страницы: пациентка нашла доктора по месту жительства, который будет её осматривать, забронировала гостиницу на несколько дней и, как было запланировано, прилетела к нам точно ко времени.
«… и даже то, что быть не может — однажды тоже может быть!»
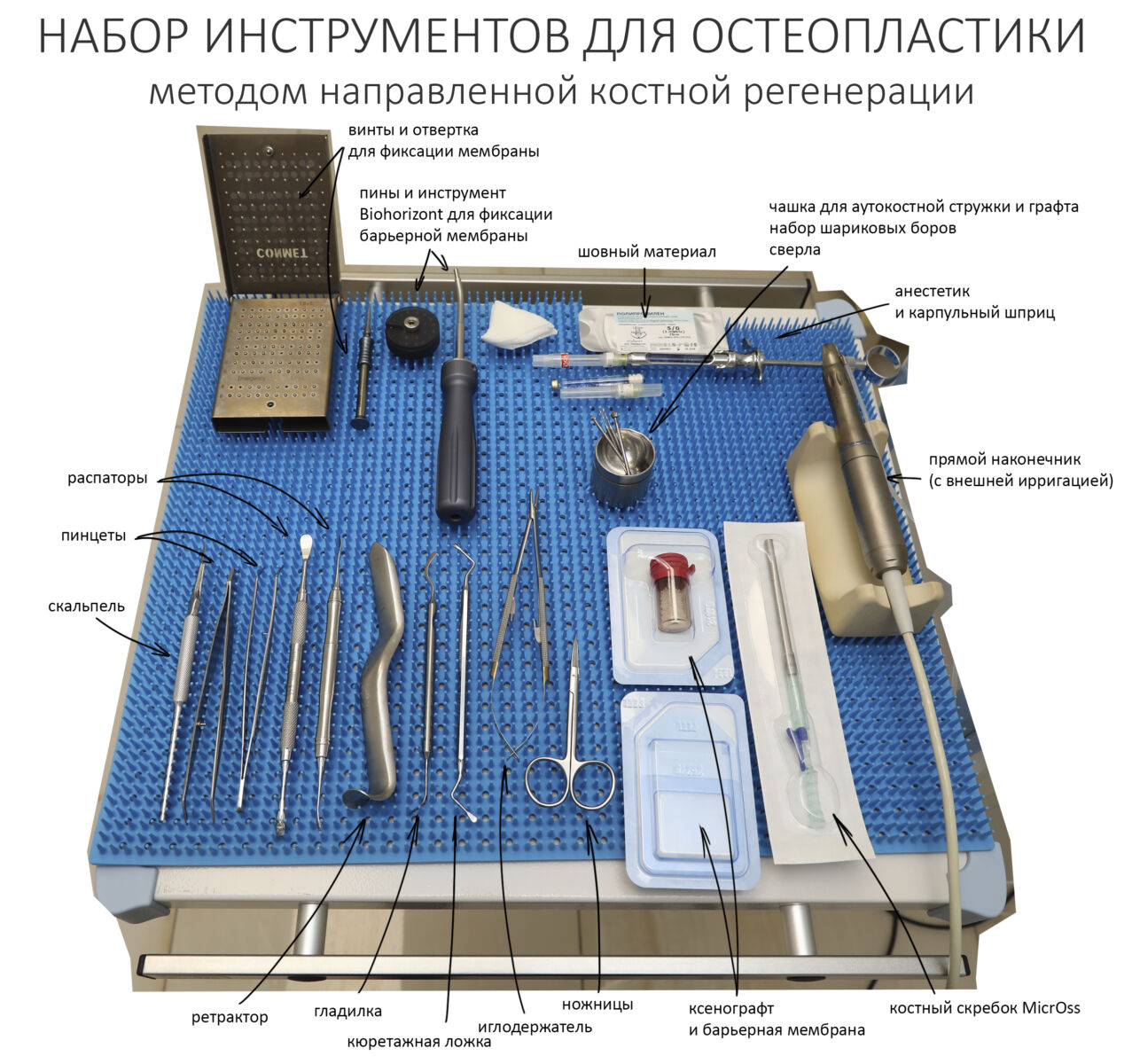
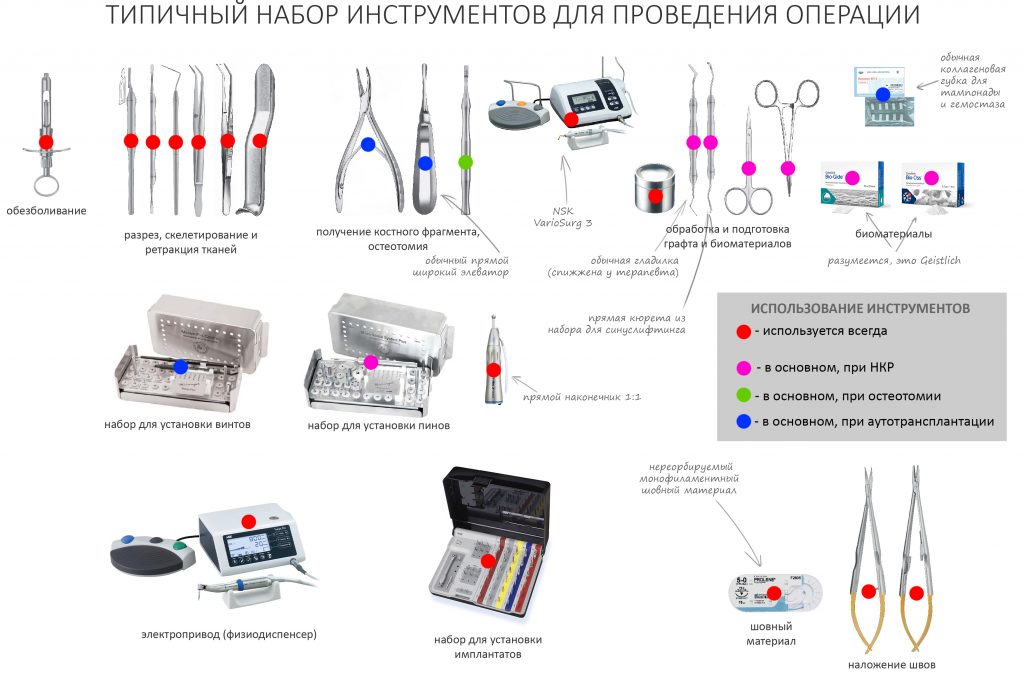
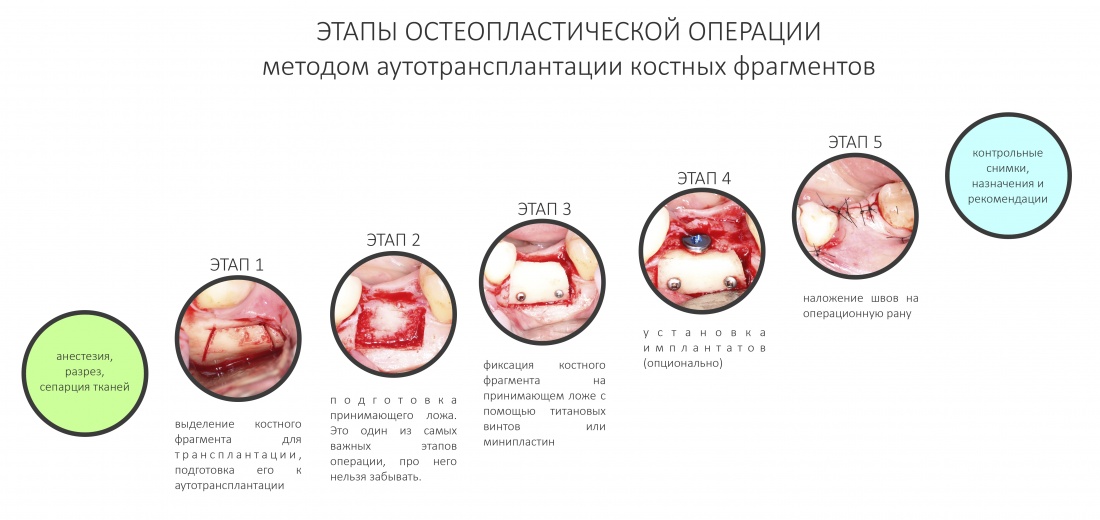
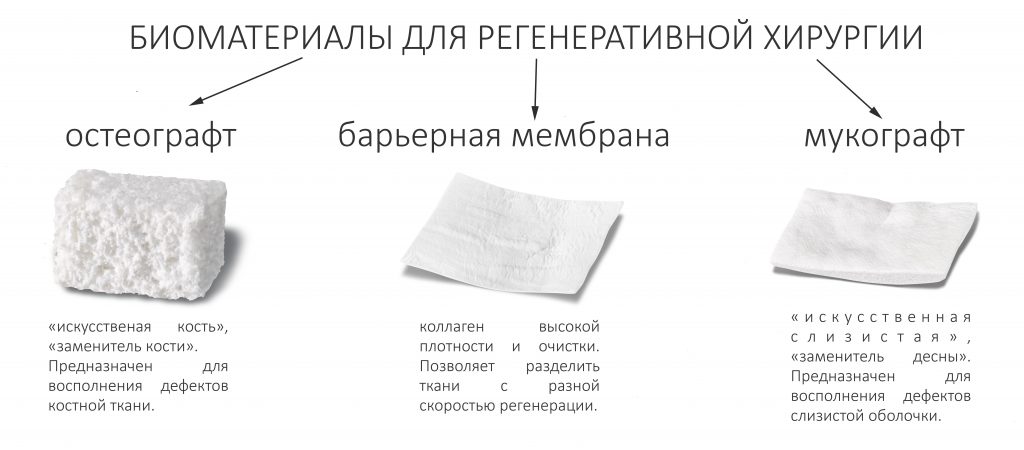
Что бы ты ни планировал — всегда что-то может пойти не по плану. Хирургии это касается в первую очередь, именно поэтому мы держим в клинике солидный запас биоматериалов и имплантатов, все основные инструменты продублированы, а к остеопластике операционную готовят по принципу «хз, по ходу дела решим…»
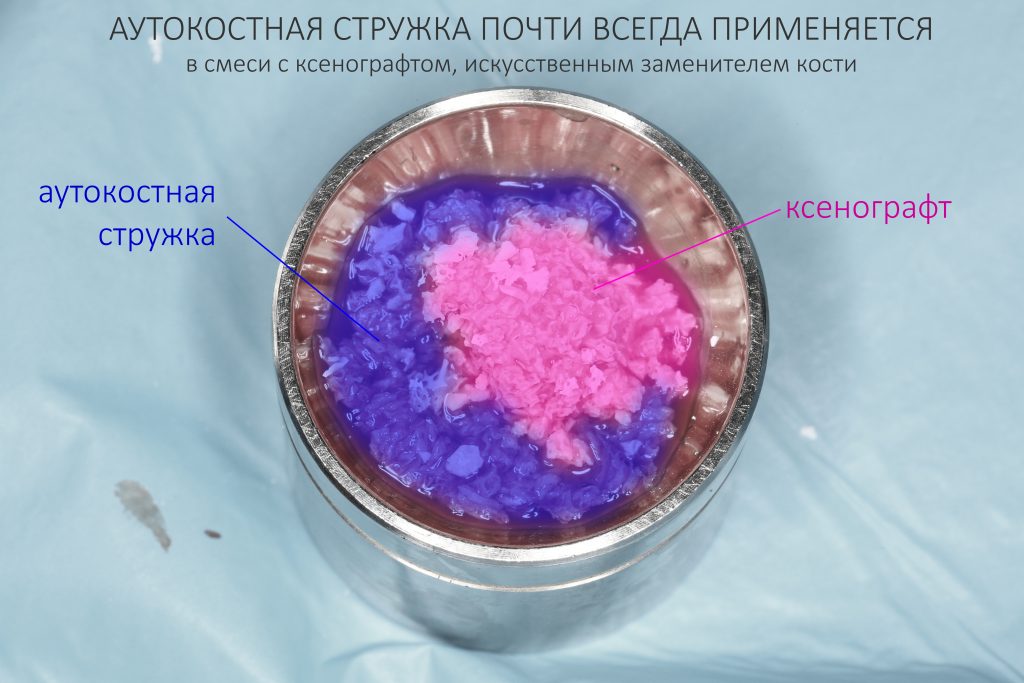
Ремарка: последнее означает, что ассистенты готовят операционную не к конкретному методу остеопластики (например, к АТККФ или НКР), а ко всему сразу, поскольку не всегда ясно, каким методом будет проводиться наращивание костной ткани.
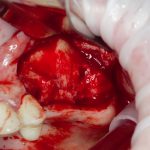
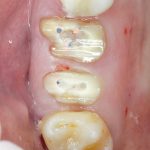
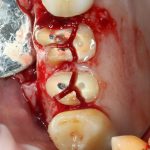
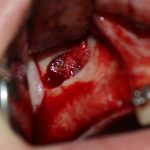
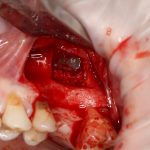
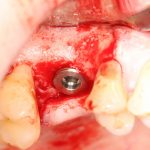
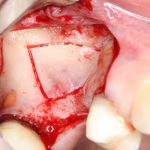
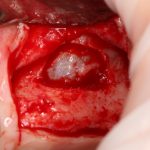
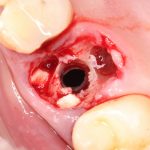
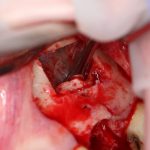
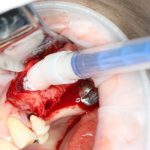
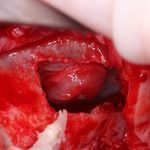
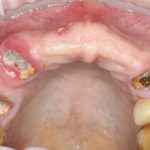
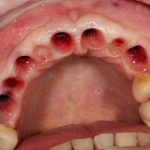
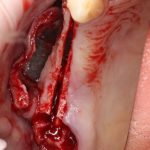
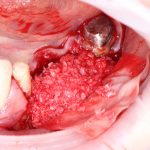
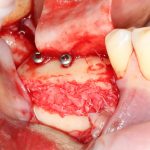
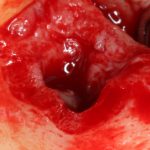
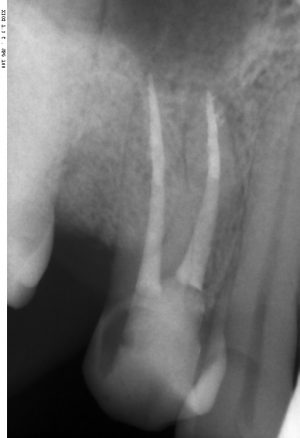
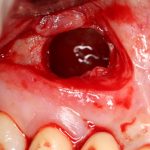
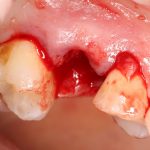
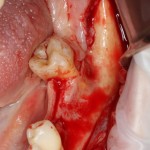
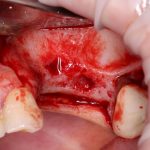
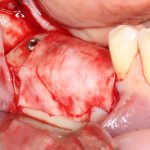
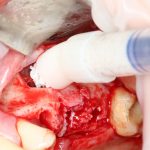
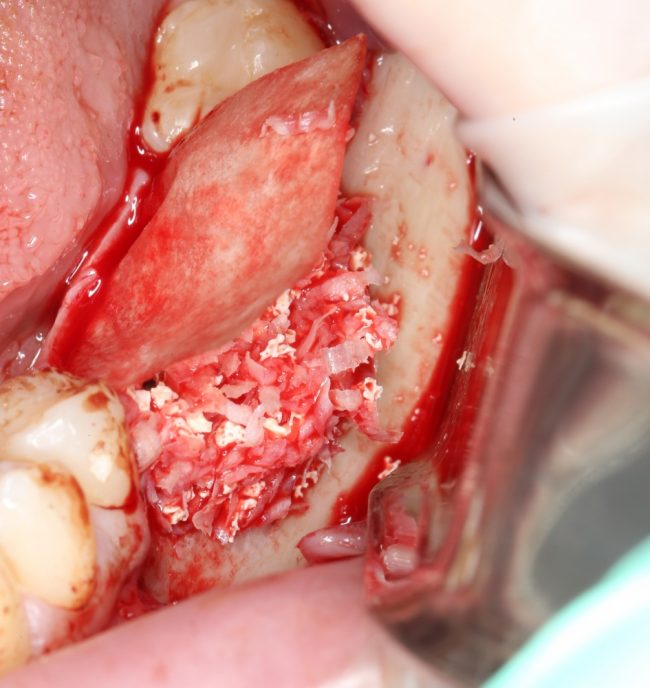
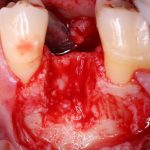
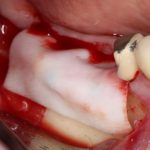
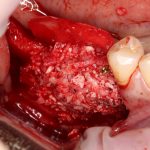
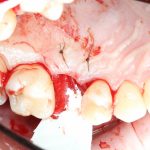
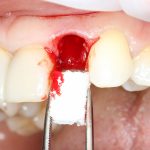
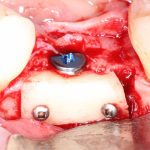
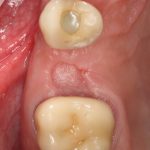
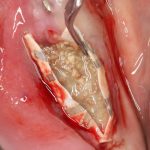
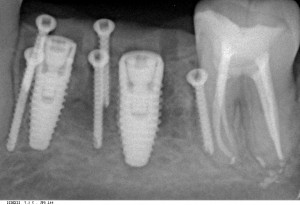
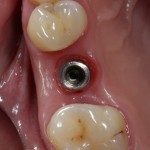
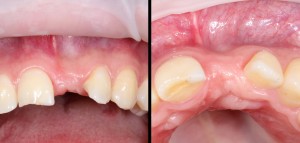
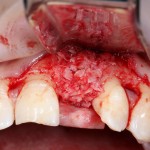
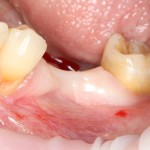
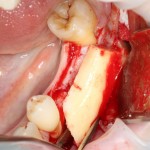
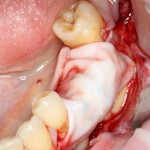
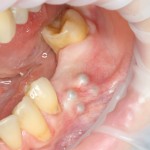
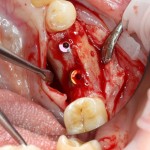
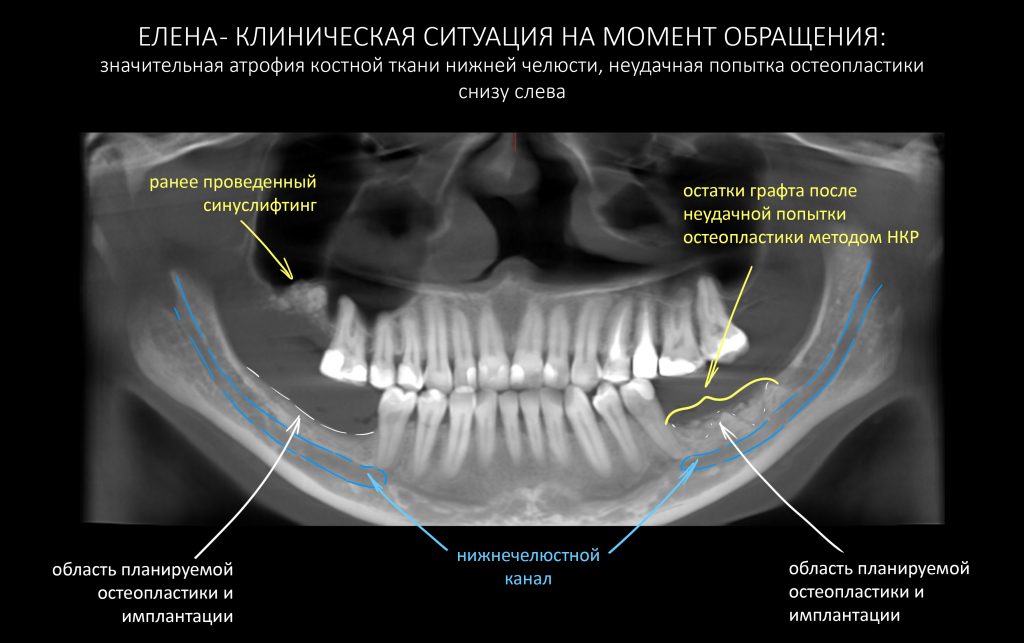
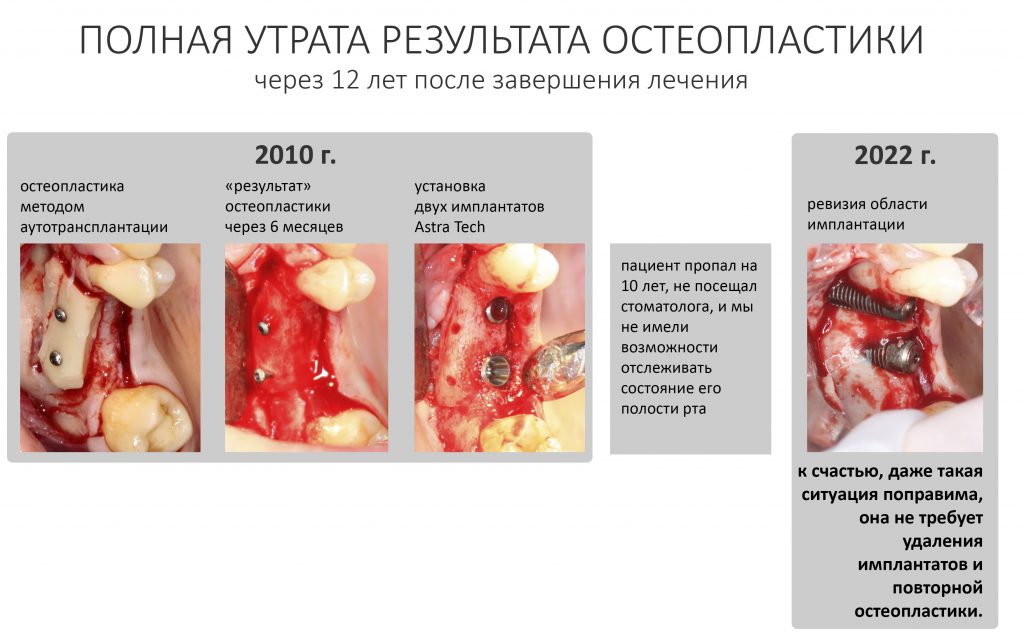
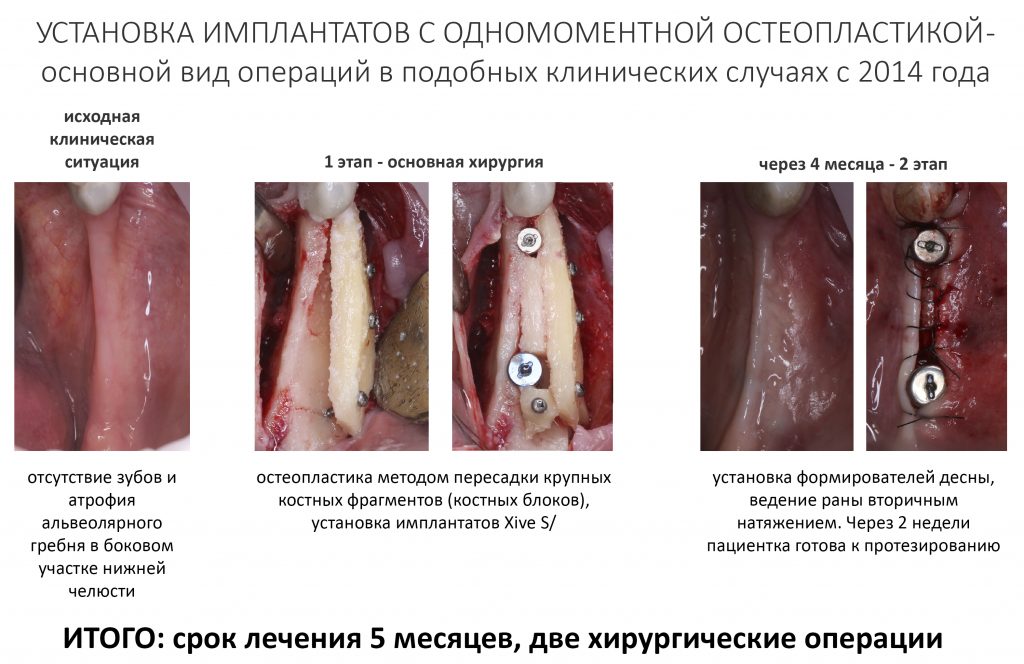
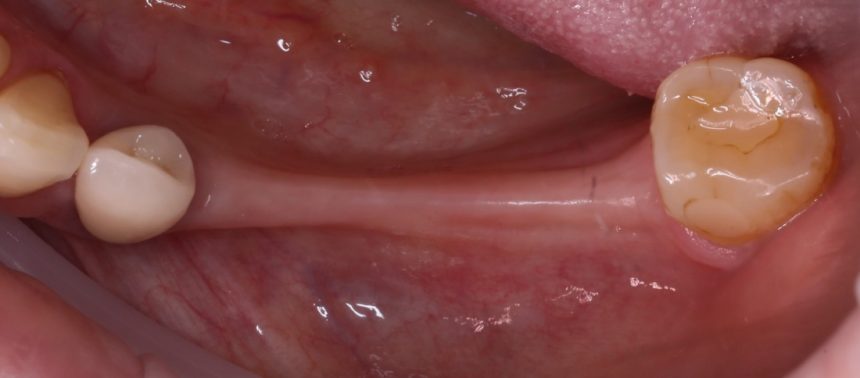
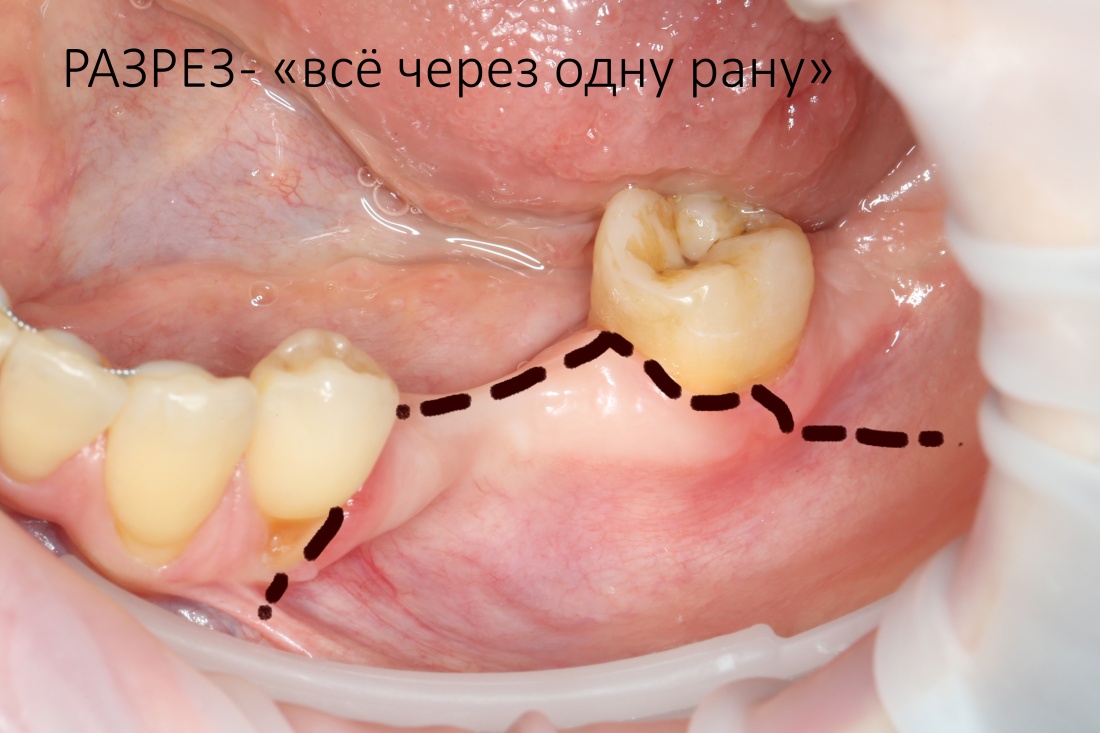
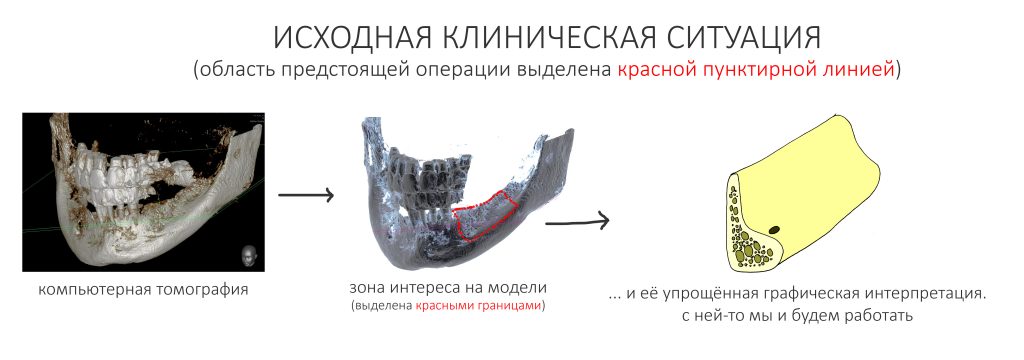
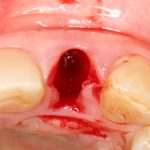
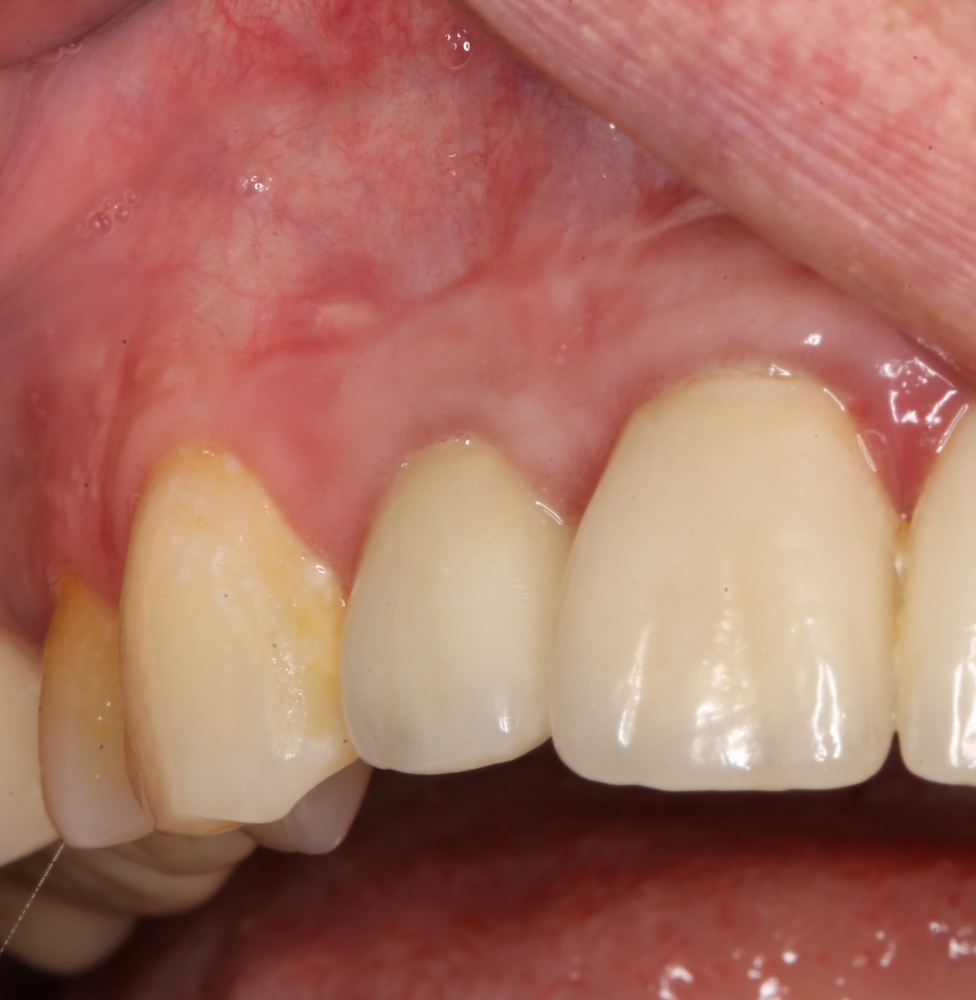
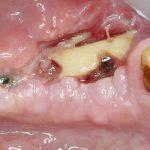
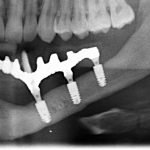
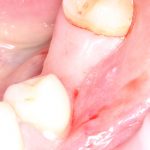
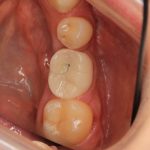
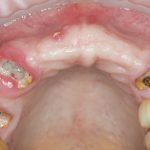
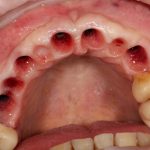
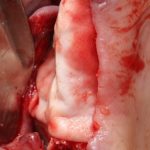
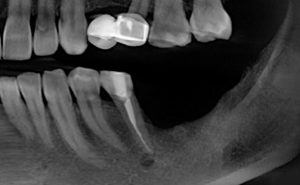
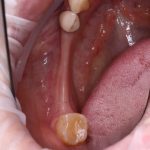
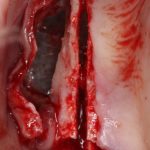
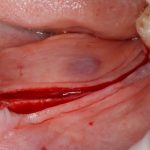
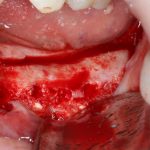
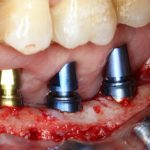
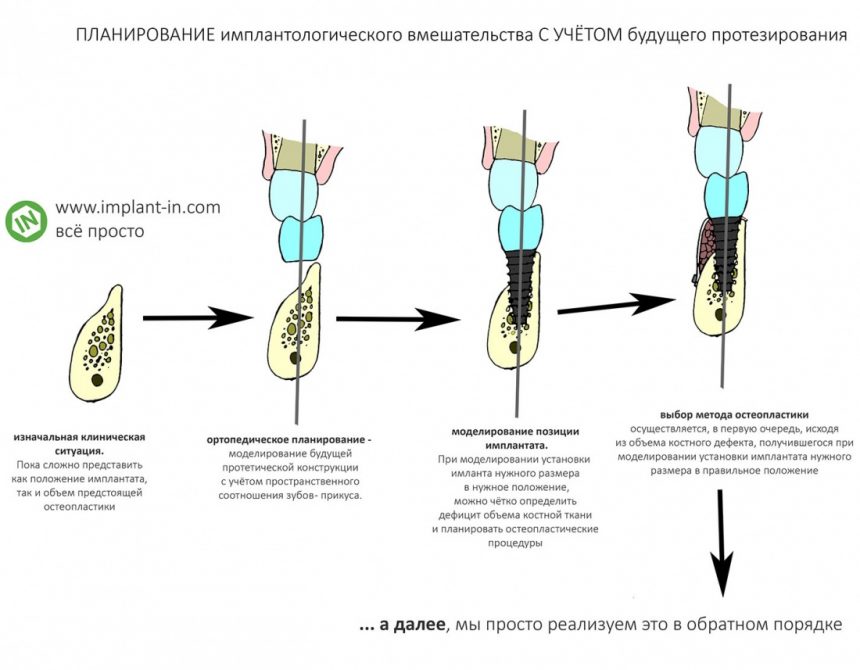
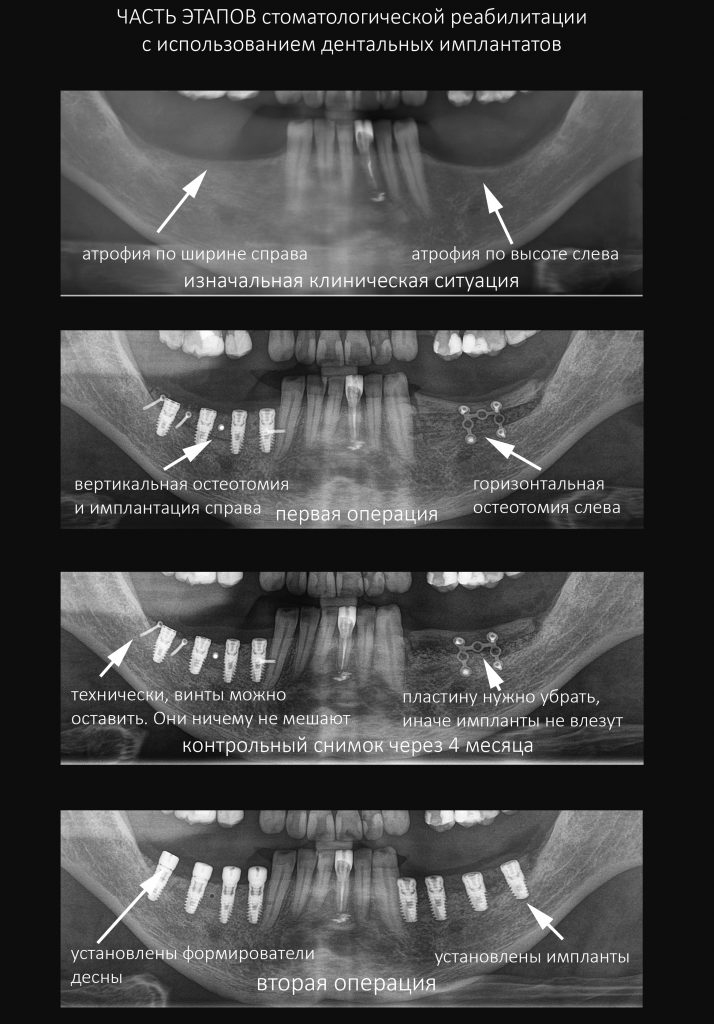
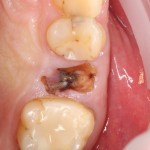
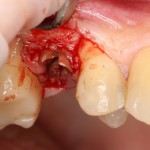
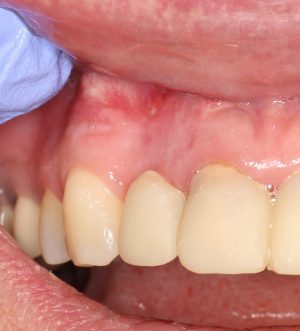
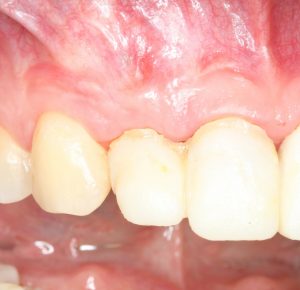
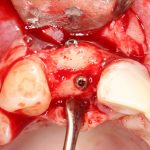
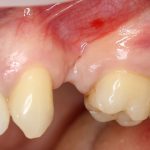
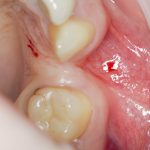
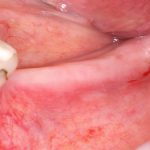
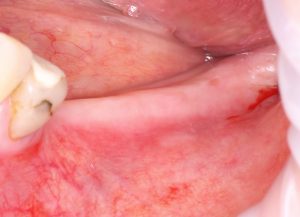
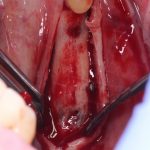
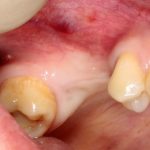
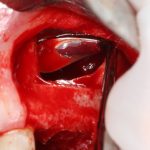
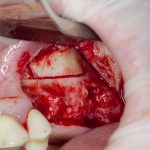
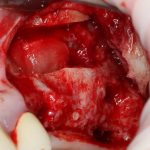
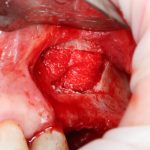
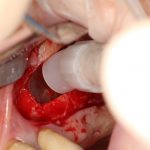
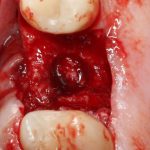
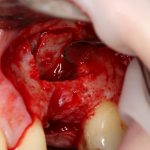
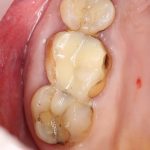
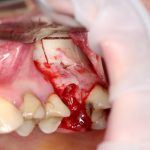
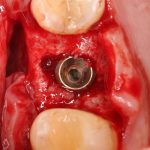
В общем, так и получилось. Уж не помню, почему я наобещал пациентке, что мы поставим ей имплантаты одновременно с остеопластикой. Но я наобещал. И, когда увидел клиническую картину в полости рта:
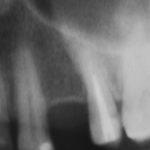
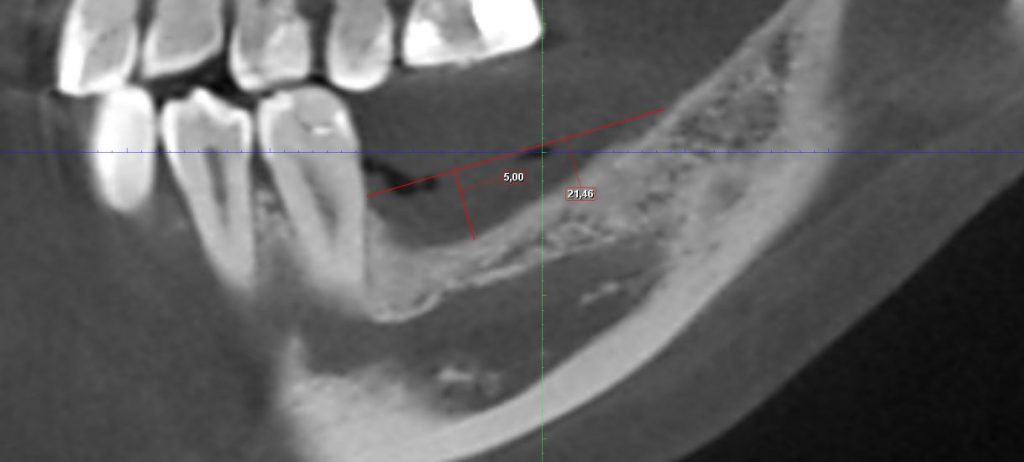
у меня появились серьезные сомнения, смогу ли я выполнить своё обещание. Вот только не спрашивай меня «Вот чо, сложно было по КЛКТ посмотреть?». Я же не спрашиваю тебя, где ты был в 2013 году, и сделал ли ты домашку. Но, в целом, план операции у нас не поменялся. Как и было оговорено, мы проведем остеопластику с одновременной имплантацией в боковом участке нижней челюсти справа.
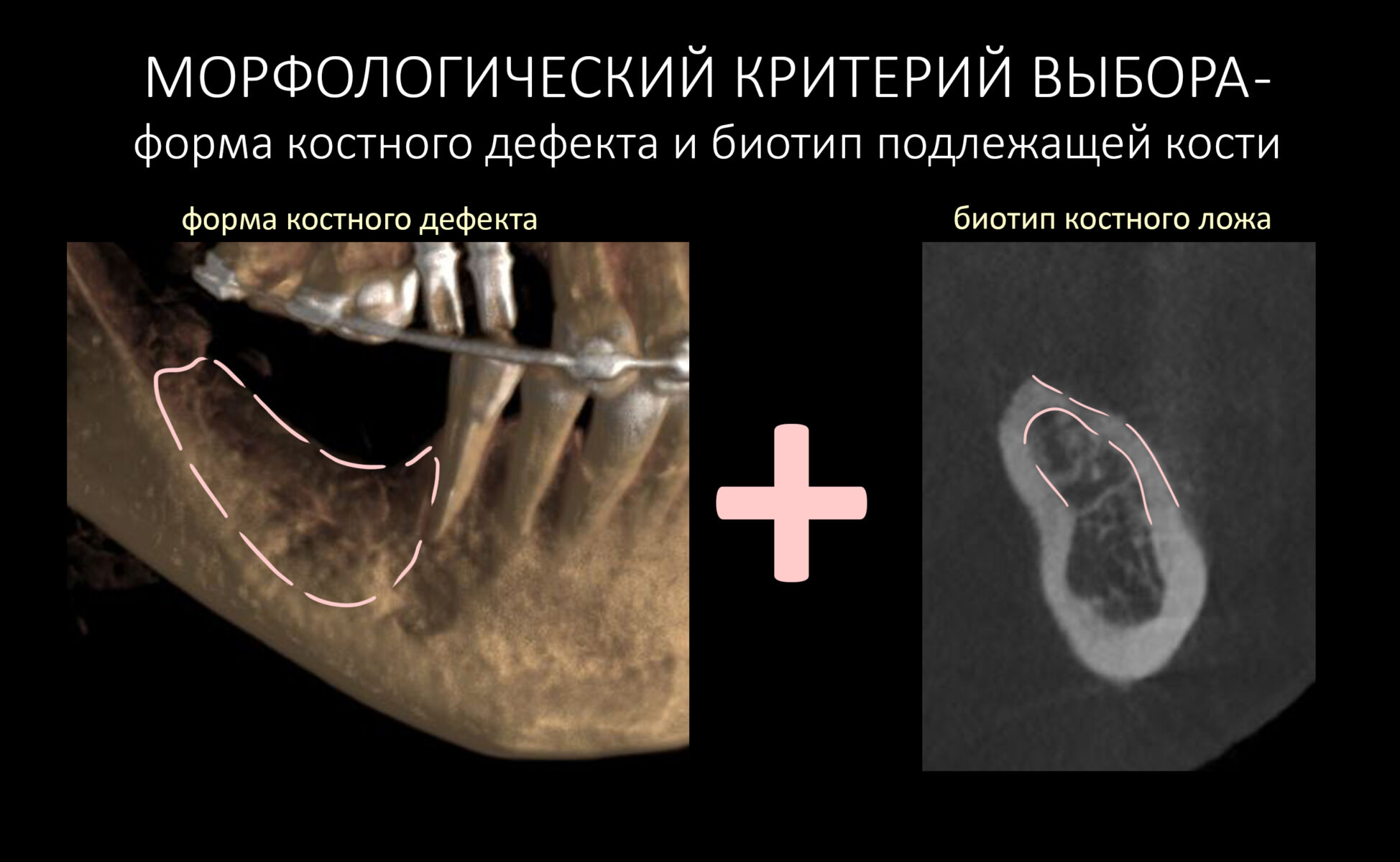
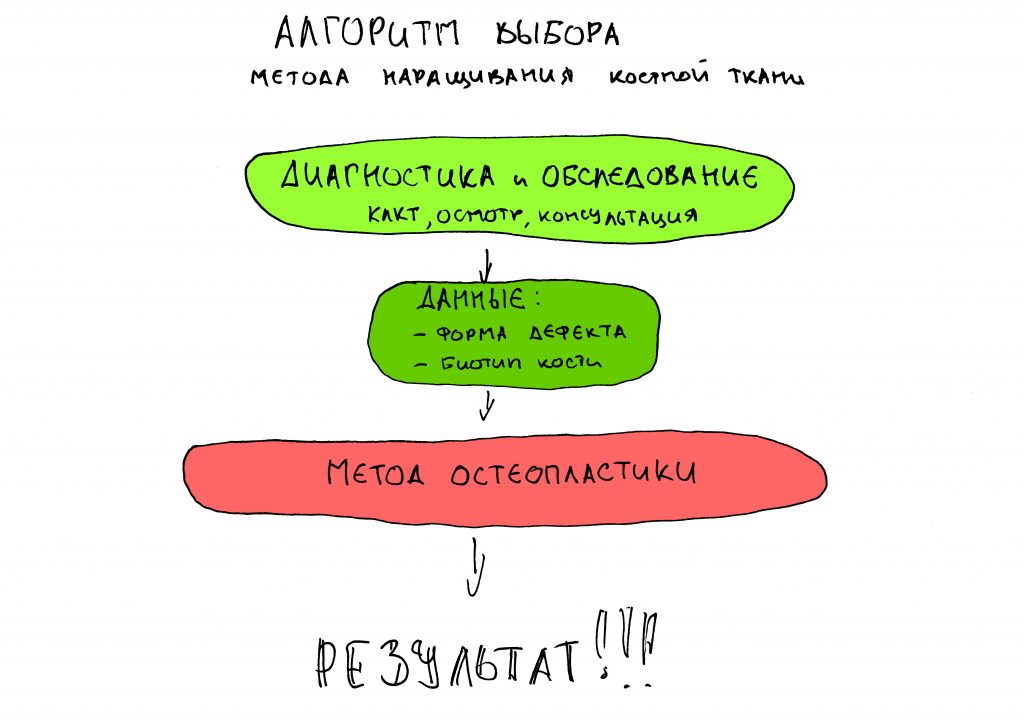
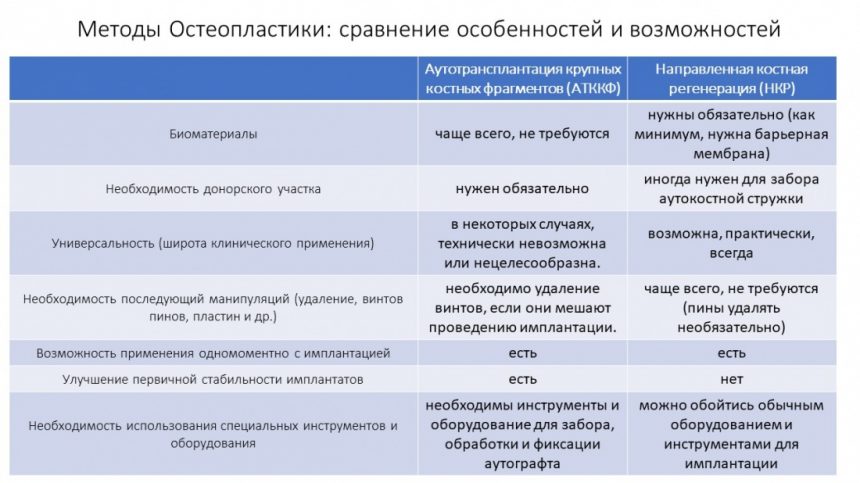
Выбор метода.
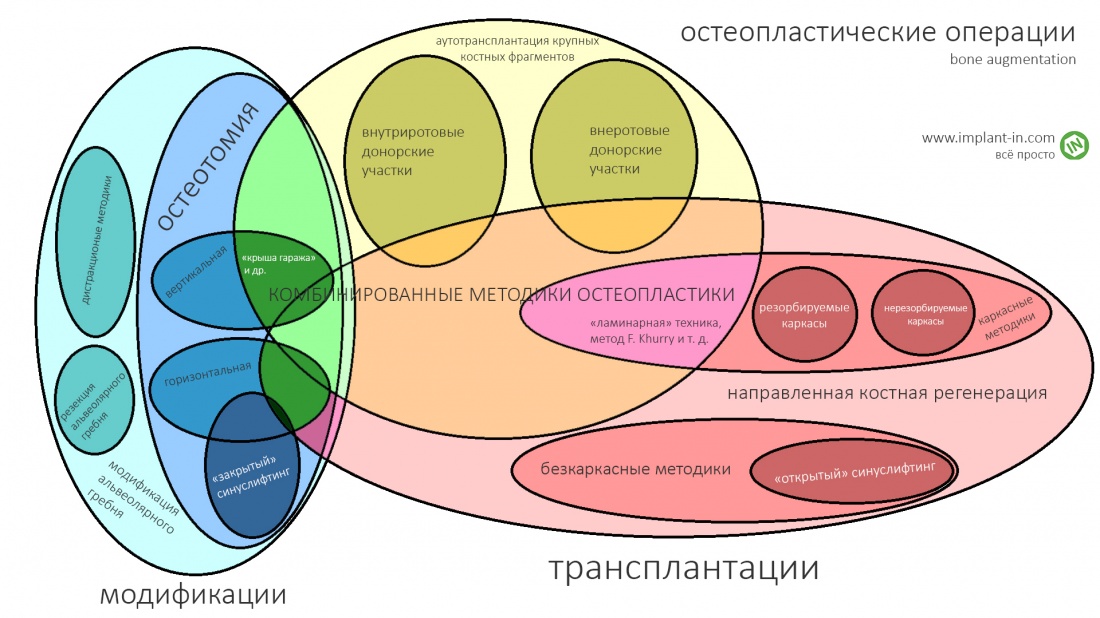
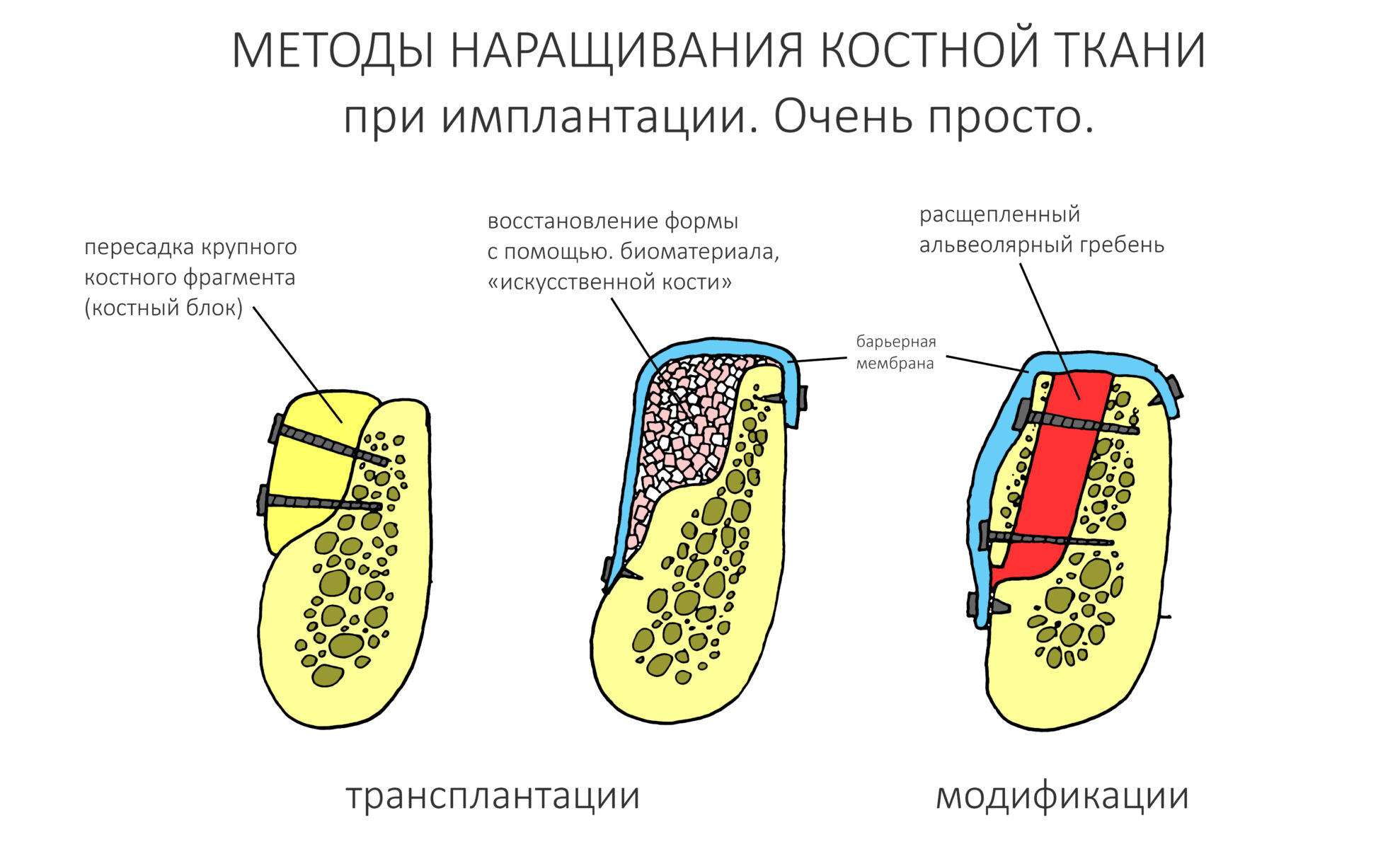
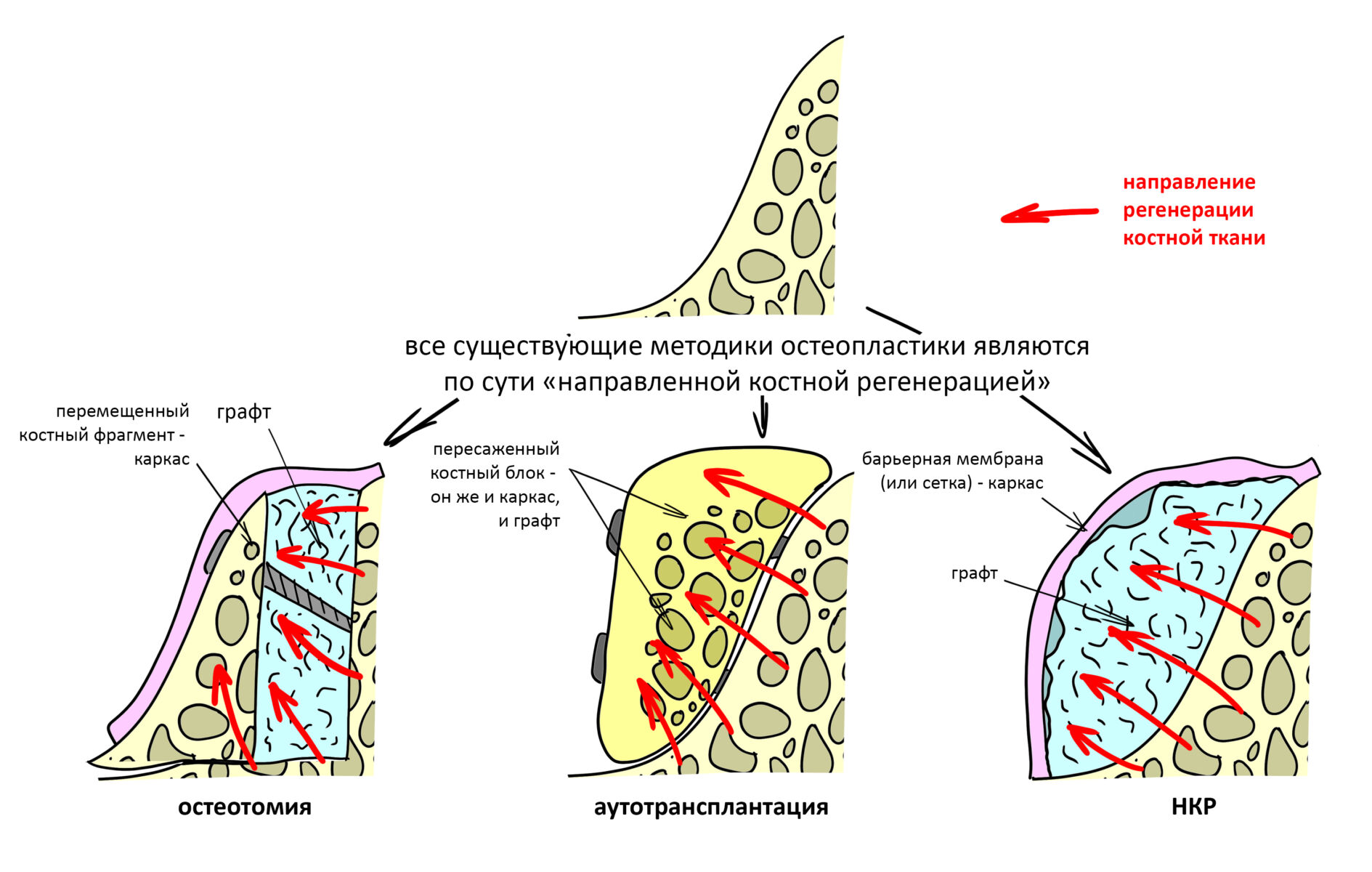
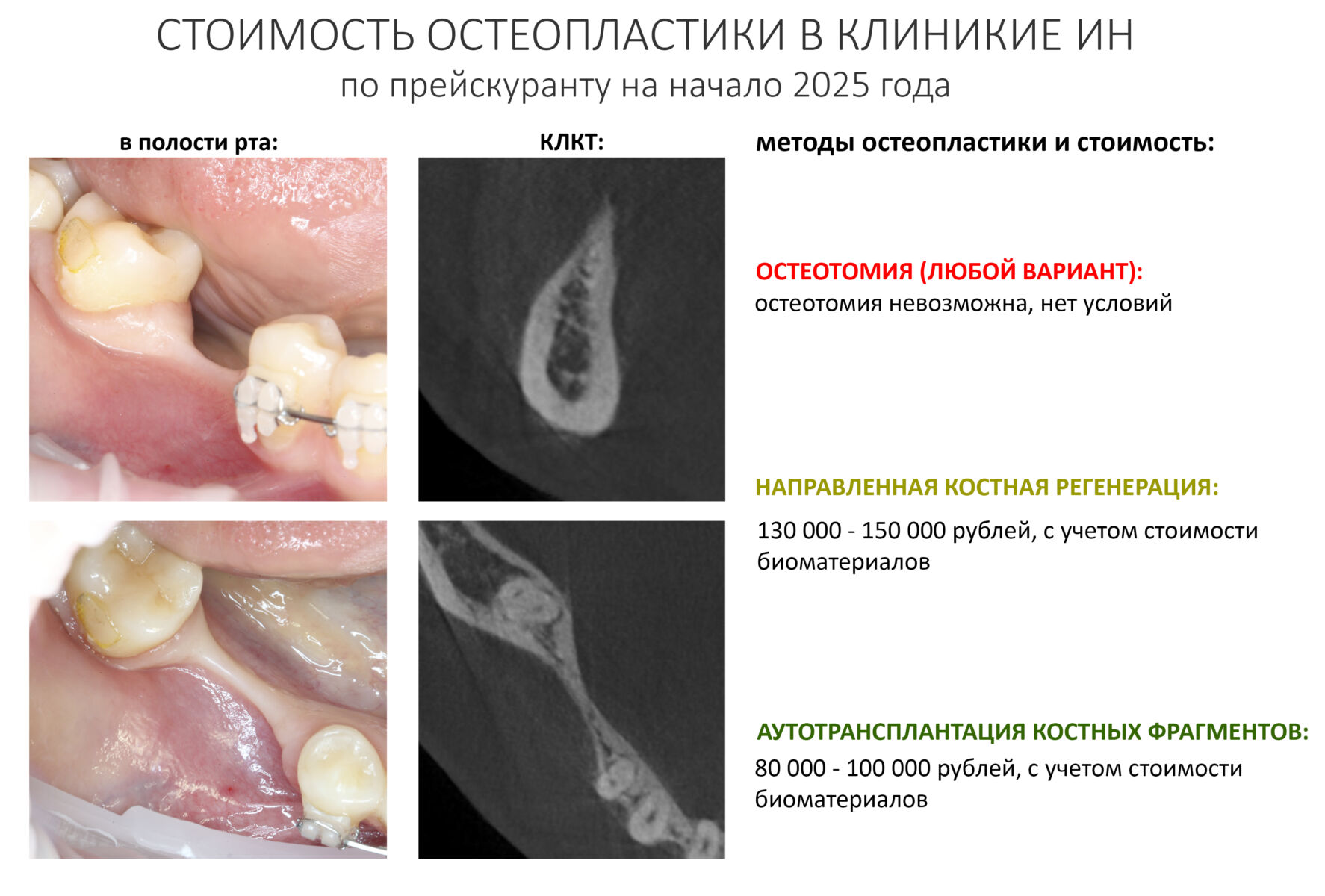
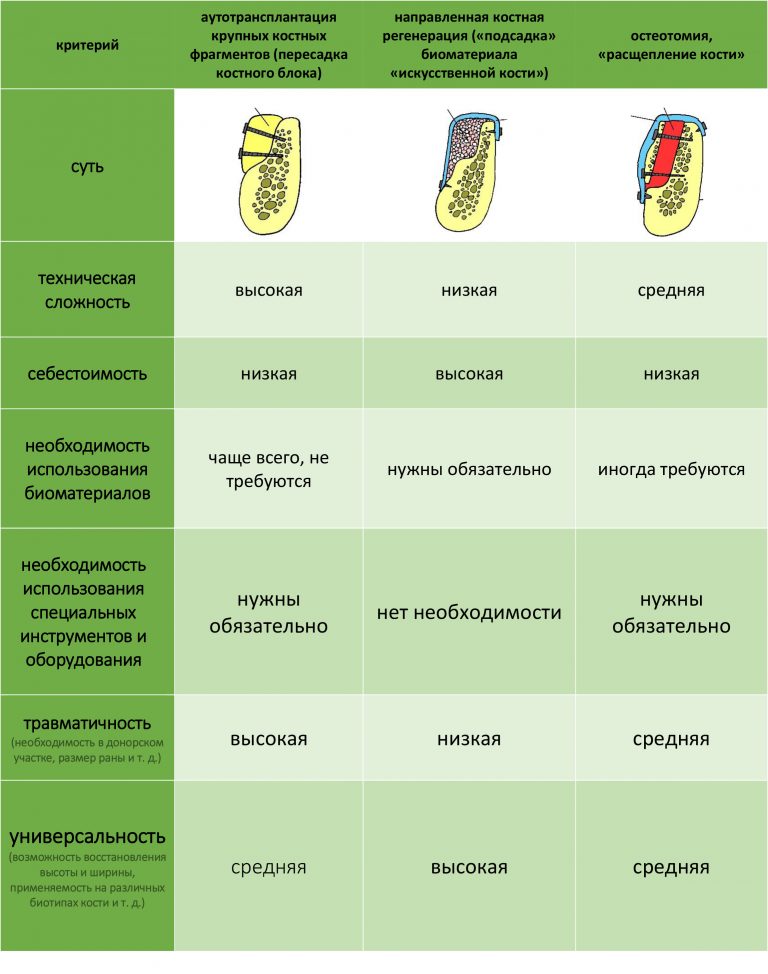
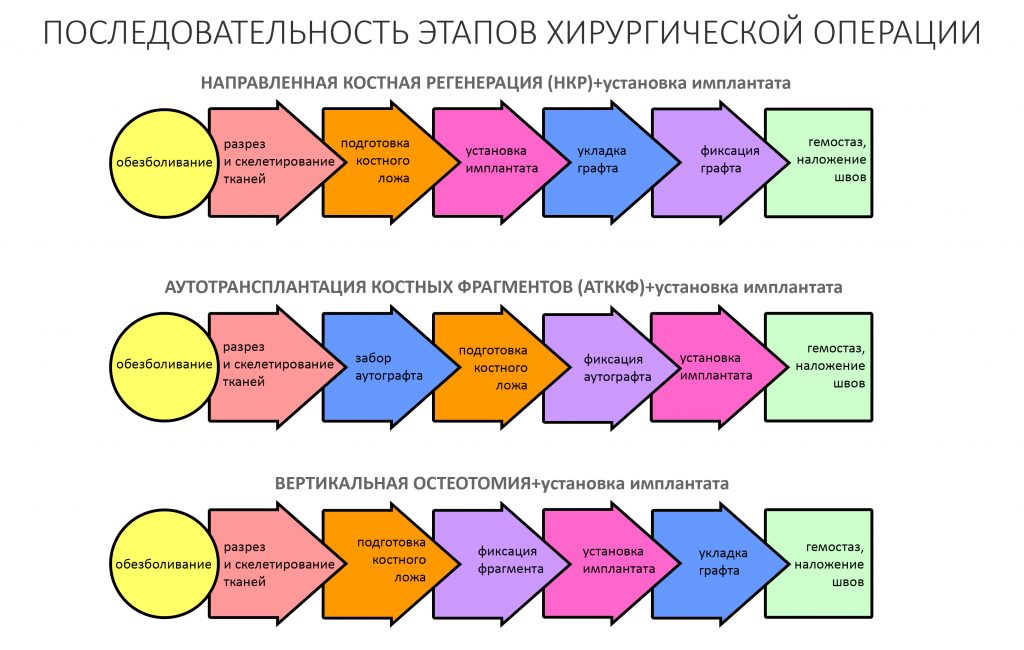
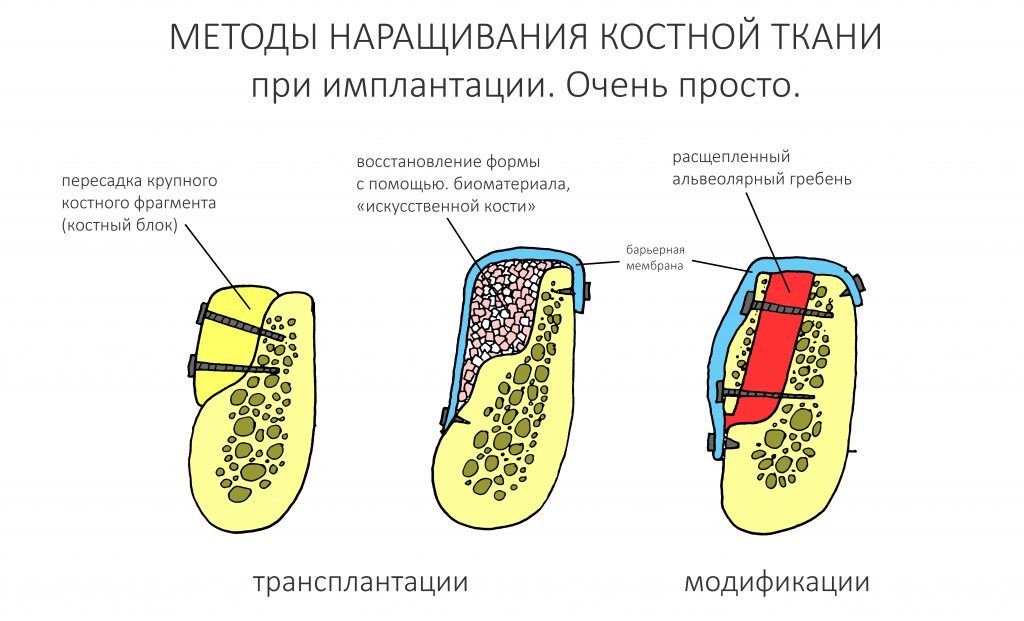
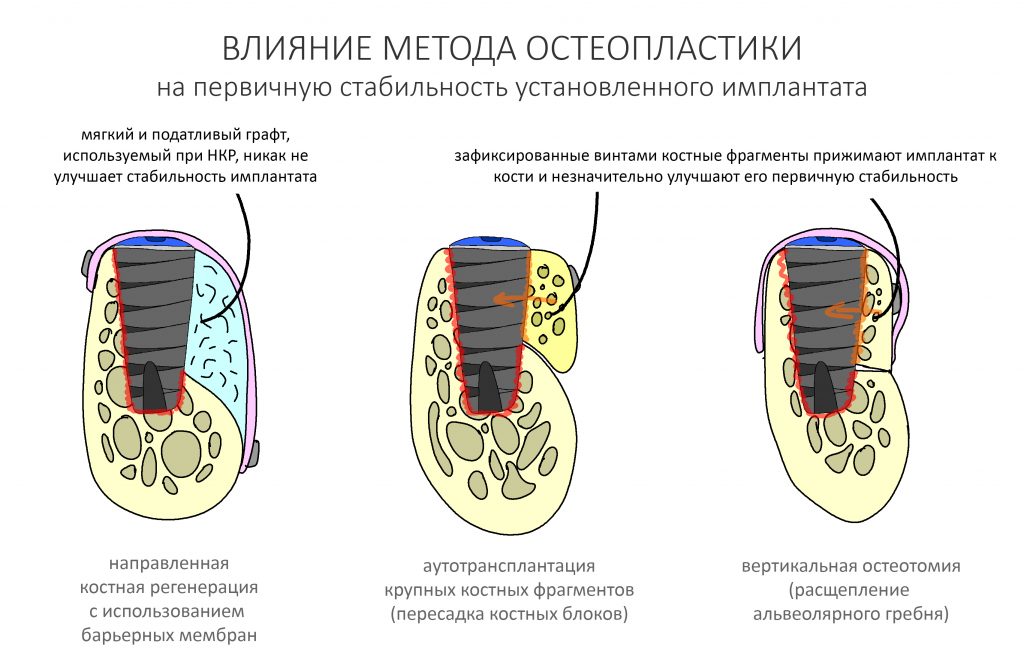
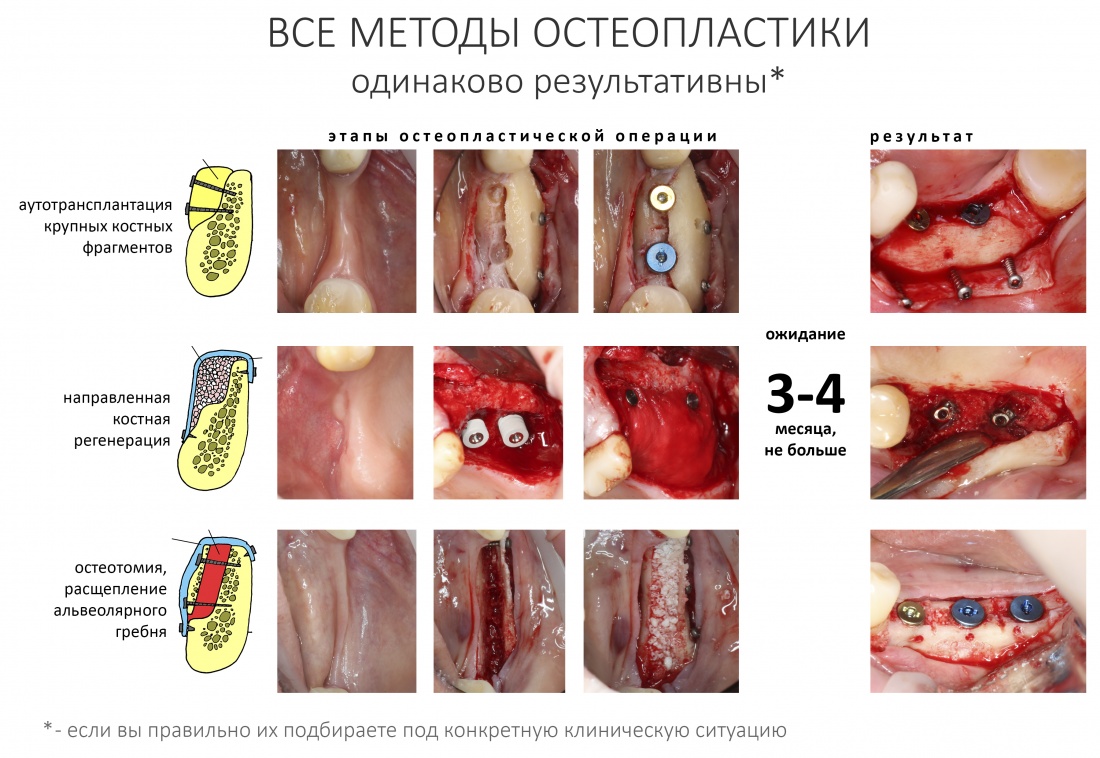
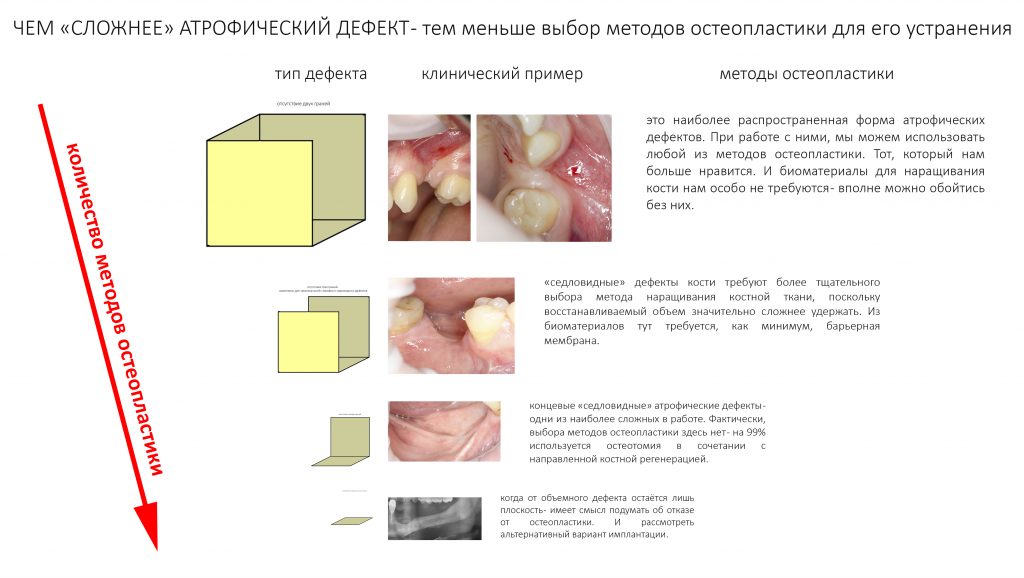
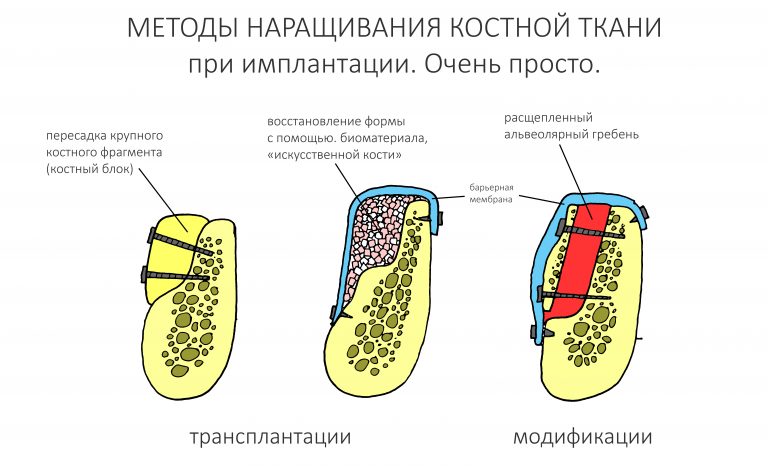
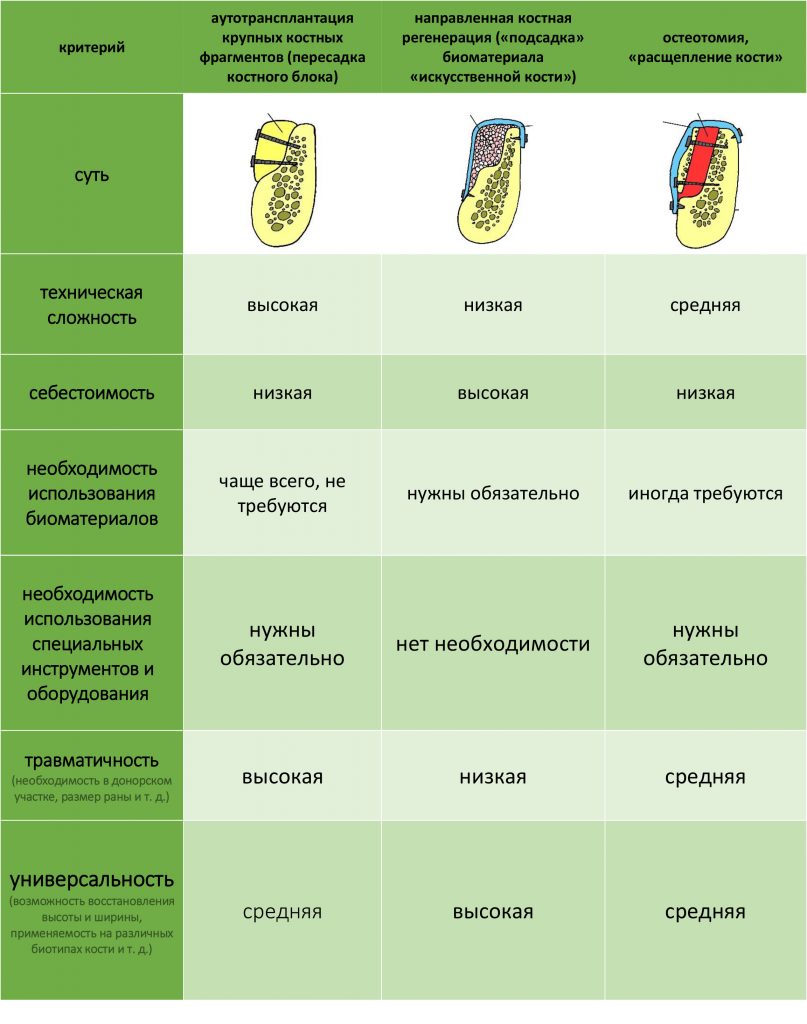
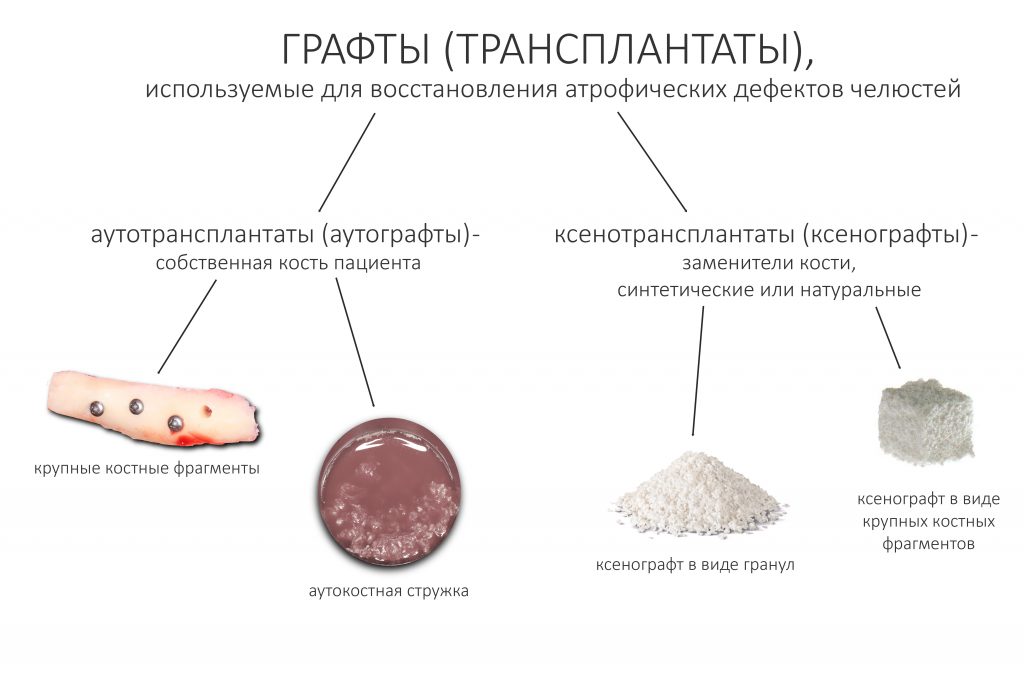
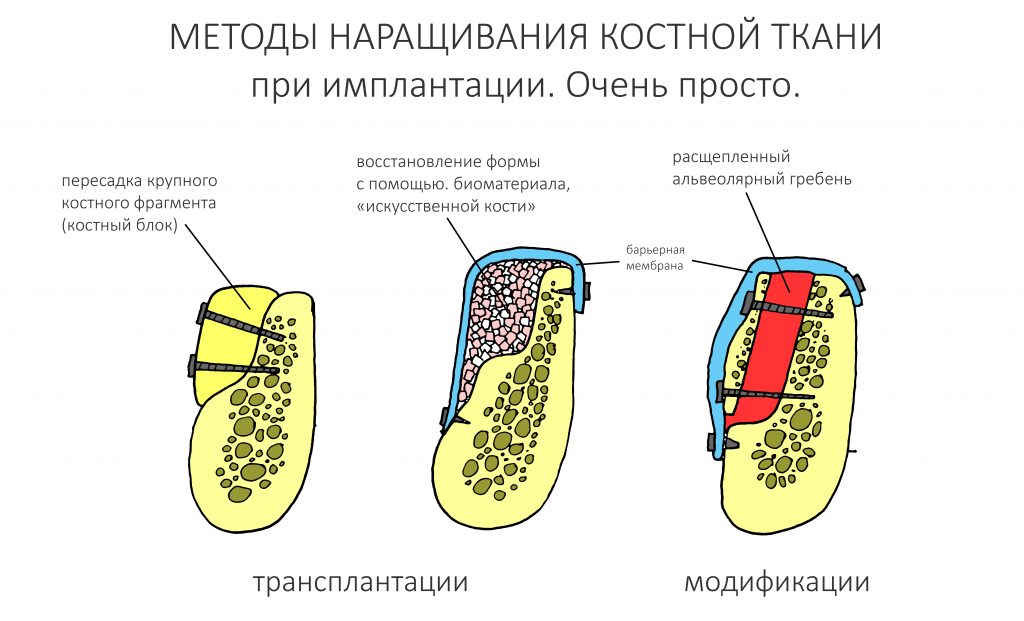
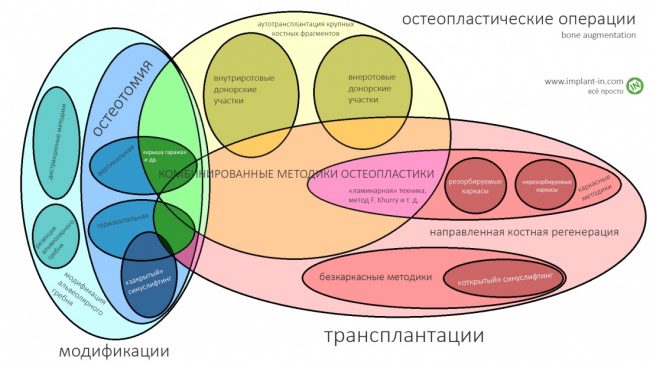
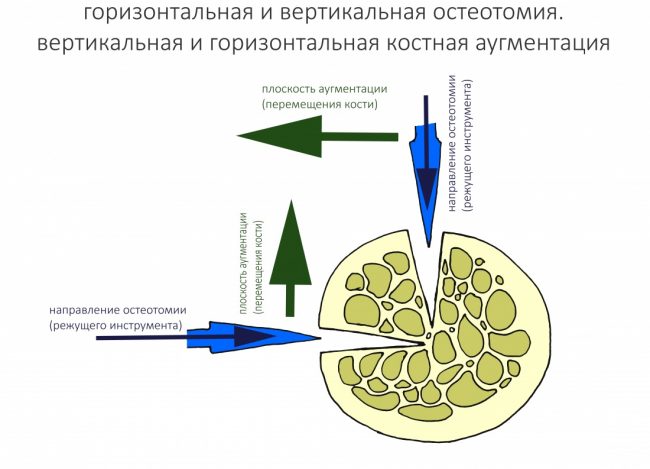
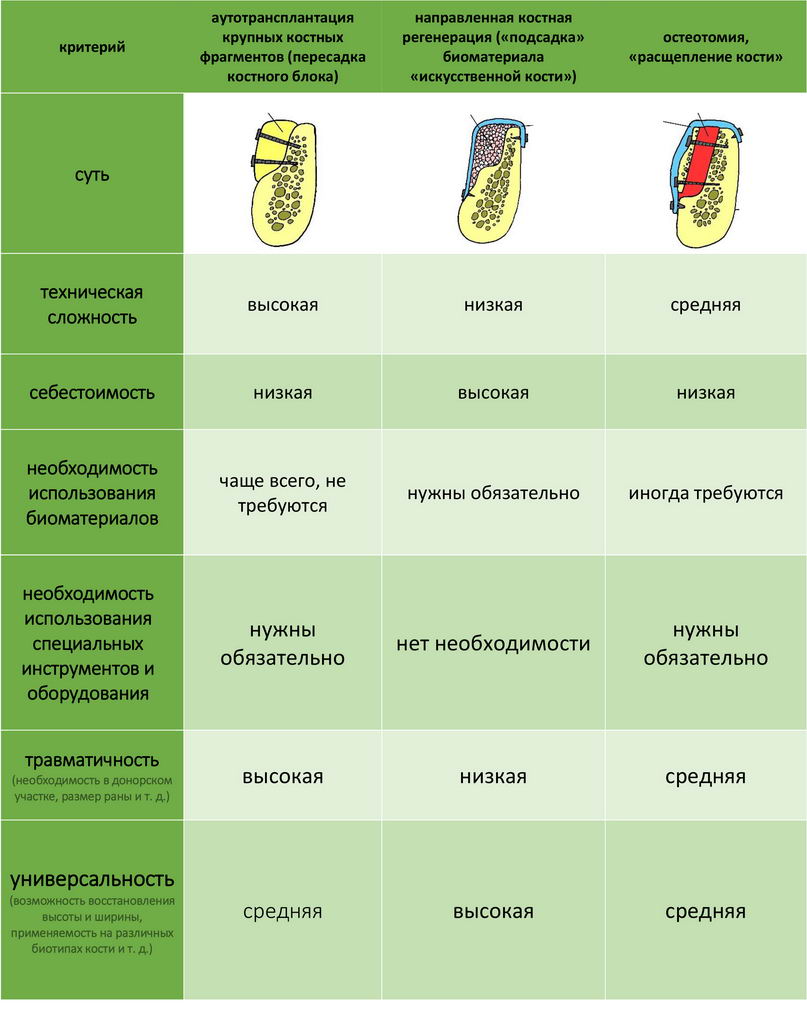
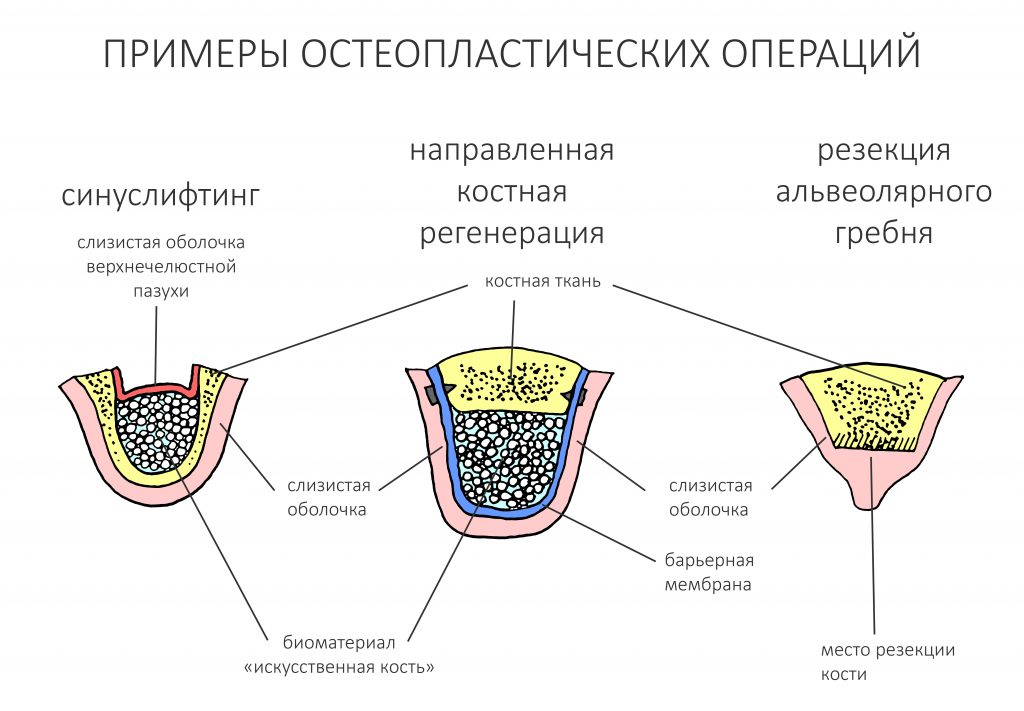
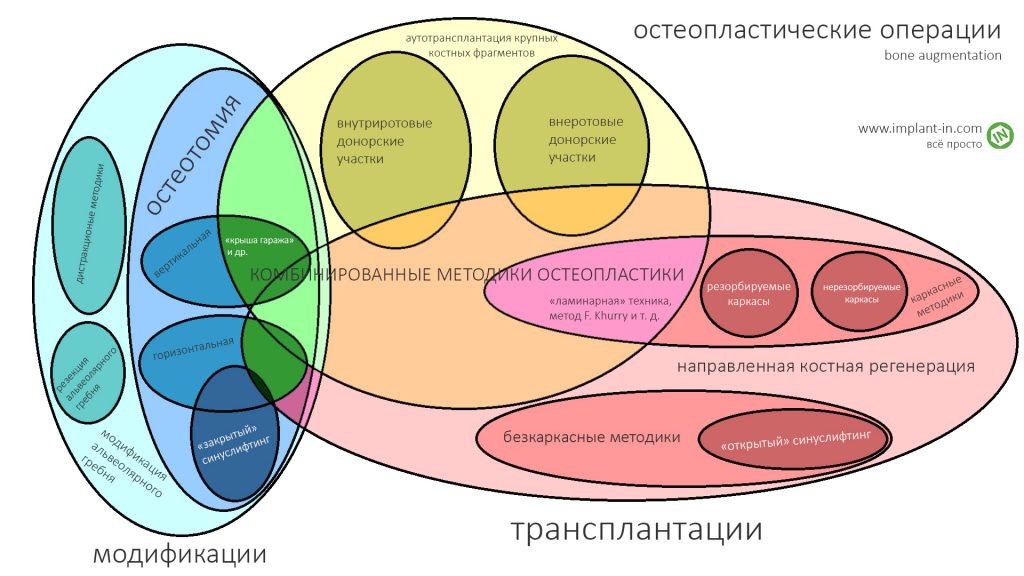
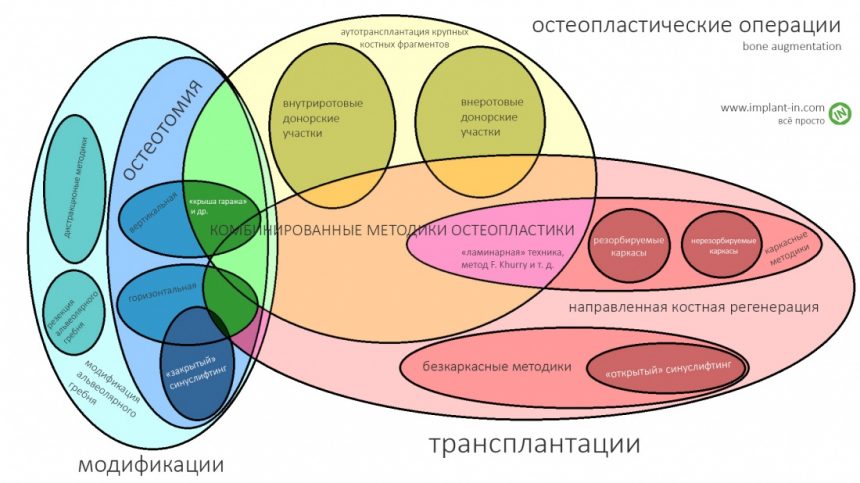
Если не считать комбинированных и суперпереусложненных методик, в нашем арсенале есть три базовых вида остеопластических операций (подробно — по ссылкам):
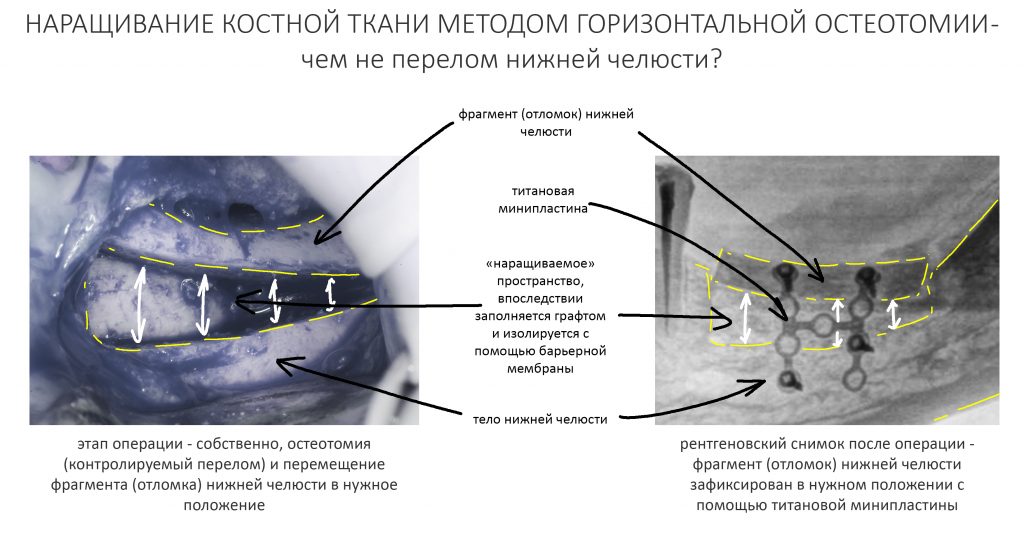
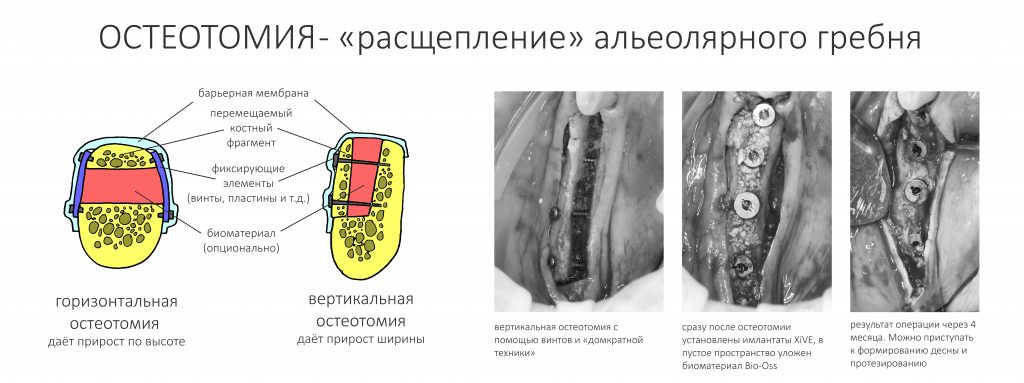
— остеотомия, расщепление альвеолярного гребня
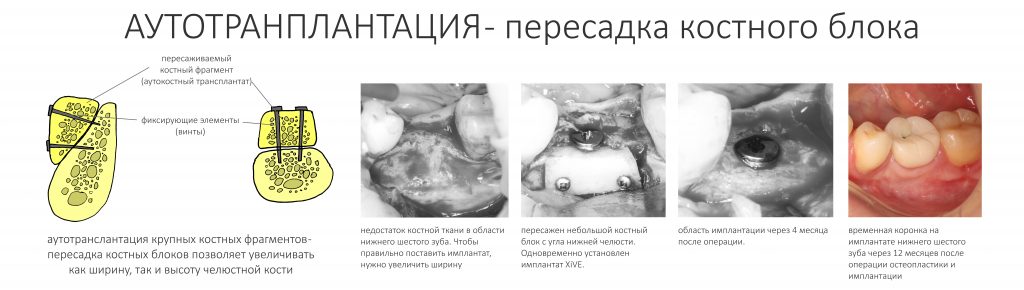
— аутотрансплантация крупных костных фрагментов, т. н. «пересадка костных блоков».
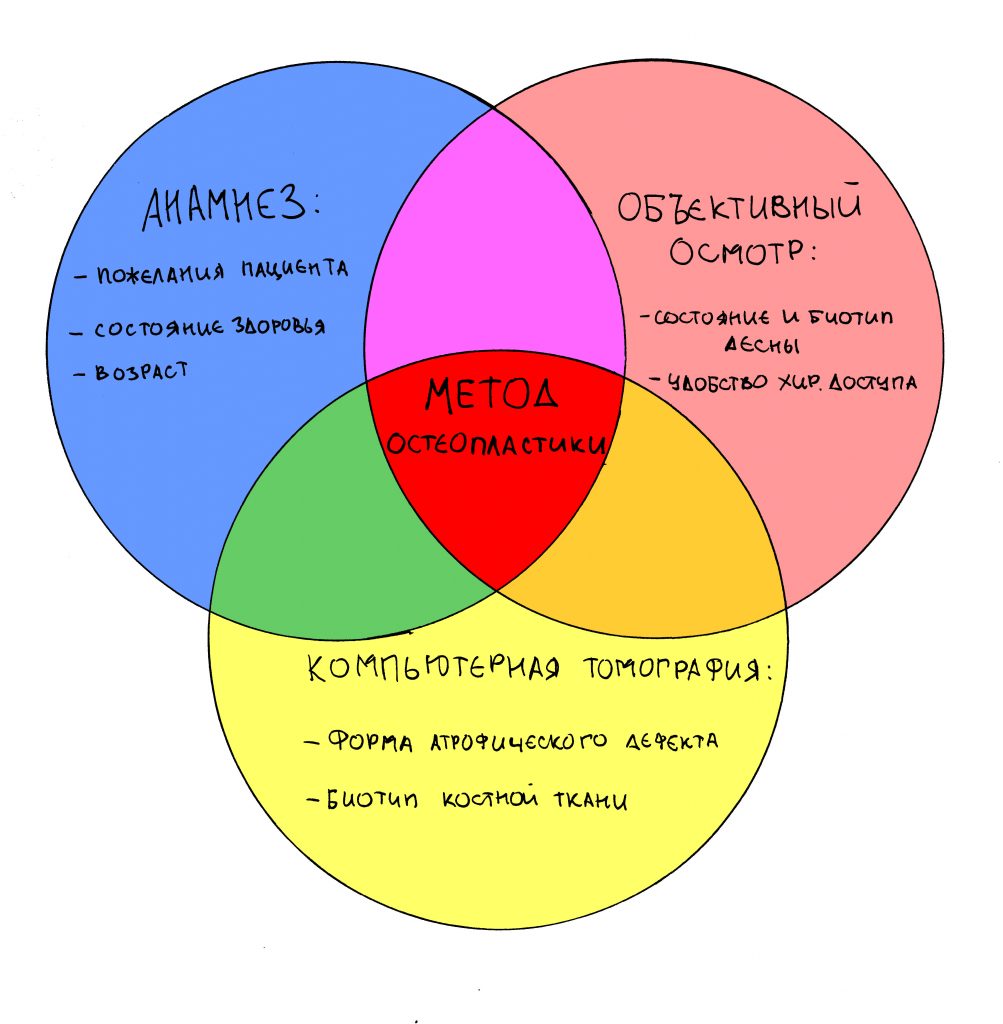
Тогда я рассуждал следующим образом.
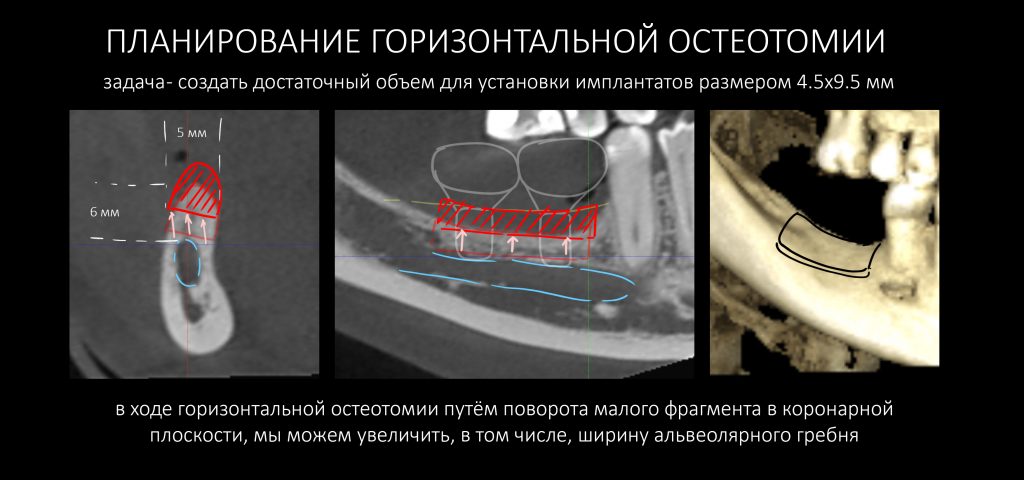
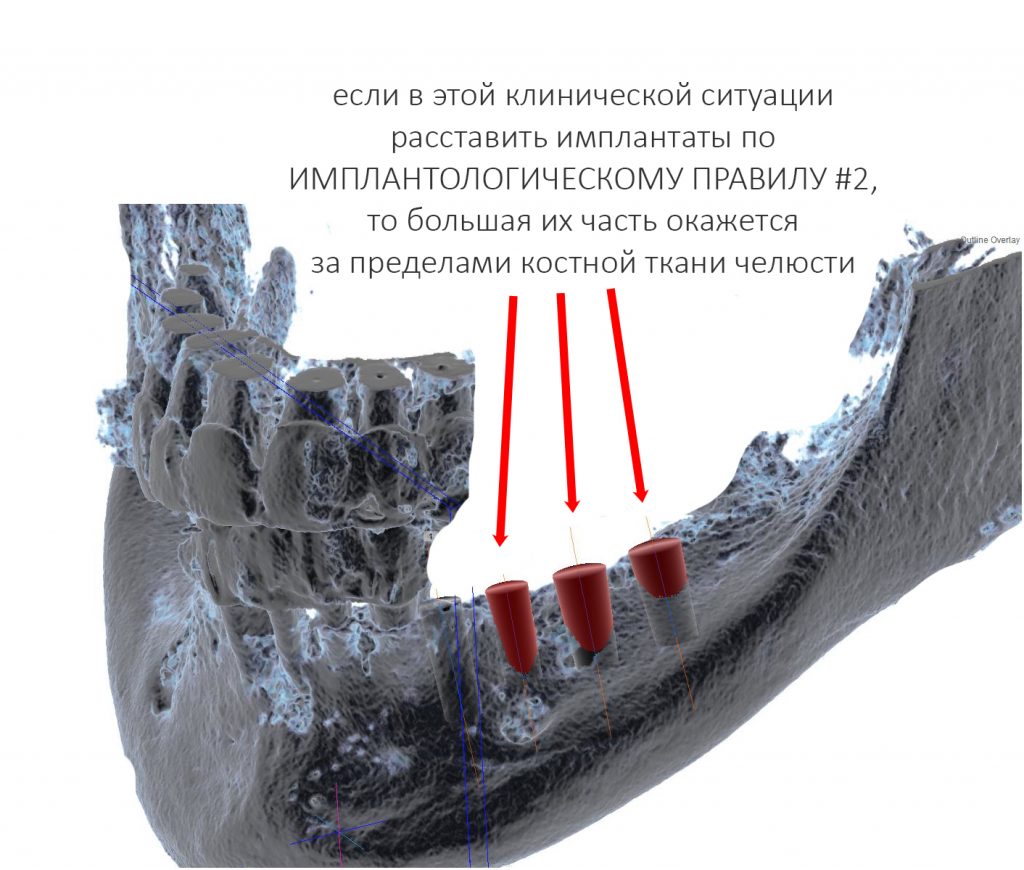
Остеотомия пролетает сразу, поскольку альвеолярный гребень такой ширины невозможно расщепить так, чтобы правильно установить имплантаты. Технически — да, но тогда имплантаты будут расположены слишком язычно, плюс риск атрофии тонкого вестибулярного фрагмента… Короче, не от случай для остеотомии.
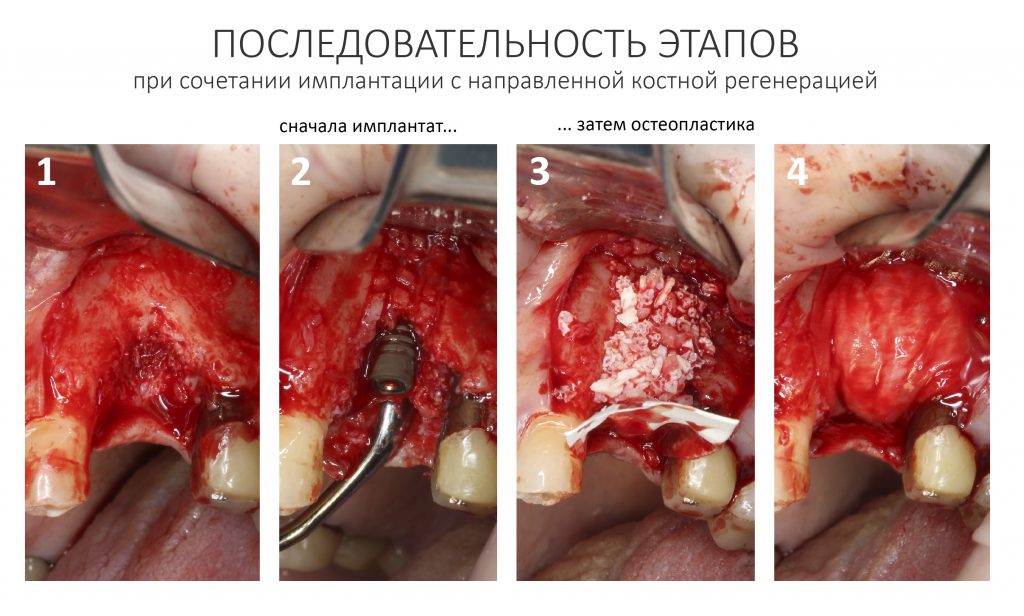
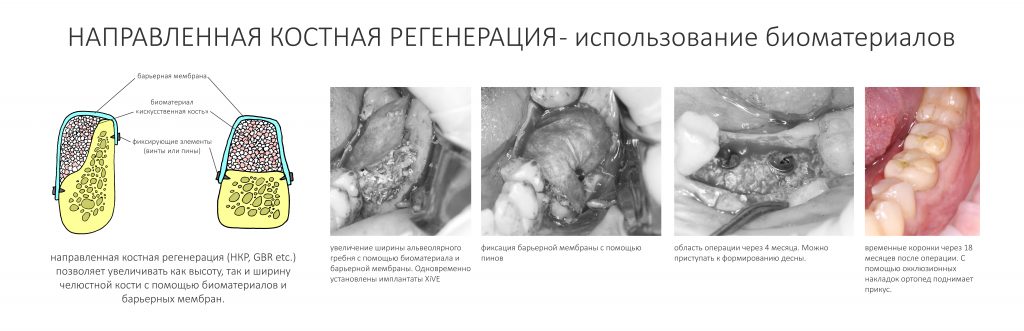
А вот направленная костная регенерация — это вариант. И по условиям, и по клинической ситуации. Правда, НКР получается примерно в полтора раза дороже и не улучшает стабильность имплантатов. Если бы у меня была ипотека и автокредит, а пациентка после операции находилась бы в зоне досягаемости, то этот метод остеопластики был бы оптимальным с точки зрения баланса сложность/травматичность/результат.
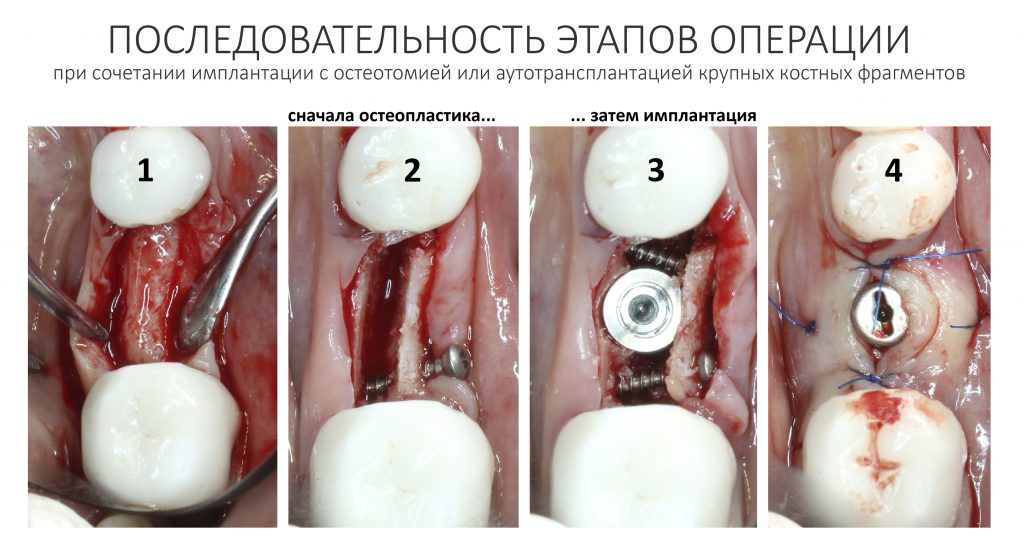
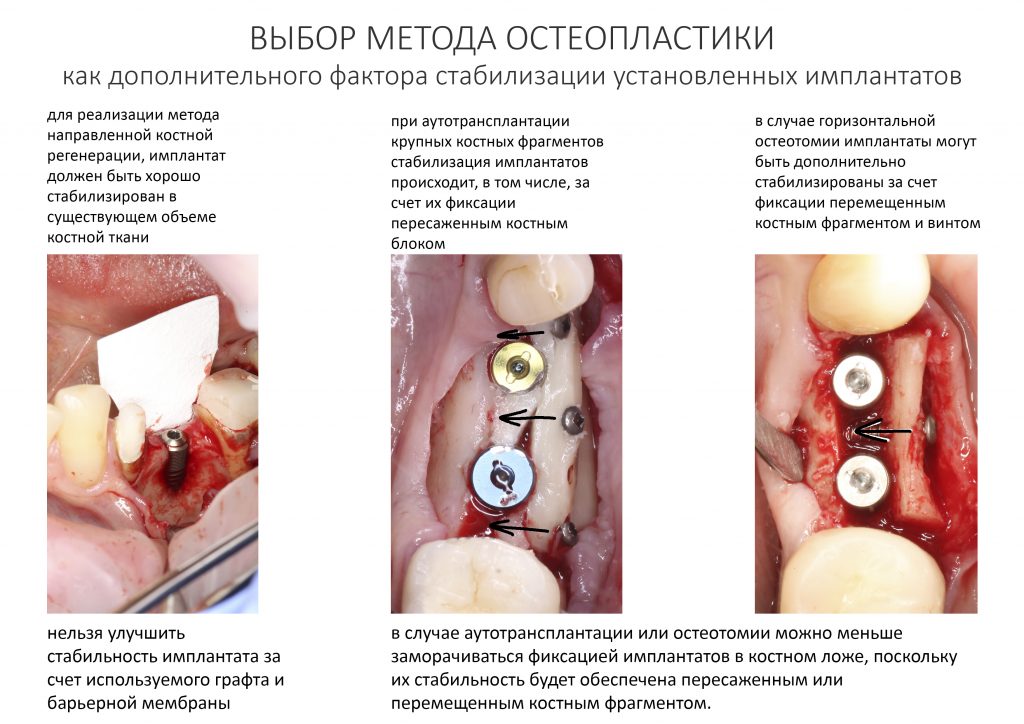
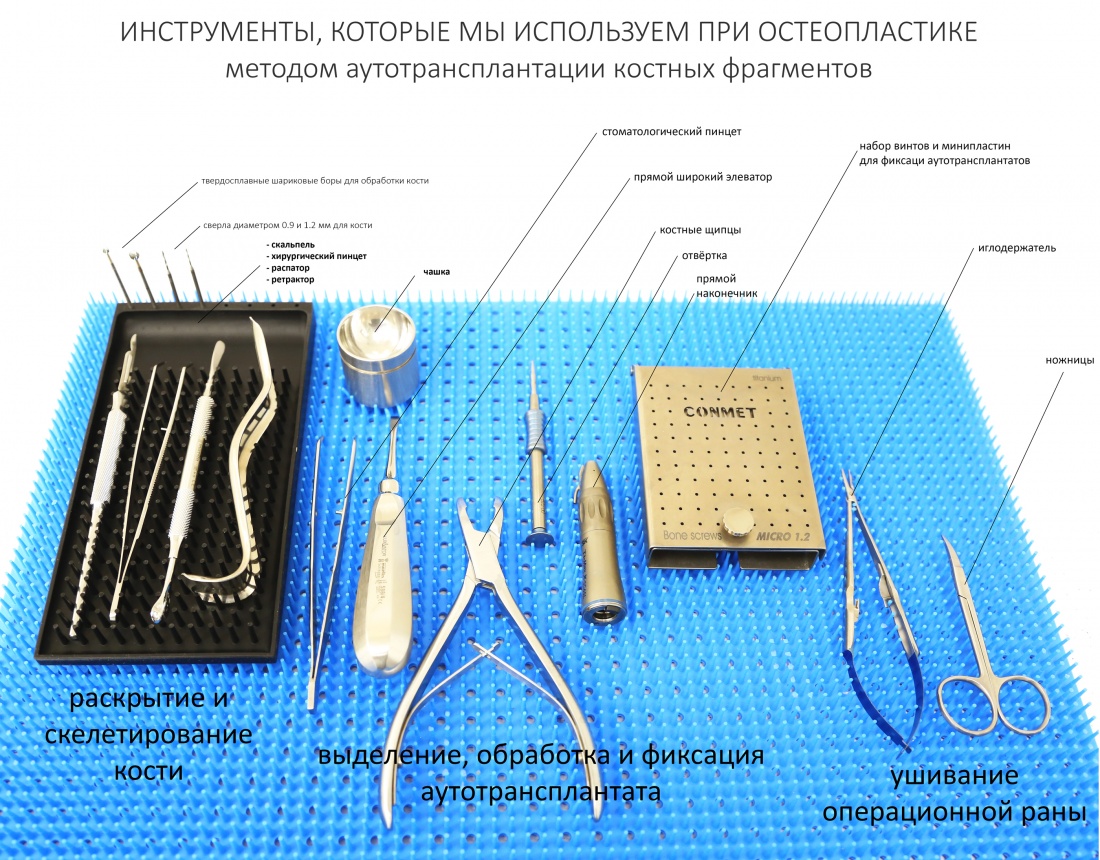
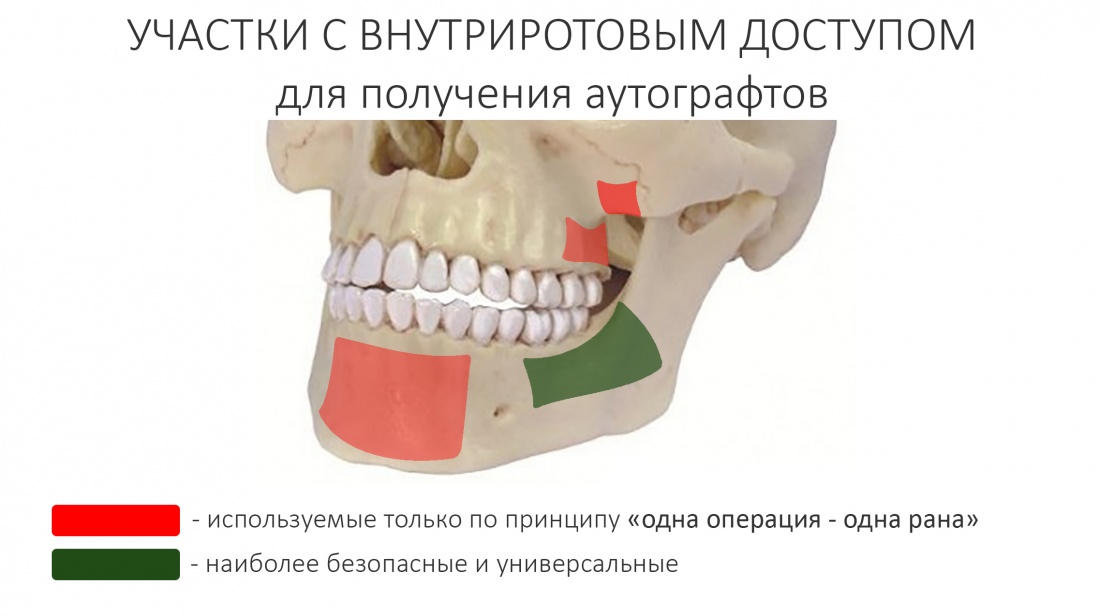
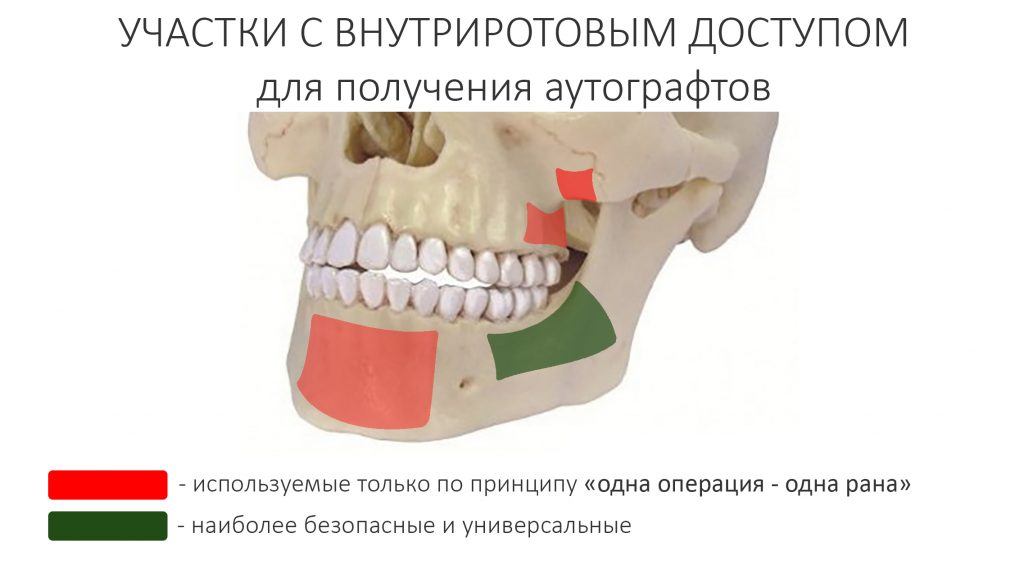
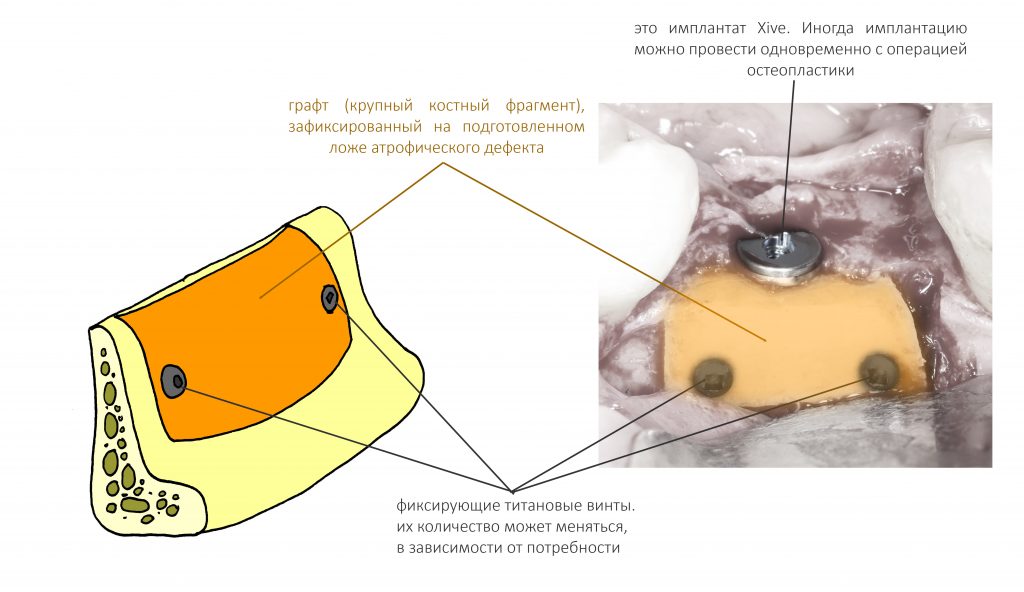
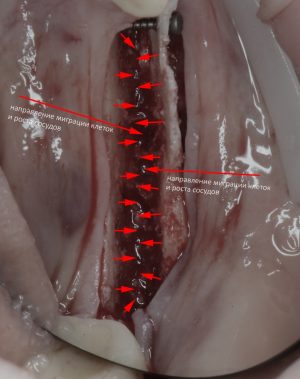
Остается одна методика, а именно — аутотрансплантация крупных костных фрагментов. Как и в случае с НКР, у нас есть и условия, и оптимальная клиническая ситуация. В частности, мы можем провести операцию по принципу «одной раны», что это очень важно. К тому же, АТККФ получается дешевле, позволяет улучшить стабилизацию имплантатов и, в целом, получается более предсказуемой и удобной конкретно в этом клиническом случае (с точки зрения «одной раны» и способов фиксации графта).
Итого, я остановился методе АТККФ как на наиболее дешевом, удобном и предсказуемом.
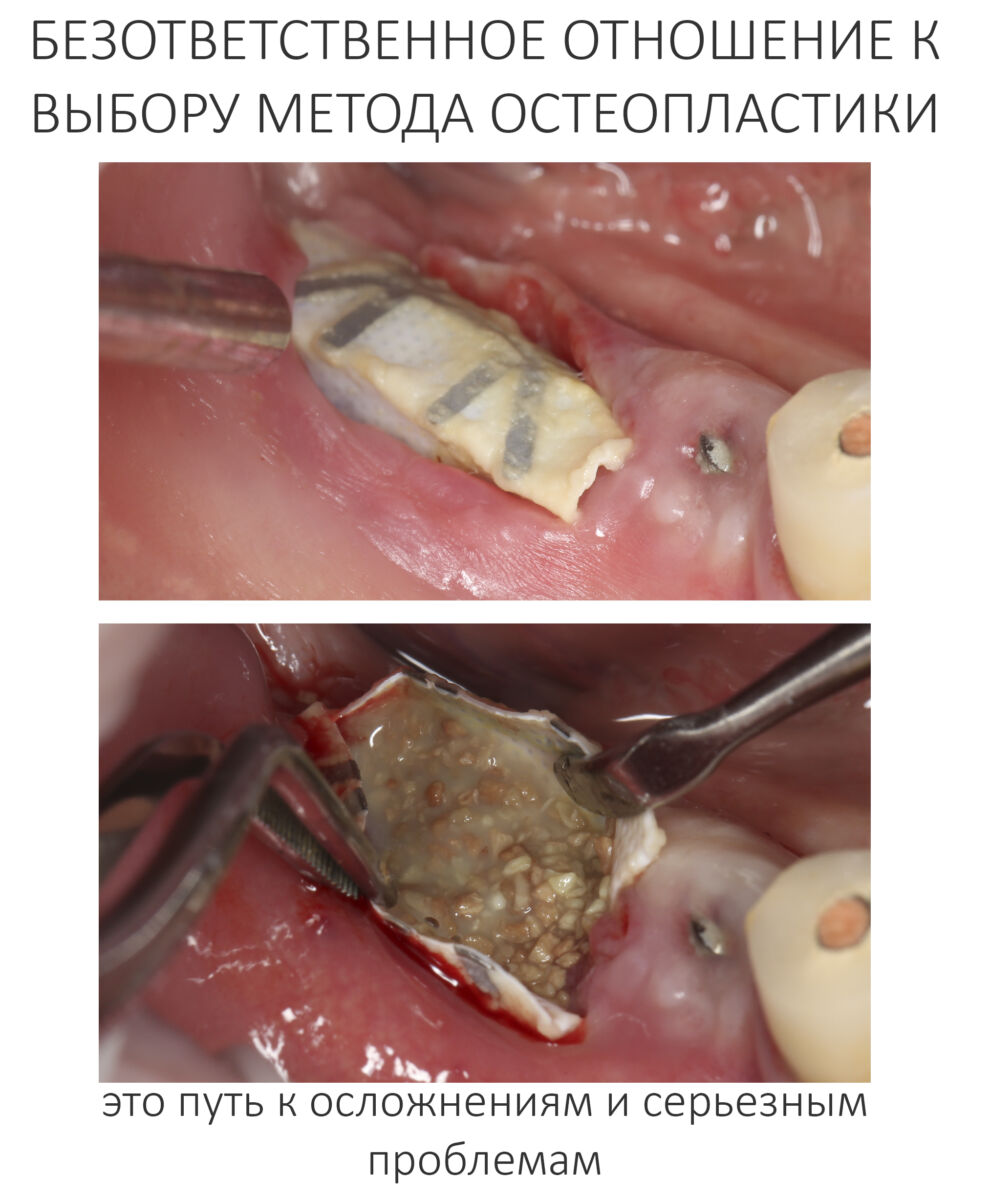
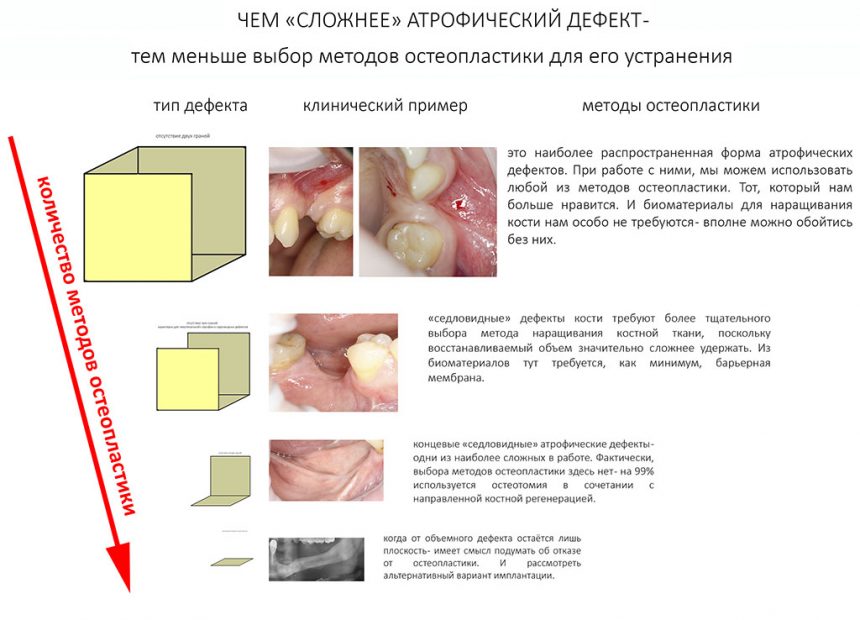
Вообще, про выбор метода остеопластики хорошо написано здесь>>
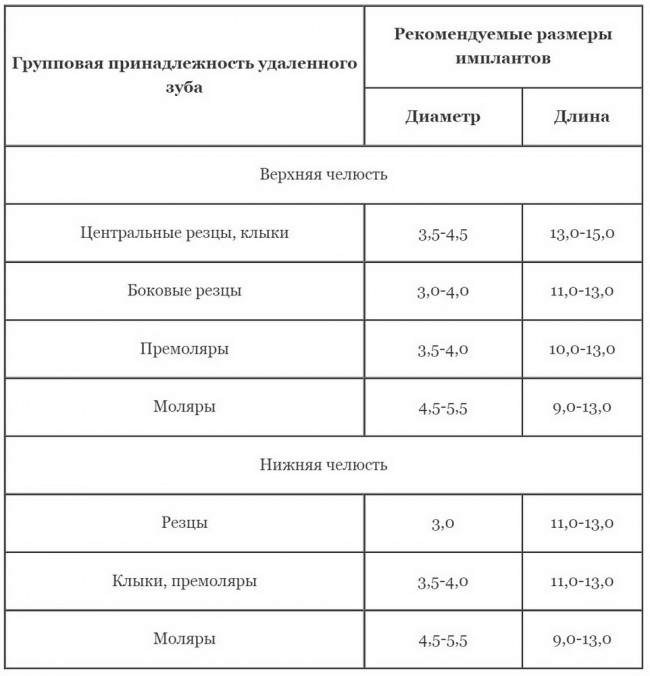
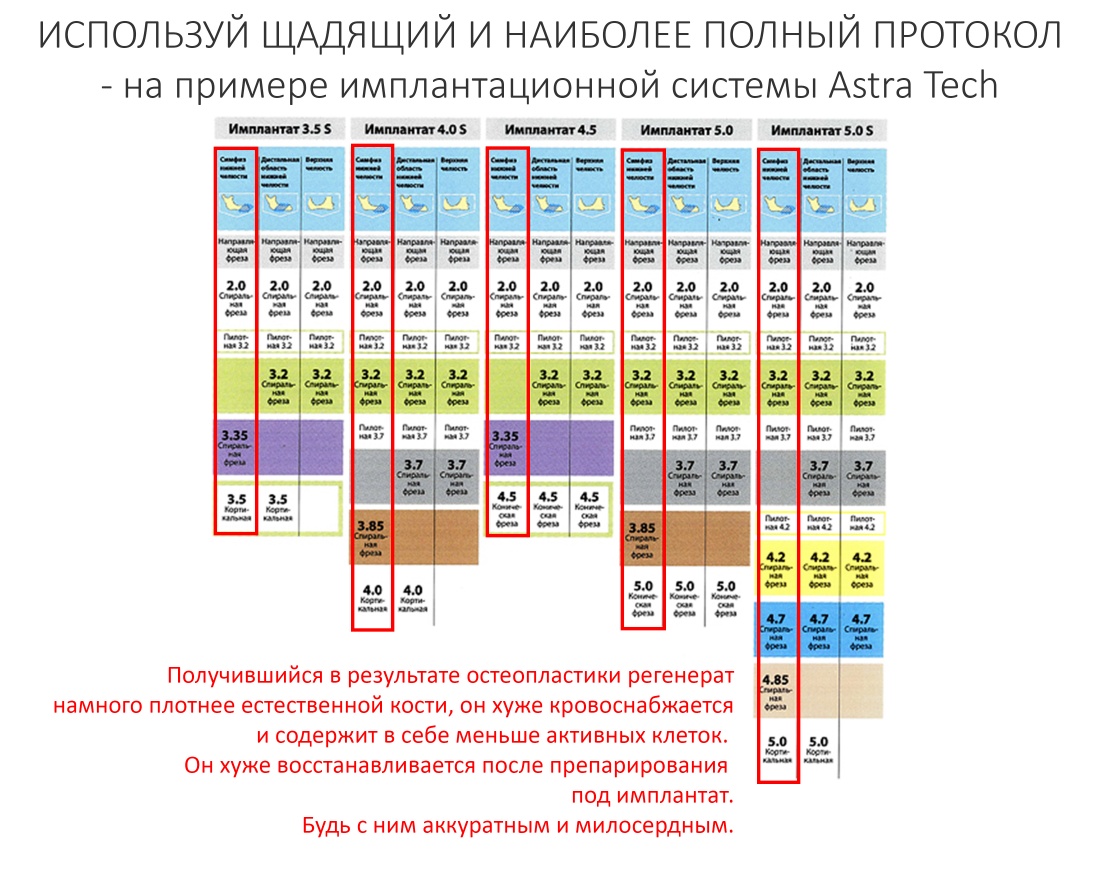
Выбор имплантатов
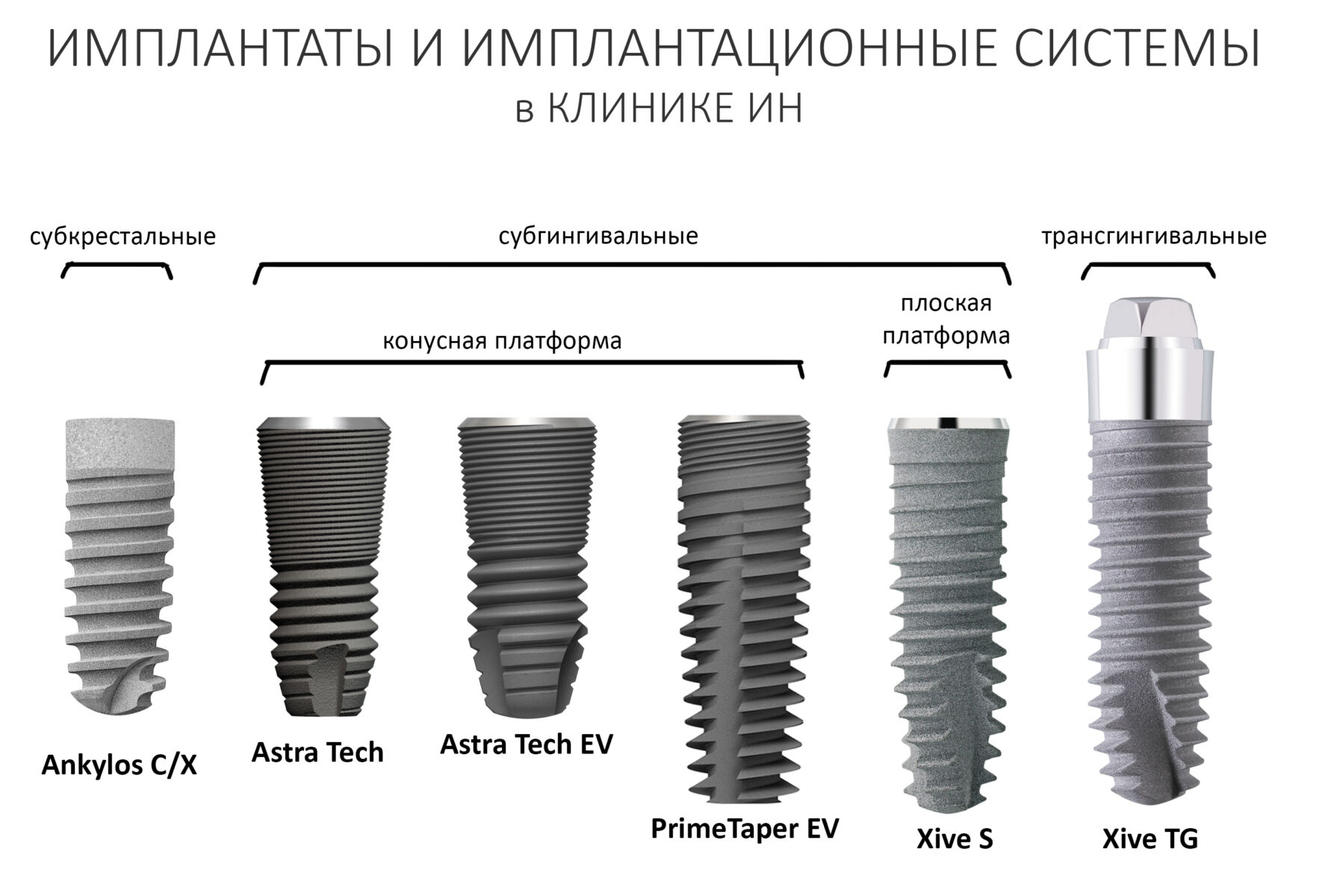
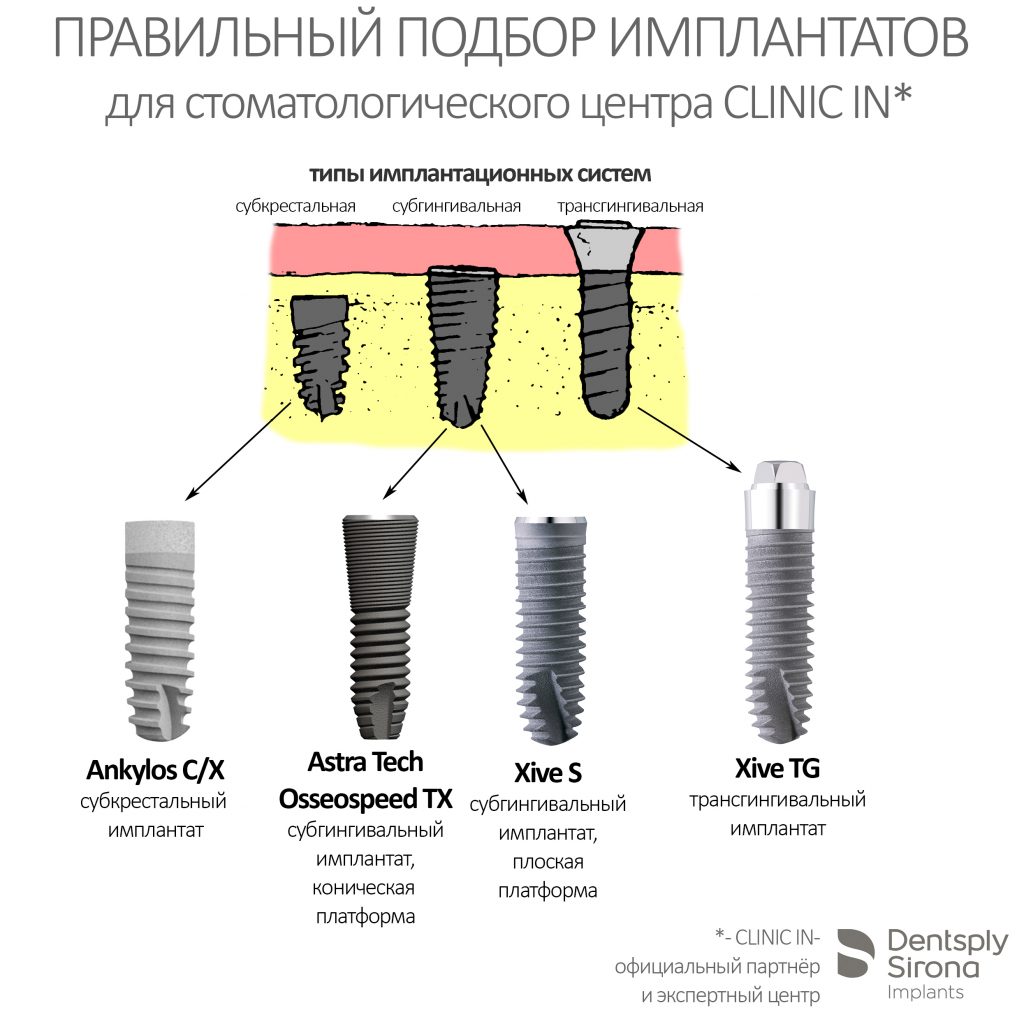
Сейчас в нашем арсенале есть аж пять имплантационных систем, включающих в себя имплантаты разных типов:
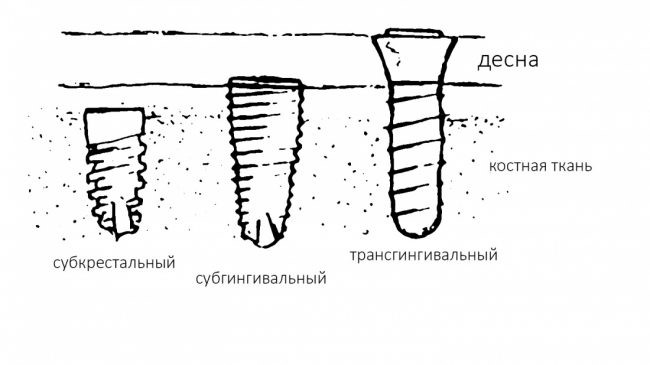
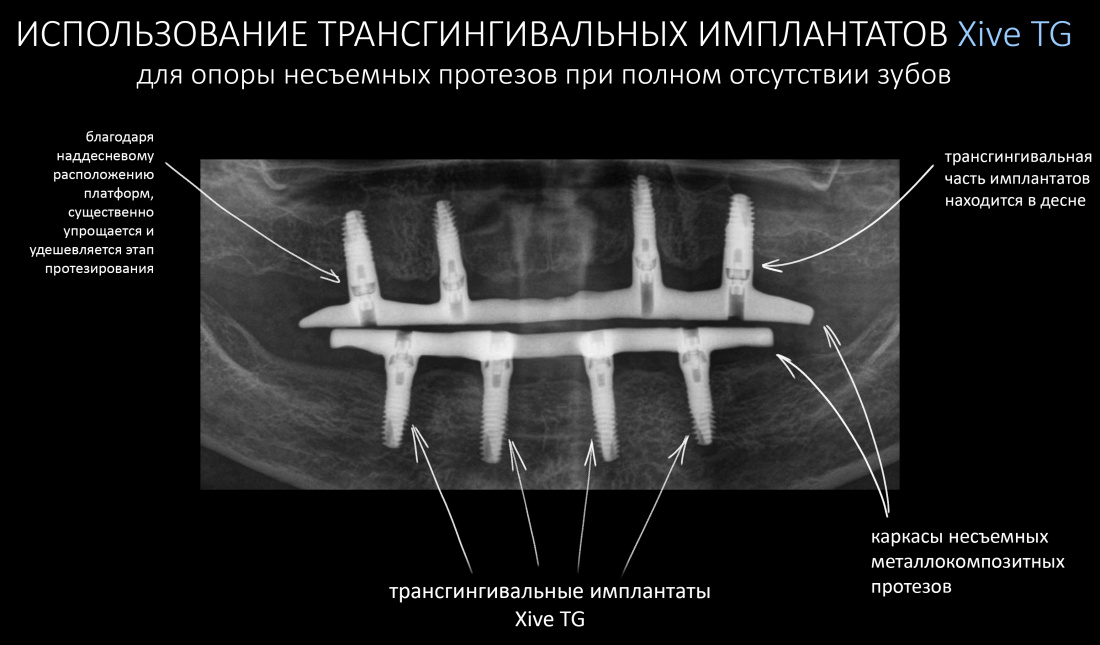
А тогда было две: субгингивальная Xive S и субкрестальная Ankylos C/X.
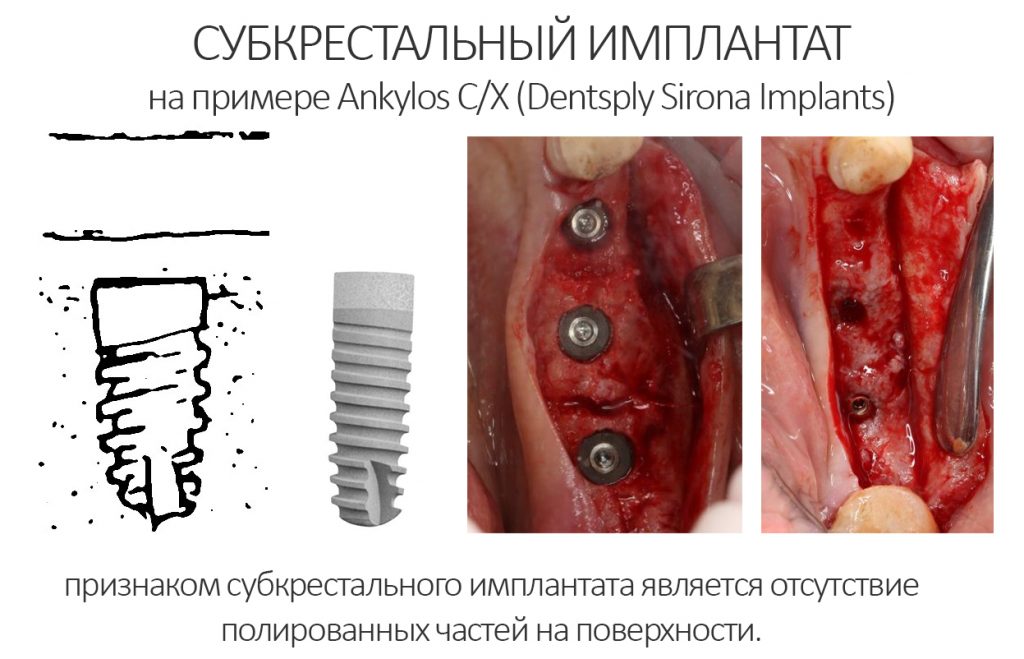
Безусловно, субгингивальные имплантаты удобнее во всех отношениях, но… после остеопластики сложно спрогнозировать уровень атрофии кости в послеоперационном участке и угадать с правильным положением платформы. К тому моменту у меня уже был опыт подобных операций, в т. ч. с субгингивальными имплантатами, но не при такой конфигурации альвеолярного гребня и не при таком объемном костном дефекте.
Платформу субкрестальных имплантатов можно позиционировать, что называется, » с запасом» — заглубить её в кость на 3-4 мм. Даже в случае интенсивной постоперационной атрофии, она останется в правильном положении, и у нас сохранятся все условия для получения хорошего результата лечения.
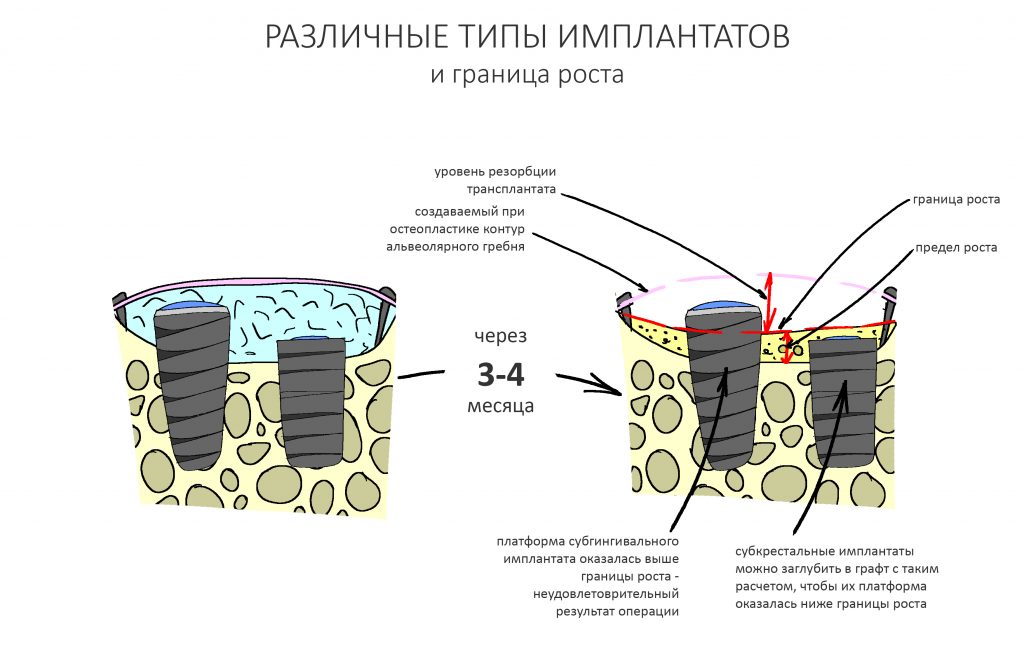
В общем, Ankylos С/X — это мой выбор конкретно в этой клинической ситуации.
Как показало дальнейшее развитие событий, выбор абсолютно правильный.
Знакомство и консультация.
Наперво — консультация. Как и было оговорено инструкцией, Зинаида приехала в Москву на несколько дней, поселилась в гостинице недалеко от нашей клиники.
Наконец, мы с ней познакомились очно, побеседовали и обсудили нюансы предстоящей операции. Зинаида согласилась с моим доводами и напоследок сказала:
— Доктор, я летела к вам две тысячи километров. Мне вас рекомендовали серьезные люди, я вам полностью доверяю. Делайте всё, что посчитаете нужным.
Нельзя подводить серьезных людей. Надо оправдать выданный мне кредит доверия.
Мы назначили операцию на следующий день.
Ход операции.
Для начала, я процитирую умного человека (А. Кутин «Хирургия остеомиелита»):
Планирование операции всегда сложнее, чем сама операция.
Поскольку всё у нас было распланировано и согласовано, операция действительно получилась несложной.
Анестезия.
Подобные операции можно и нужно проводить под местной анестезией. Совершенно точно, они не требуют ни наркоза, ни седации. И вот, почему:
Во-первых, это непродолжительное хирургическое вмешательство. На полтора часа, максимум. Местная анестезия действует значительно дольше.
Во-вторых, всё хирургическое вмешательство проходит в одном участке зубного ряда. Его можно обезболить минимальным количеством анестетика. В нашем случае потребовалось 6.8 мл Ультракаина Д-С форте. Всего 4 карпулы.
В-третьих, для работы в этой зоне требуется содействие пациента во время операции: открыть-закрыть рот, повернуть, зафиксировать голову и т. д. Для этого с пациентом нужно общаться, а для общения он должен быть в сознании. «Выключение» пациента не позволяет этого сделать. И это, как ни странно значительно усложняет хирургическое вмешательство.
В-четвертых, безопасность. Ты и сам знаешь, что наркоз нифига не полезен. Помимо этого, он превращает пациента в неконтактный кусок мяса, что развязывает хирургу руки и позволяет делать то, что он никогда бы не сделал человеку в сознании. Хирург теряет осторожность и даже страх — а это уже прямой путь к беде.
В-пятых… в-пятых, наркоз в амбулаторной стоматологии используют только мудаки. Почему? Читай здесь>>
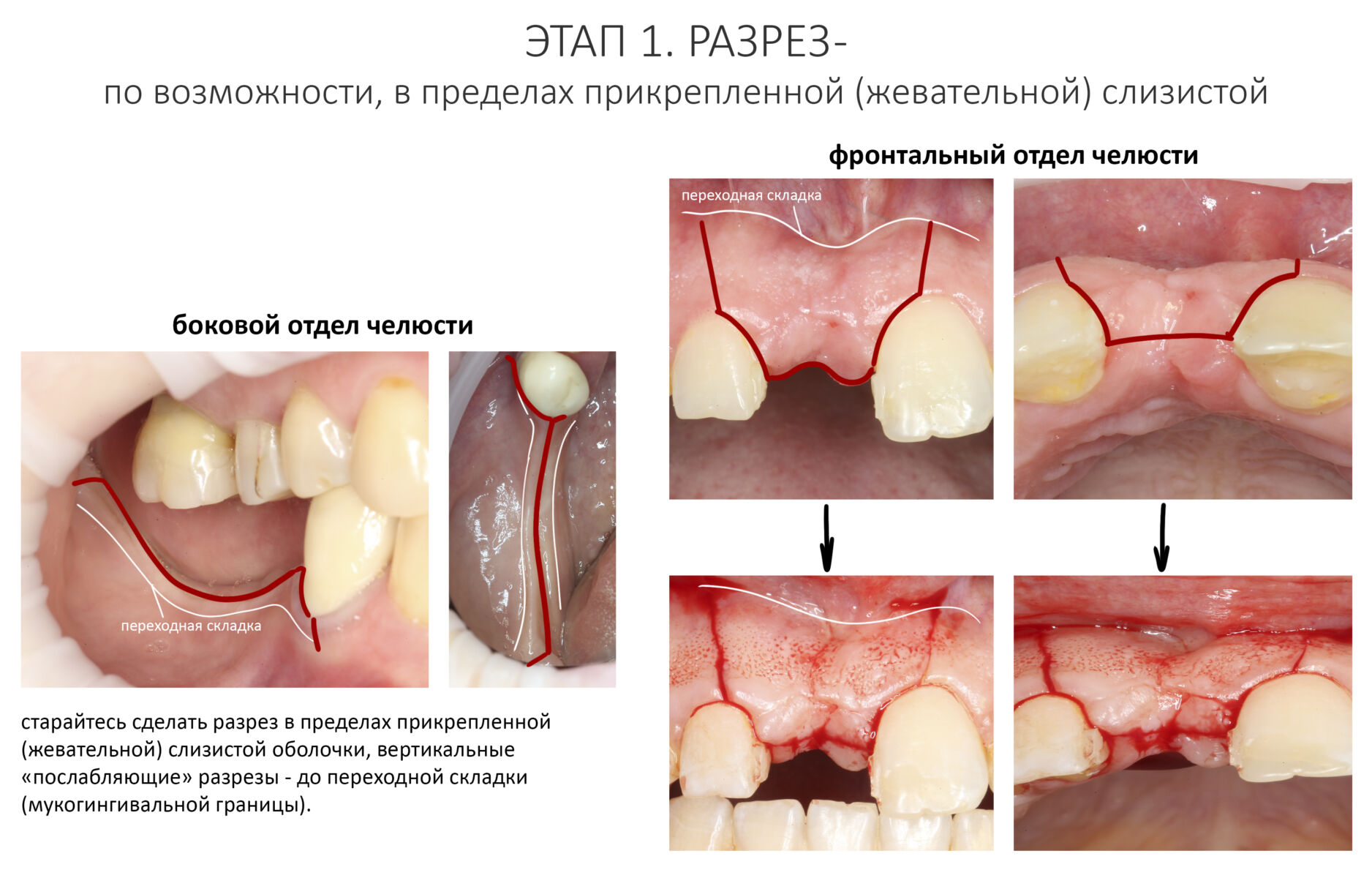
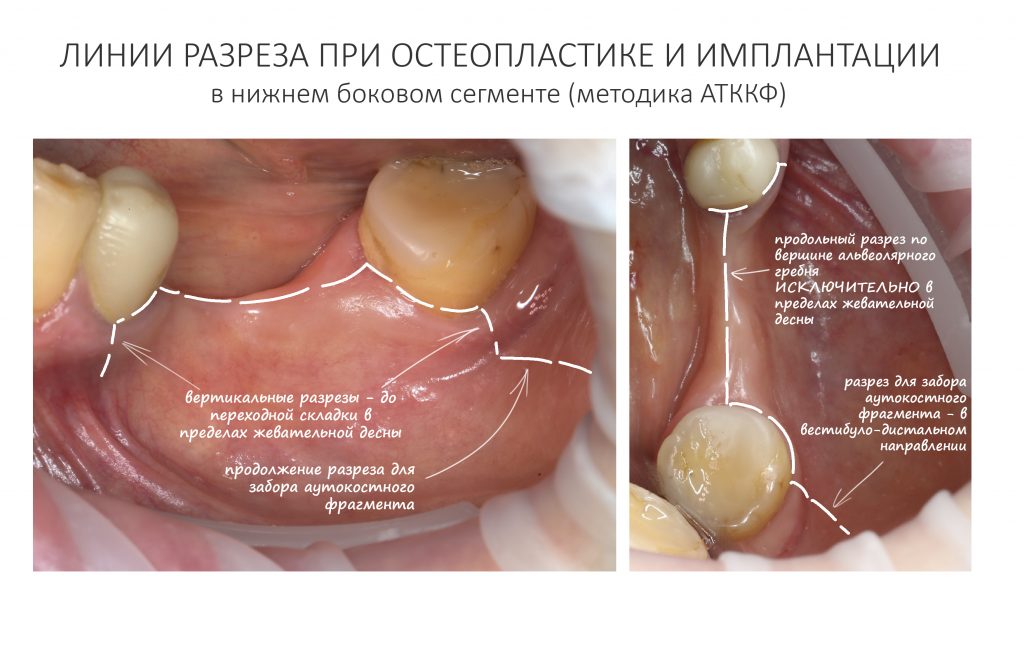
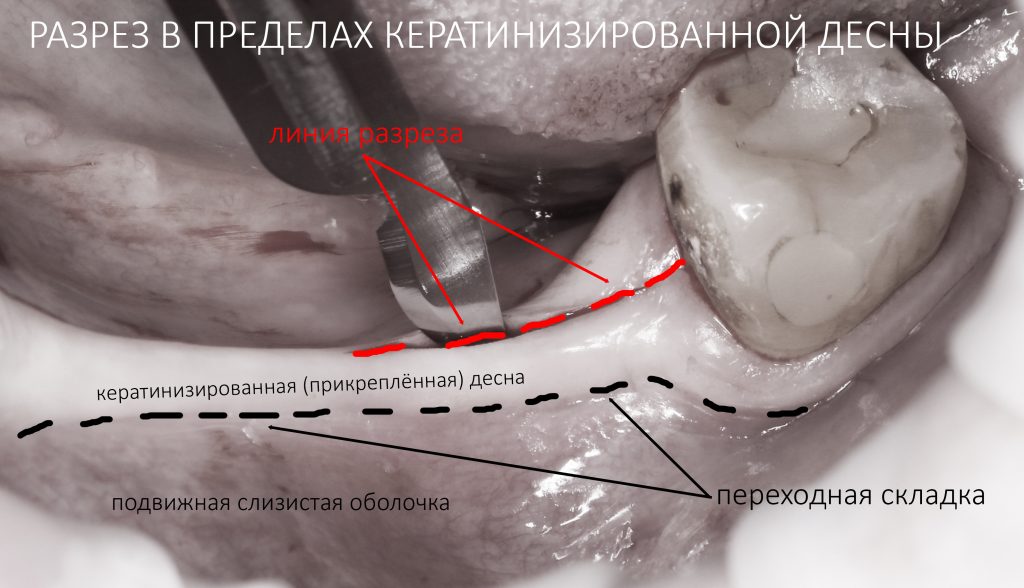
Разрез.
На этапе разреза делают дофига ошибок, что приводит к излишней травматичности вмешательства, сложностям при ушивании раны, расхождению швов и т. д. В общем, к нему нельзя относиться пофигистически.
Ремарка: еще на этапе консультации с участием стоматолога-ортопеда, мы признали 44 зуб негодным и решили его удалить. Перед проведением разреза мы убрали коронку с 44 зуба и подготовили его к удалению. Так мы избежим попадания фрагментов коронки в открытую рану, а проведение самого разреза получится проще и аккуратнее.
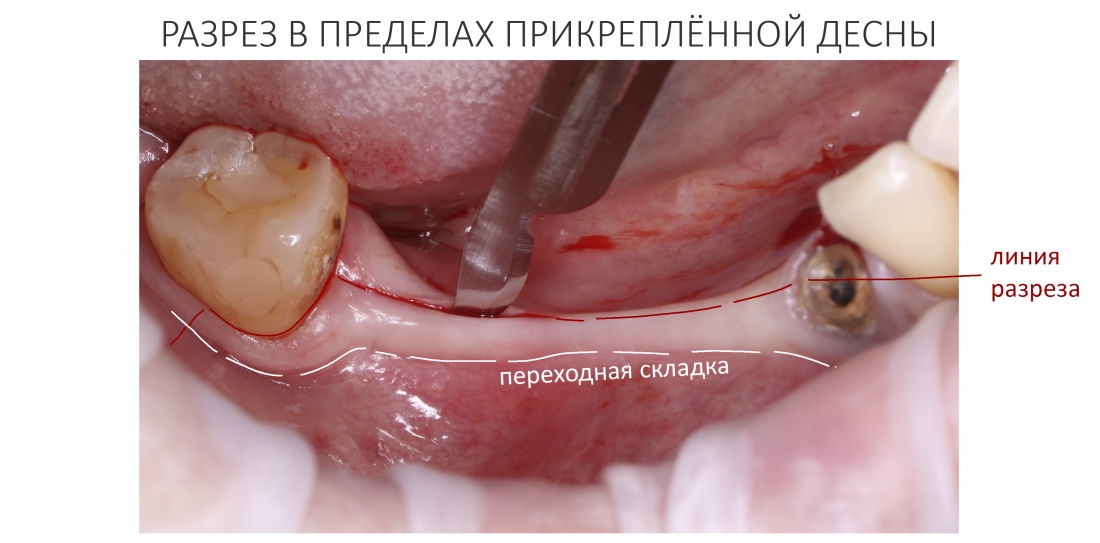
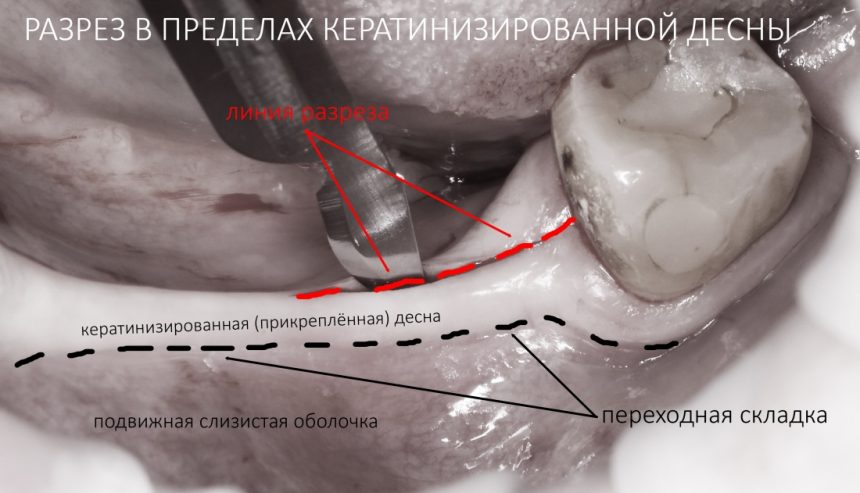
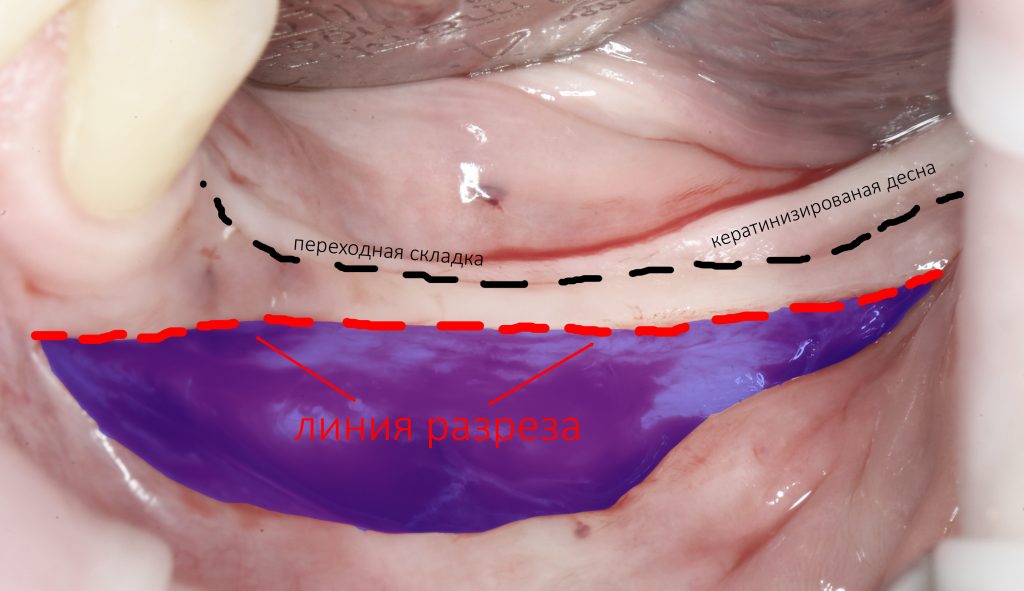
За редким исключением, мы всегда проводим разрез в пределах прикрепленной десны. Даже если её участок шириной всего полтора-два миллиметра — постарайся оставить его в этих границах.
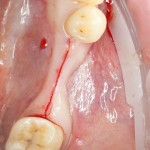
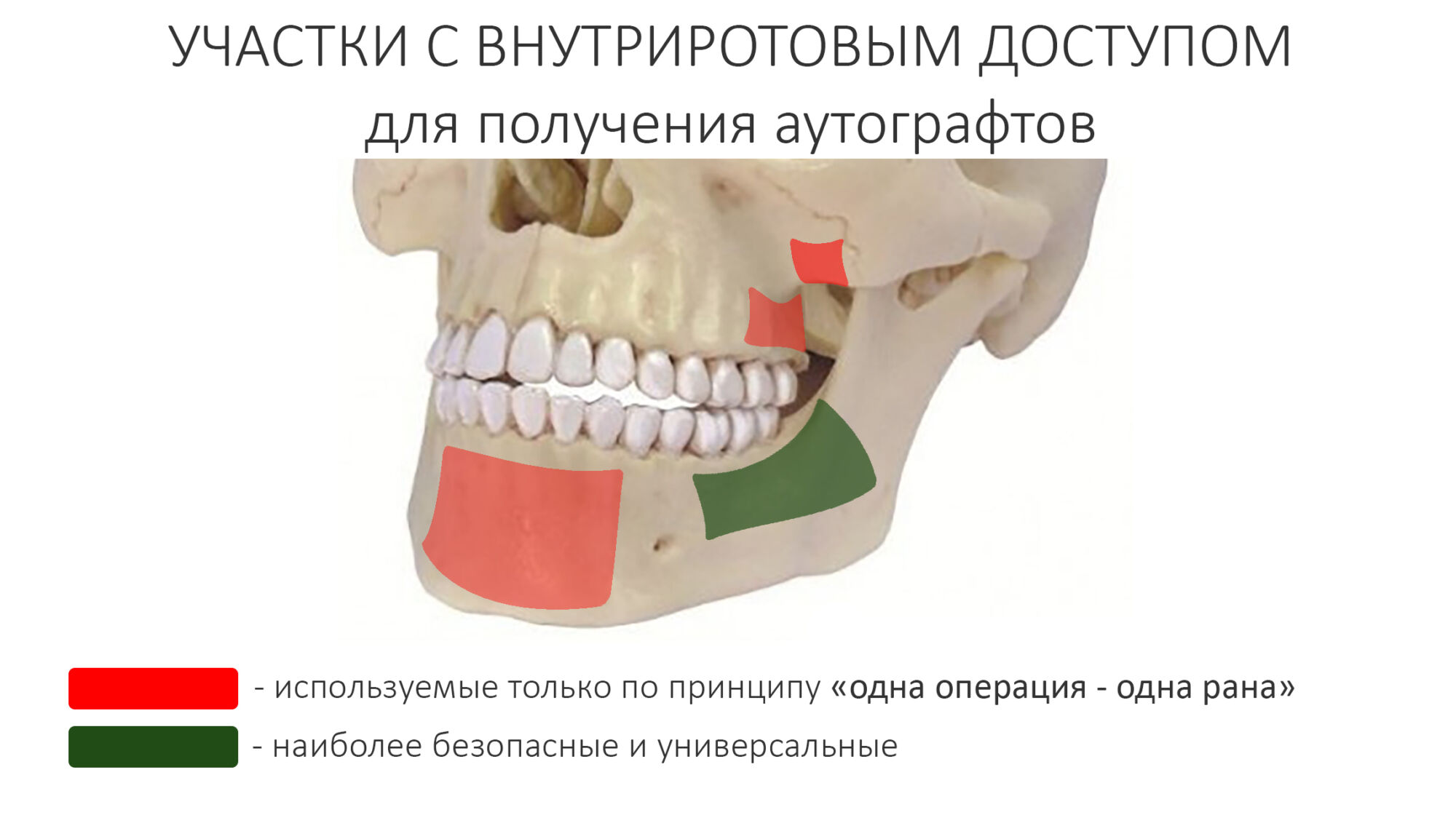
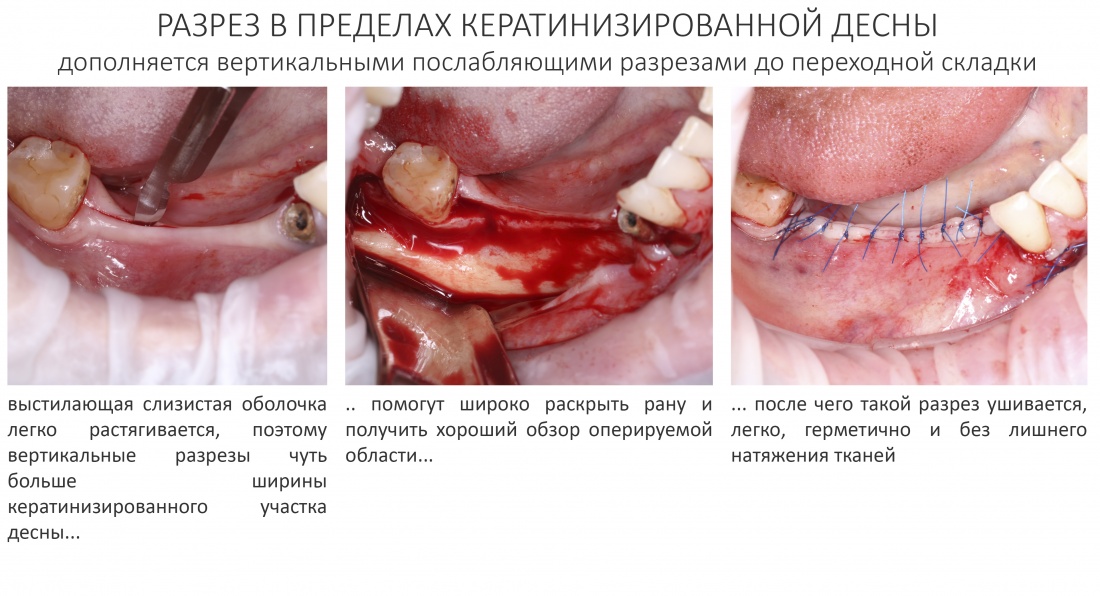
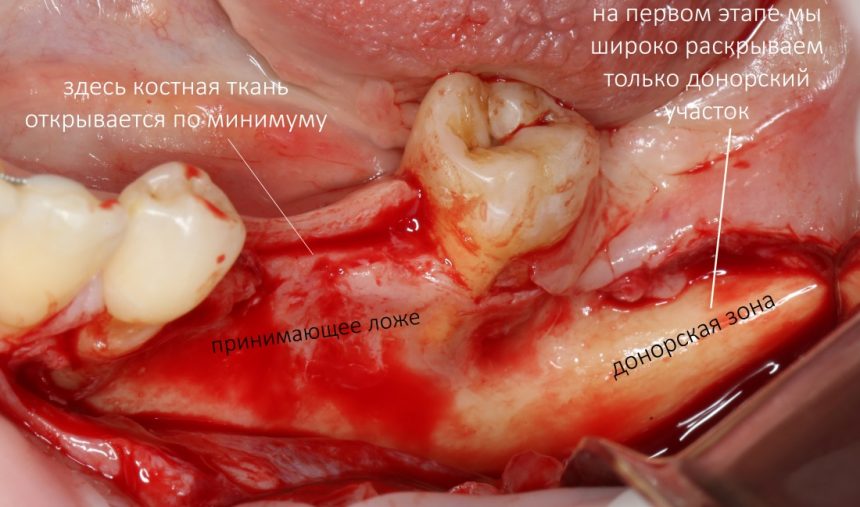
Поскольку мы планируем получать аутотрансплантат из этой же области, мы продляем разрез до донорской зоны. В этом участке удобно вывести его вестибулярно, прямо в проекции наружной косой линии.
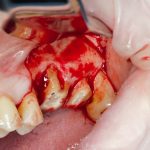
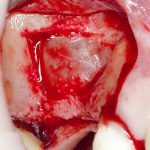
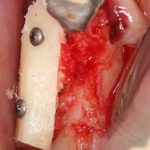
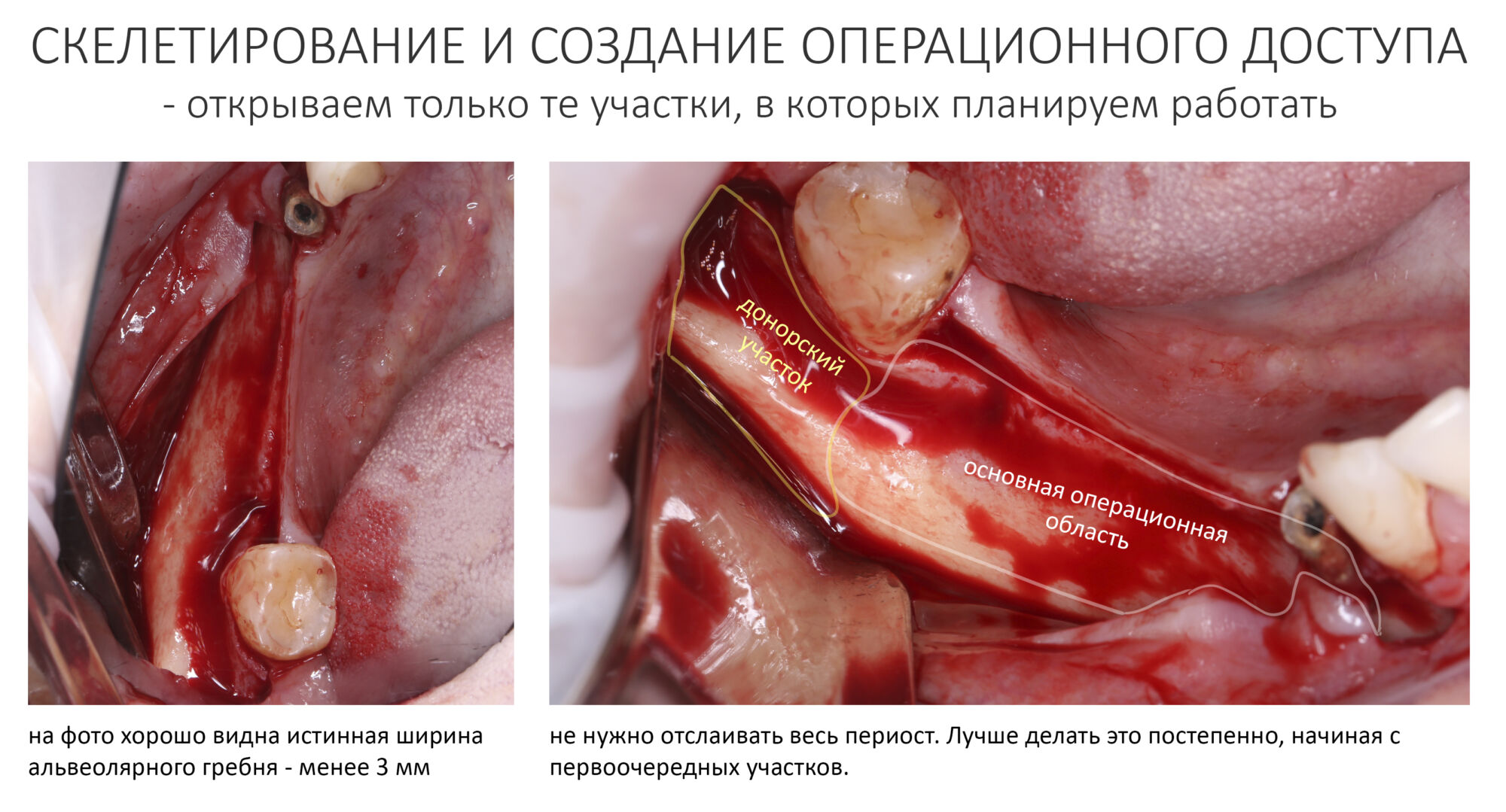
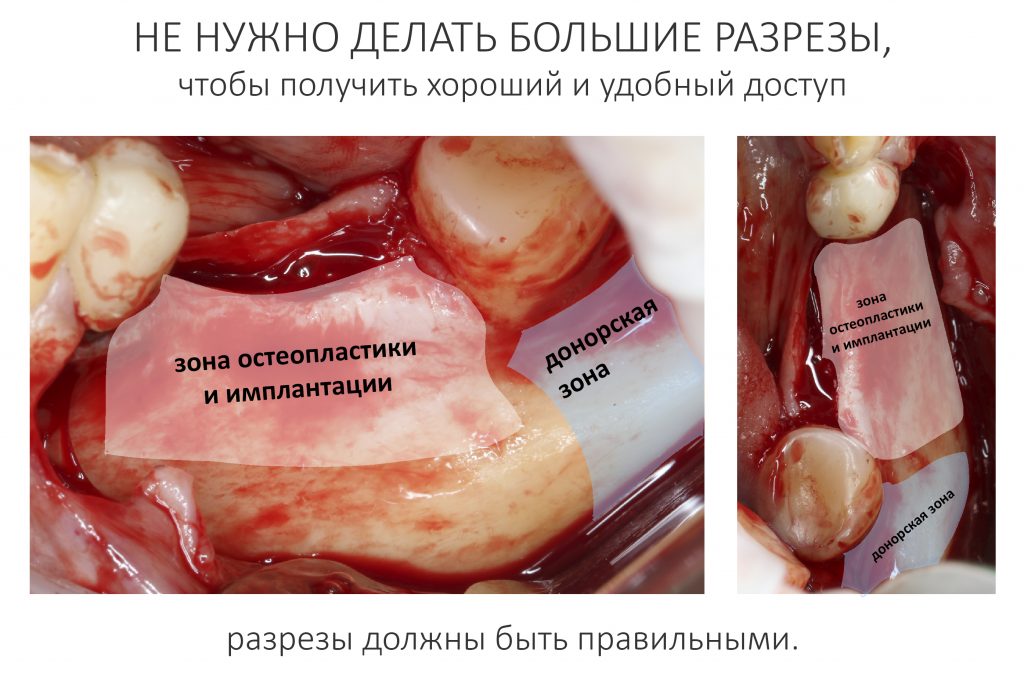
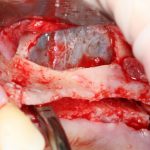
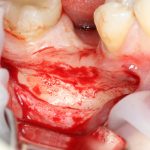
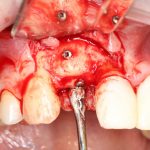
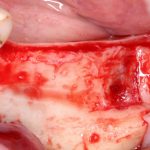
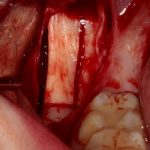
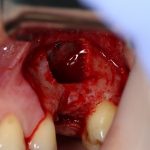
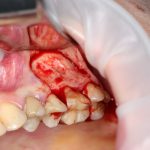
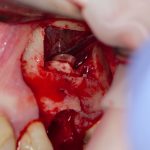
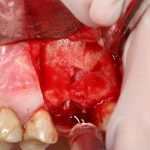
Скелетирование и создание доступа.
Не нужно отслаивать периост сразу и отовсюду. Зачем? Вместо этого, мы последовательно открываем те участки, в которых предполагаем вести манипуляции.
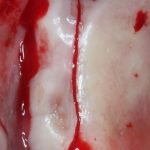
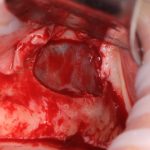
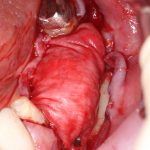
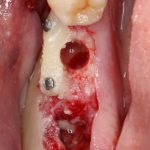
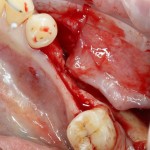
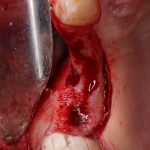
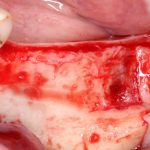
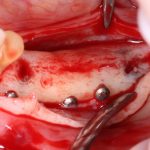
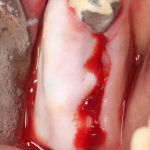
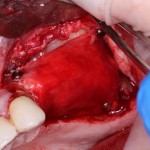
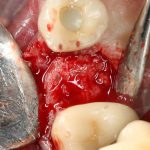
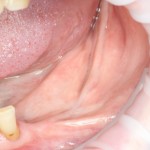
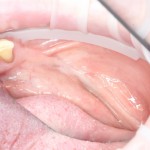
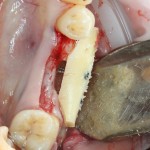
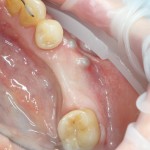
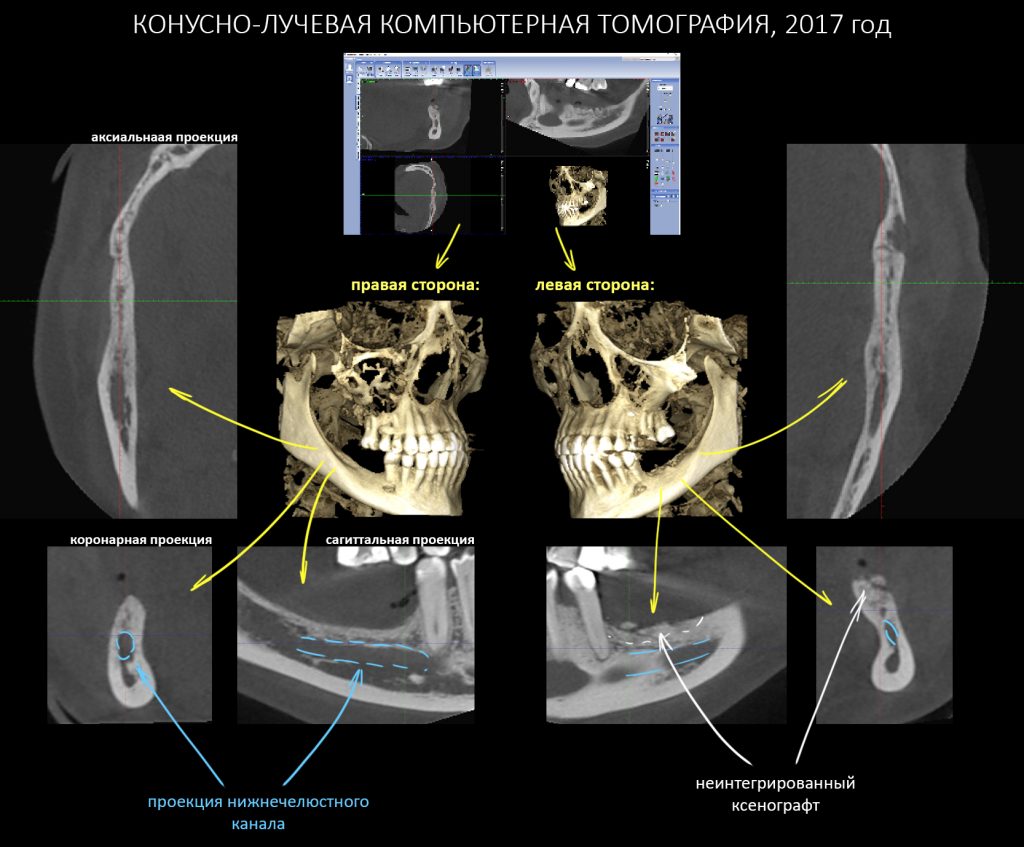
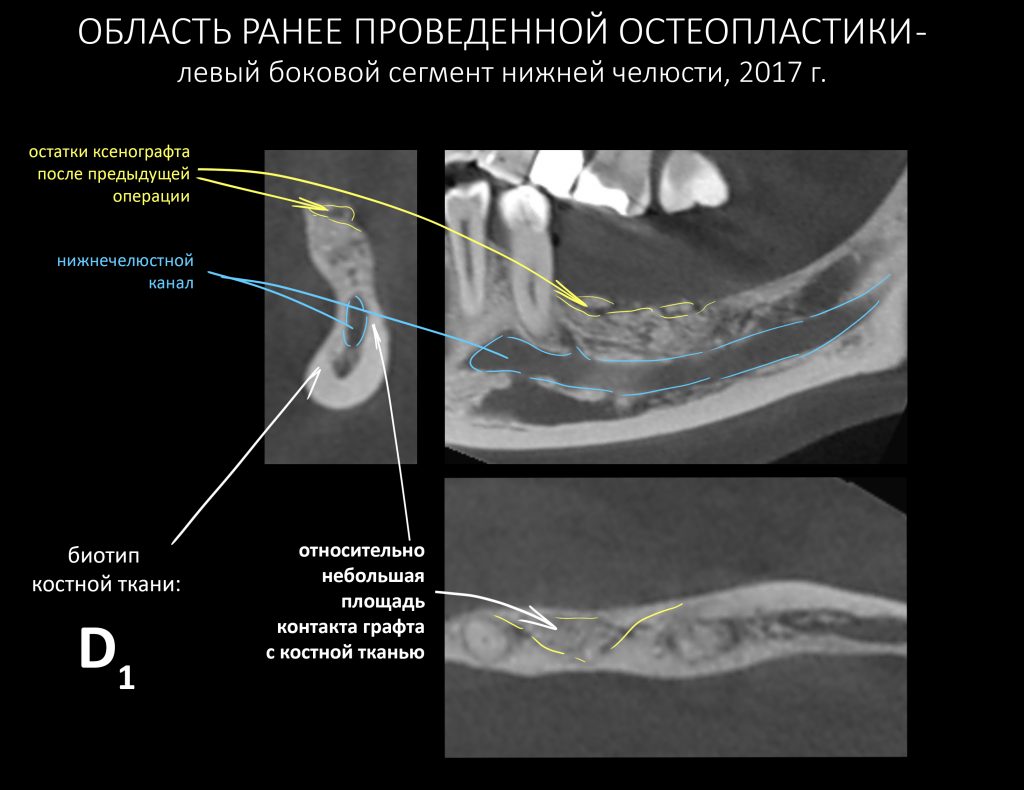
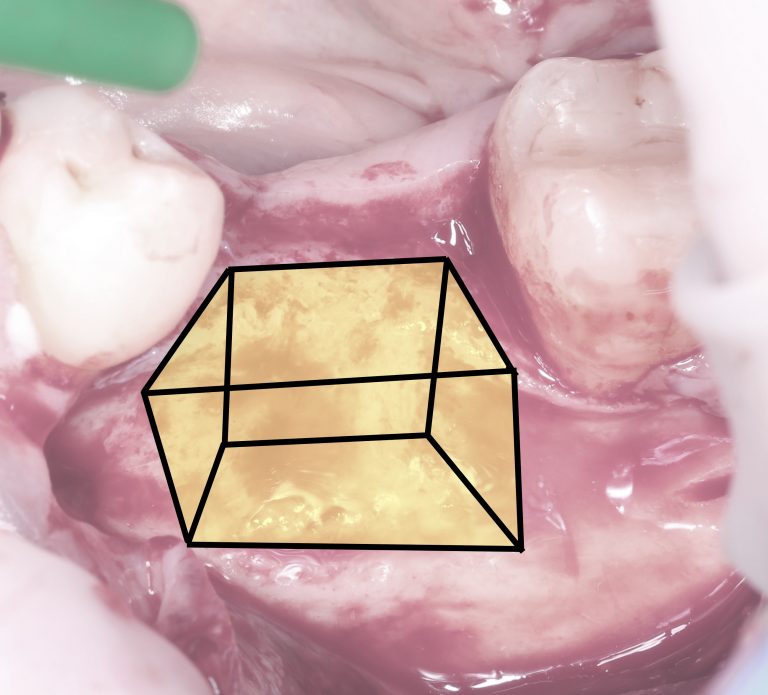
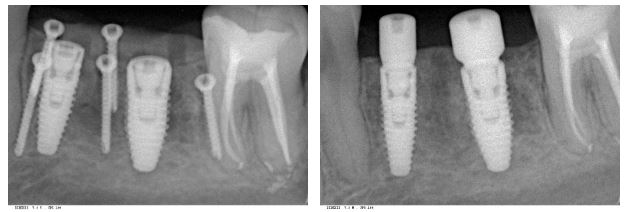
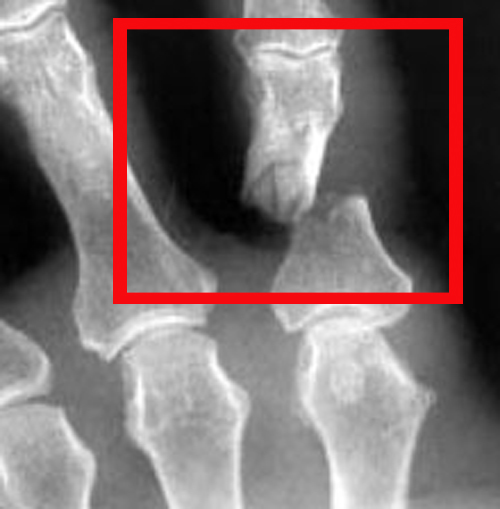
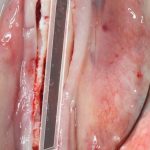
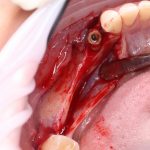
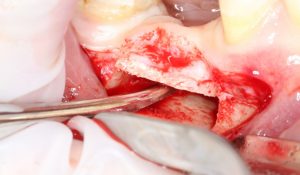
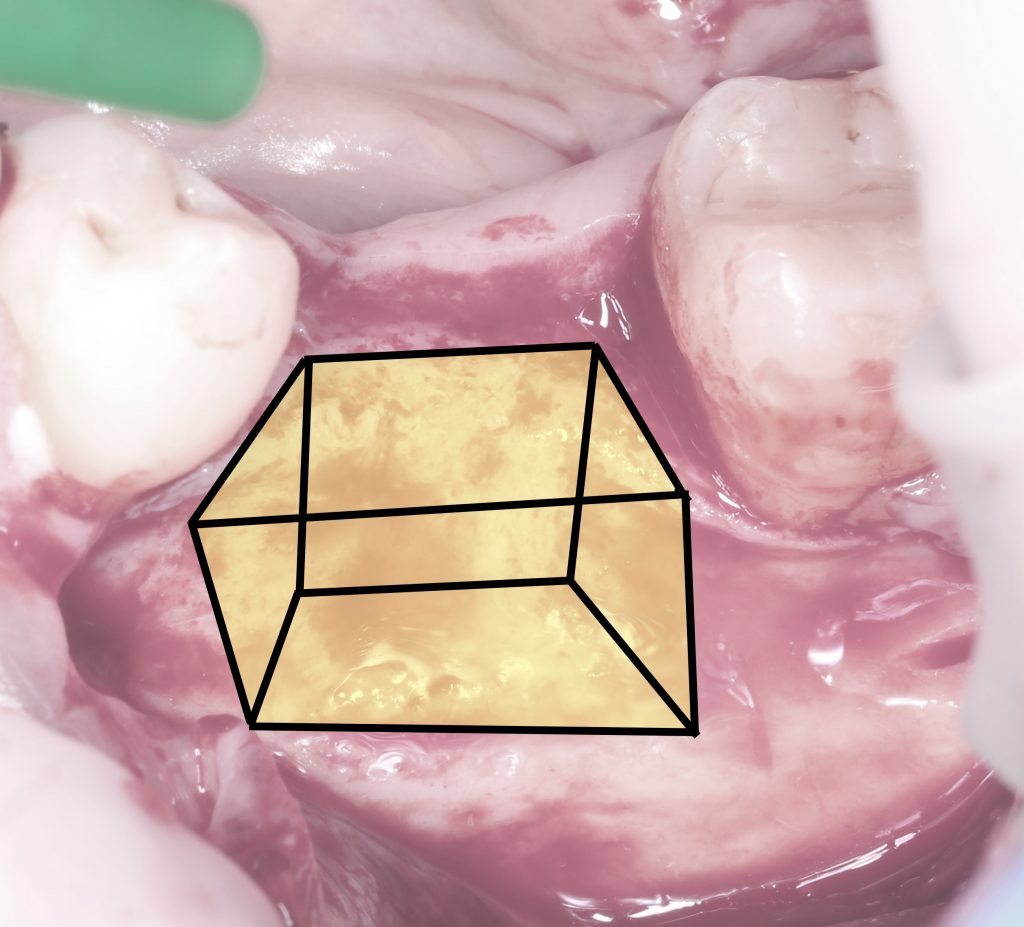
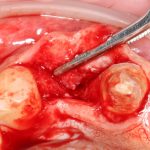
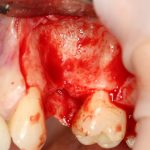
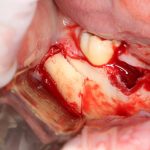
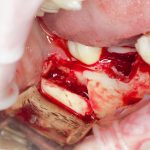
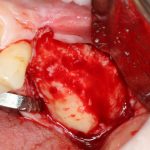
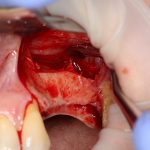
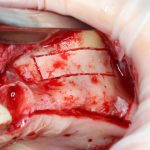
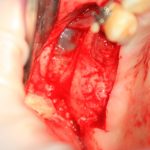
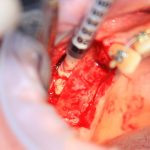
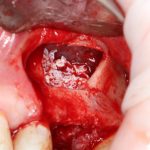
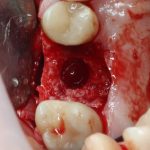
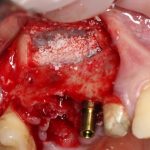
Кстати, обрати внимание на ширину альвеолярного гребня (левая картинка). Она чуть меньше 3 мм. Это объясняет, почему я засомневался в возможности установки имплантатов одновременно с остеопластикой. Понятно и без КЛКТ.
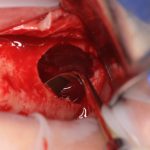
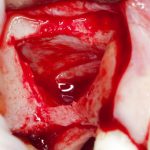
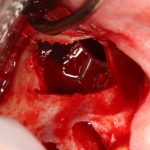
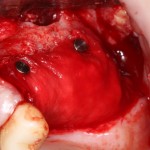
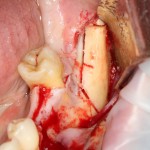
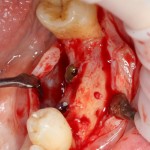
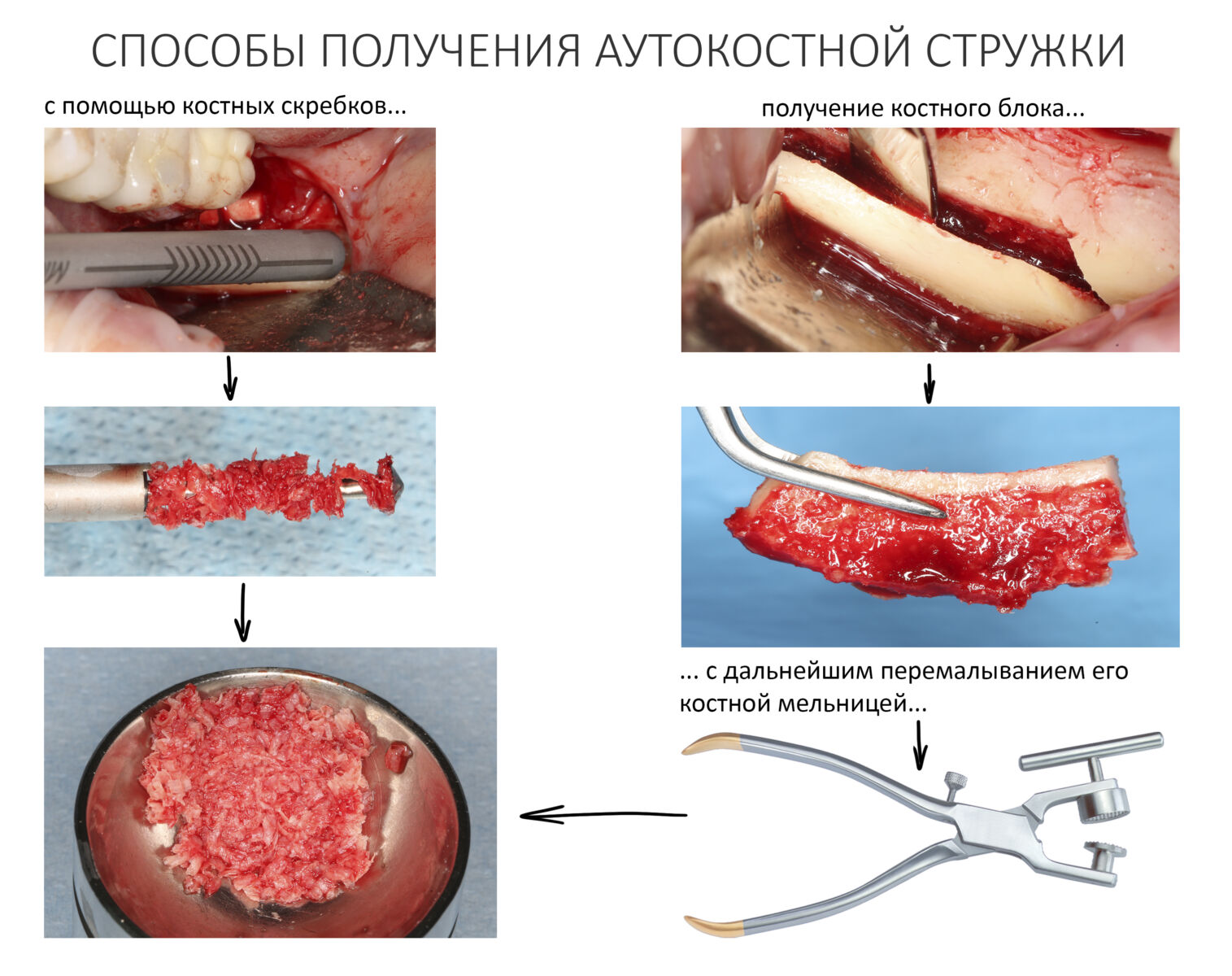
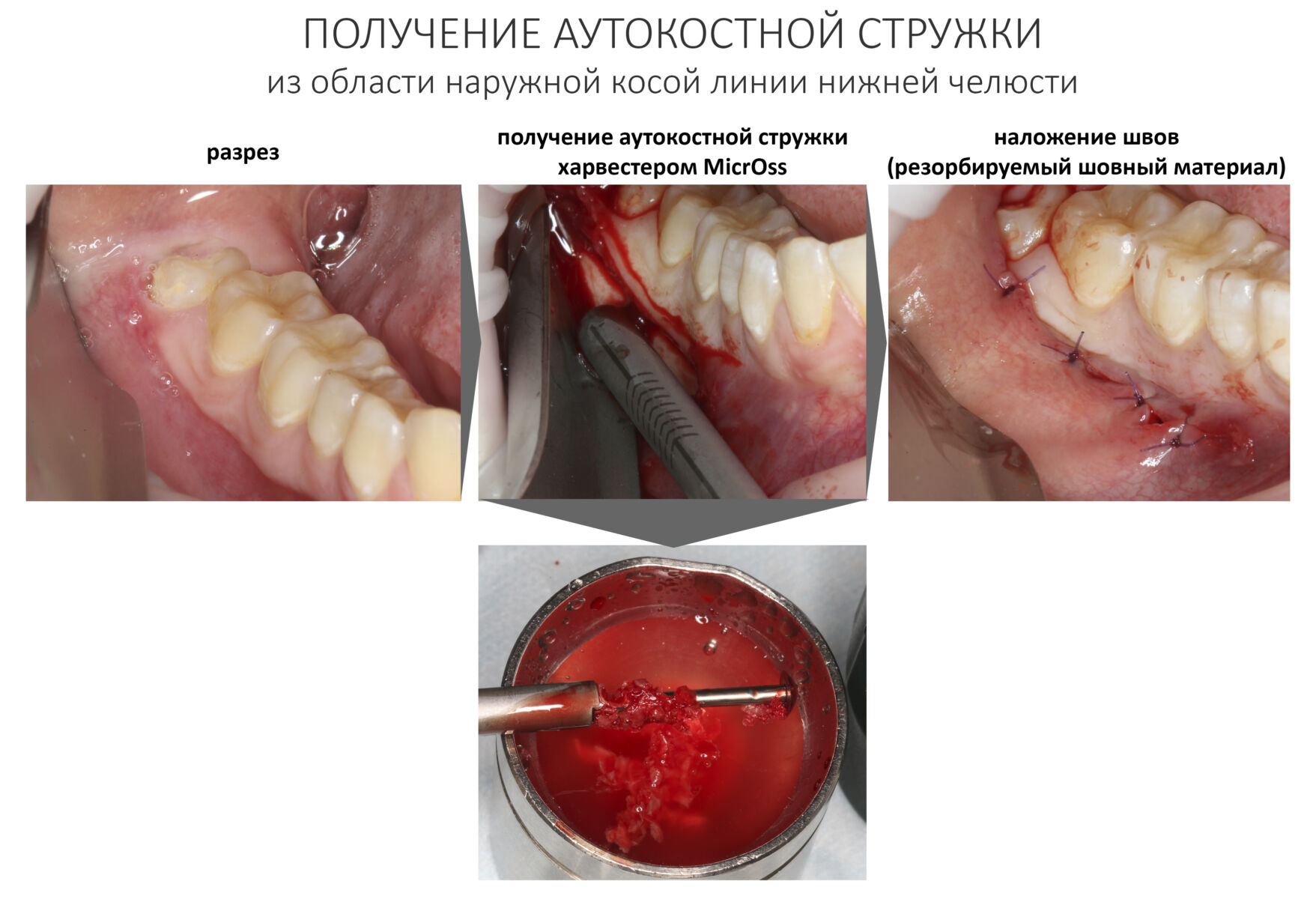
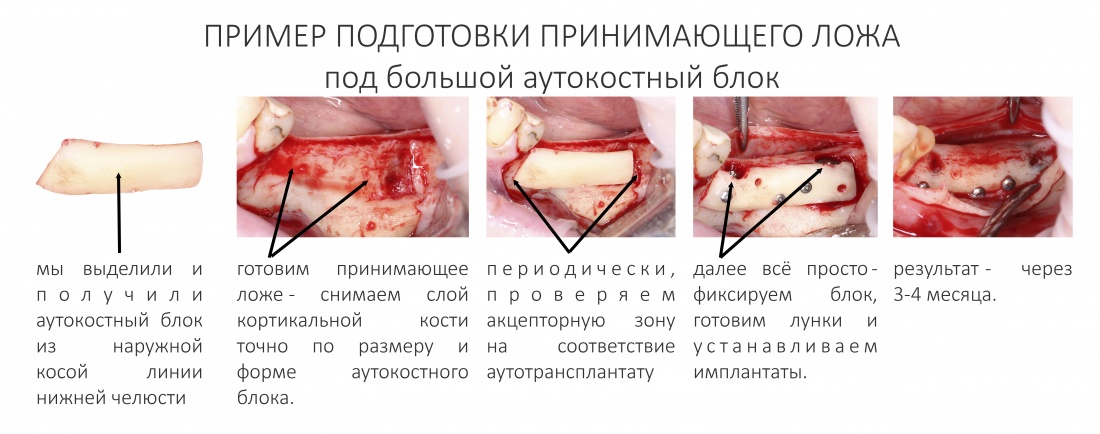
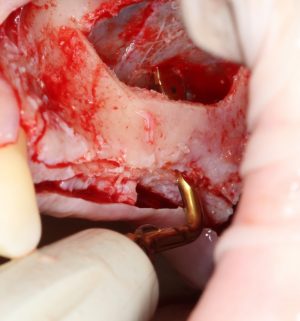
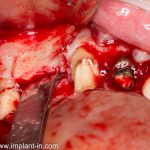
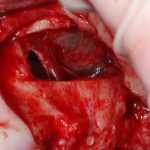
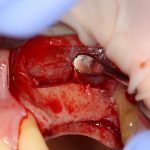
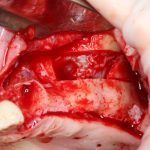
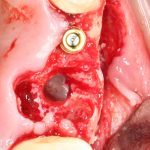
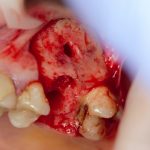
Наперво, мне нужно удалить разрушенный зуб и получить костный аутотрансплантат.
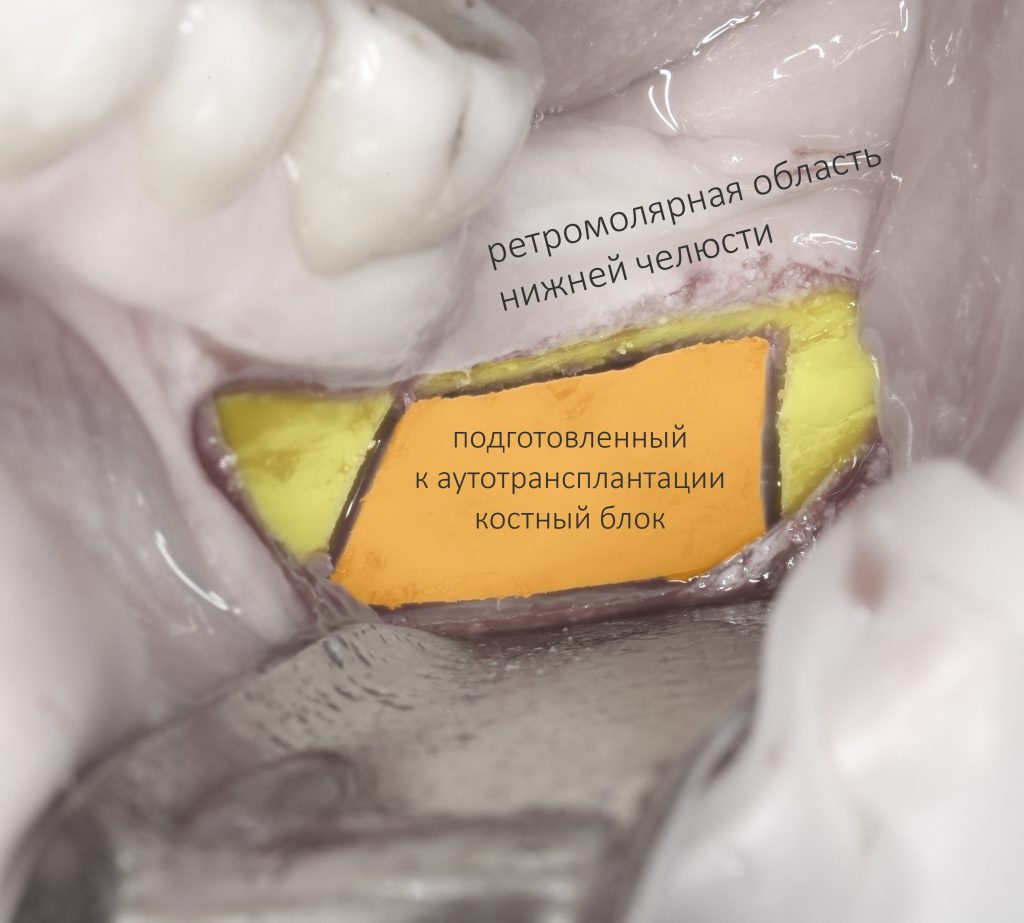
Для получения костного блока, мы открываем донорскую зону, наружную косую линию нижней челюсти.
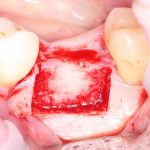
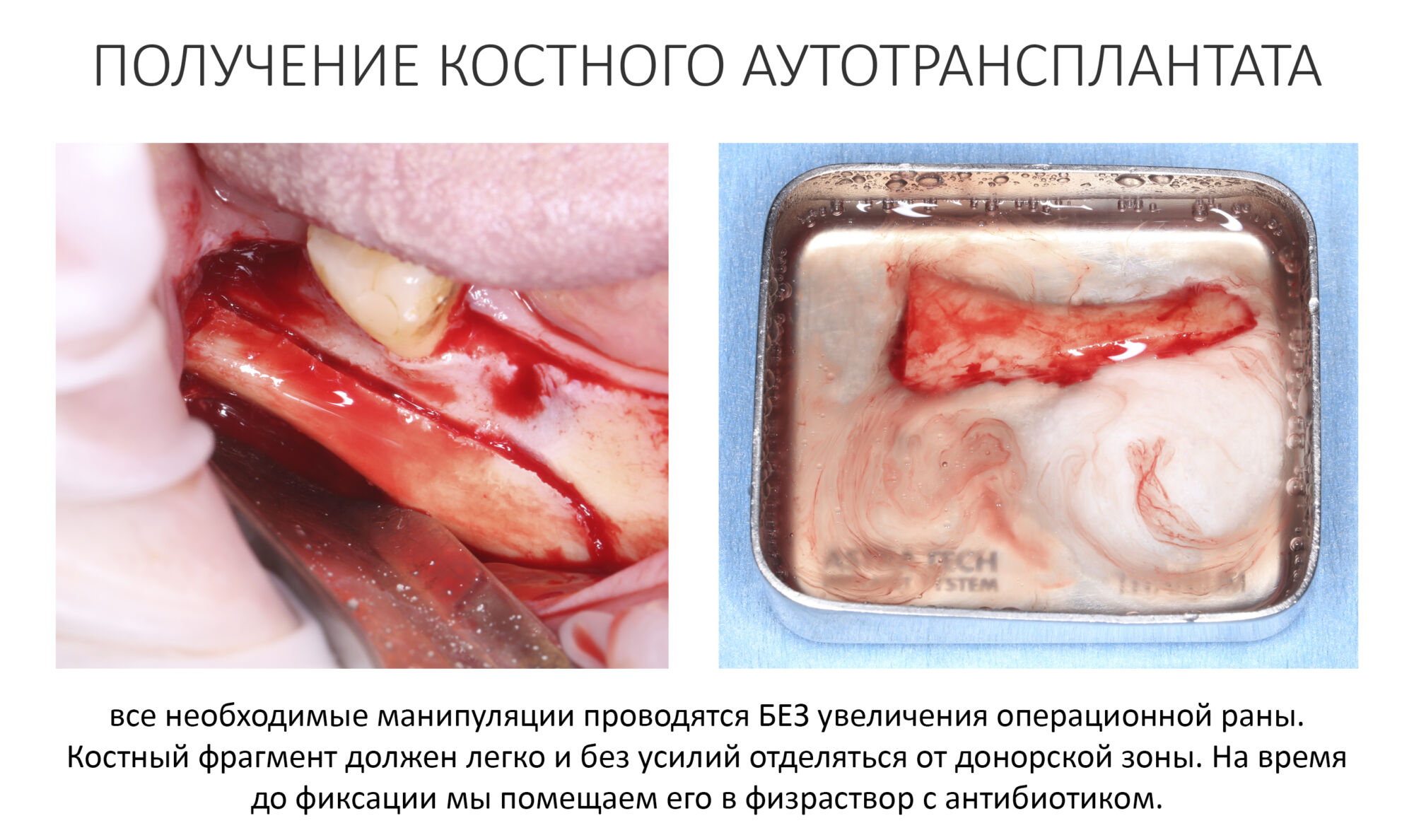
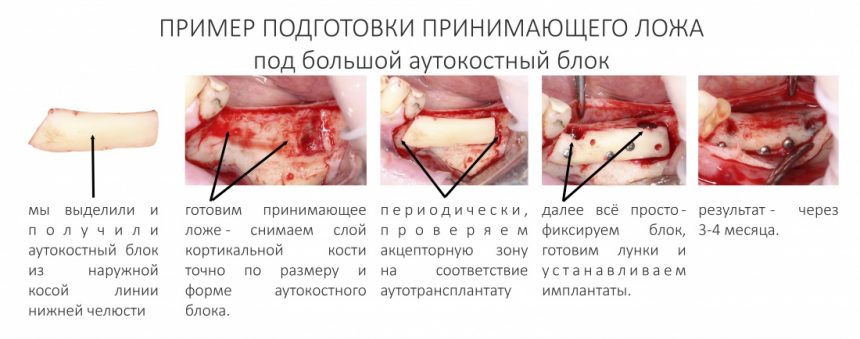
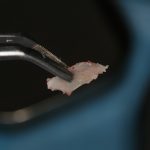
Получение костного аутотрансплантата.
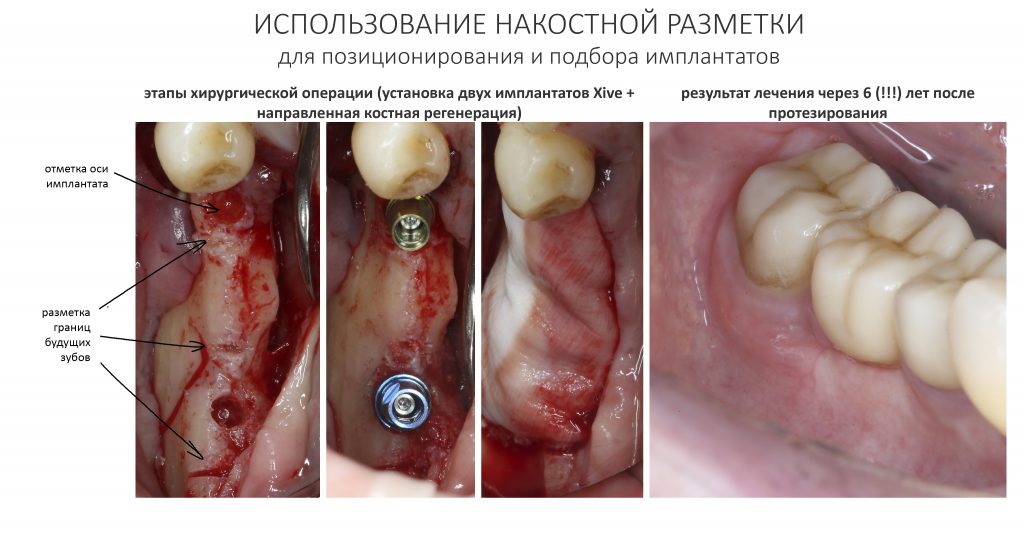
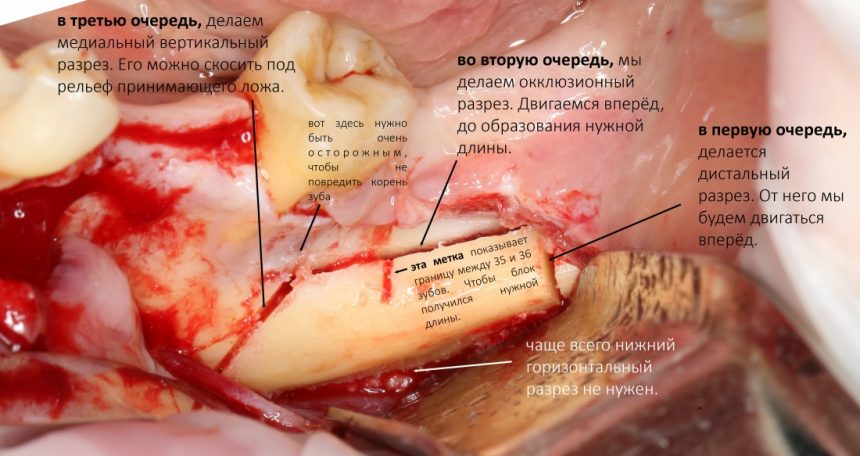
Здесь потребуется пародонтологический зонд с миллиметровой разметкой или какой-то другой измерительный прибор (операционная линейка). Ранее по КЛКТ я измерил костный дефект, теперь нужно нанести границы будущего костного блока на донорскую зону.
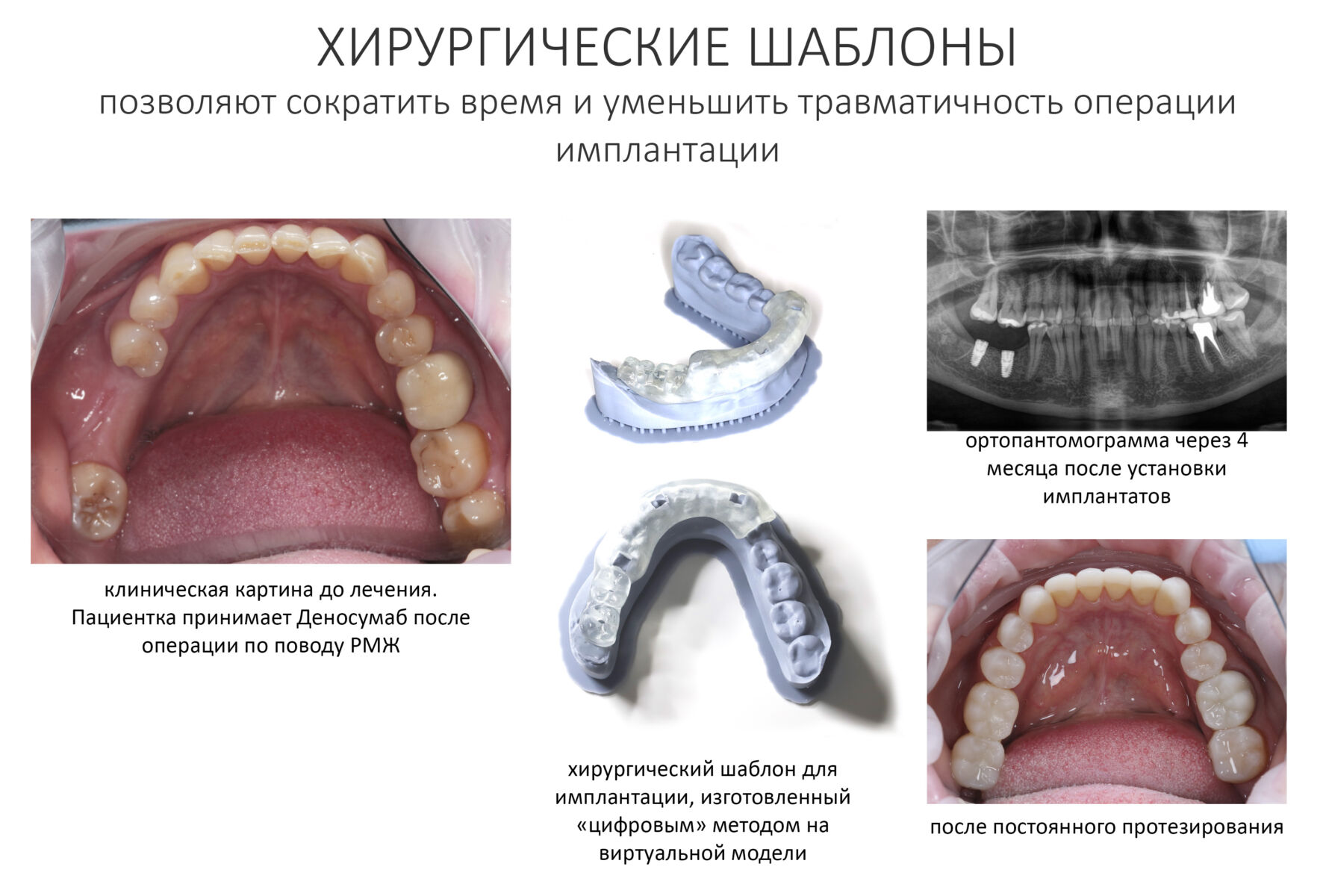
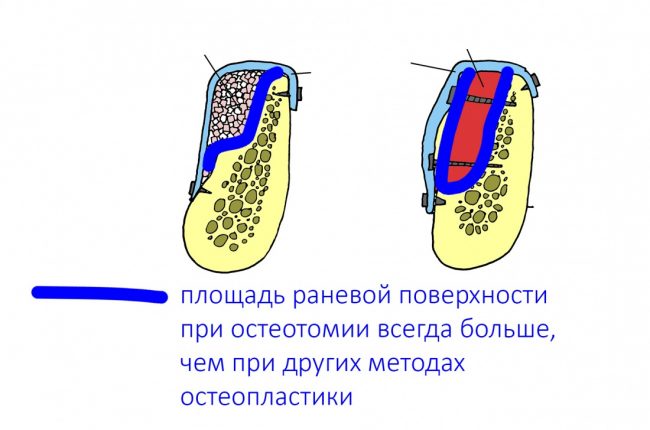
Ремарка: некоторые доктора предлагают делать хирургические шаблоны или выкройки специально для точного забора костного блока. На мой взгляд, это чрезмерное усложнение - во-первых, использование подобных шаблонов или выкроек требует увеличения площади раны, во-вторых, это увеличивает время и стоимость лечения, в-третьих, на этом этапе не требуется высокая точность, поскольку блок всё равно потребует адаптации.
Иными словами, важна не точность, а быстрый, аккуратный и, что главное, малотравматичный забор аутотрансплантата.
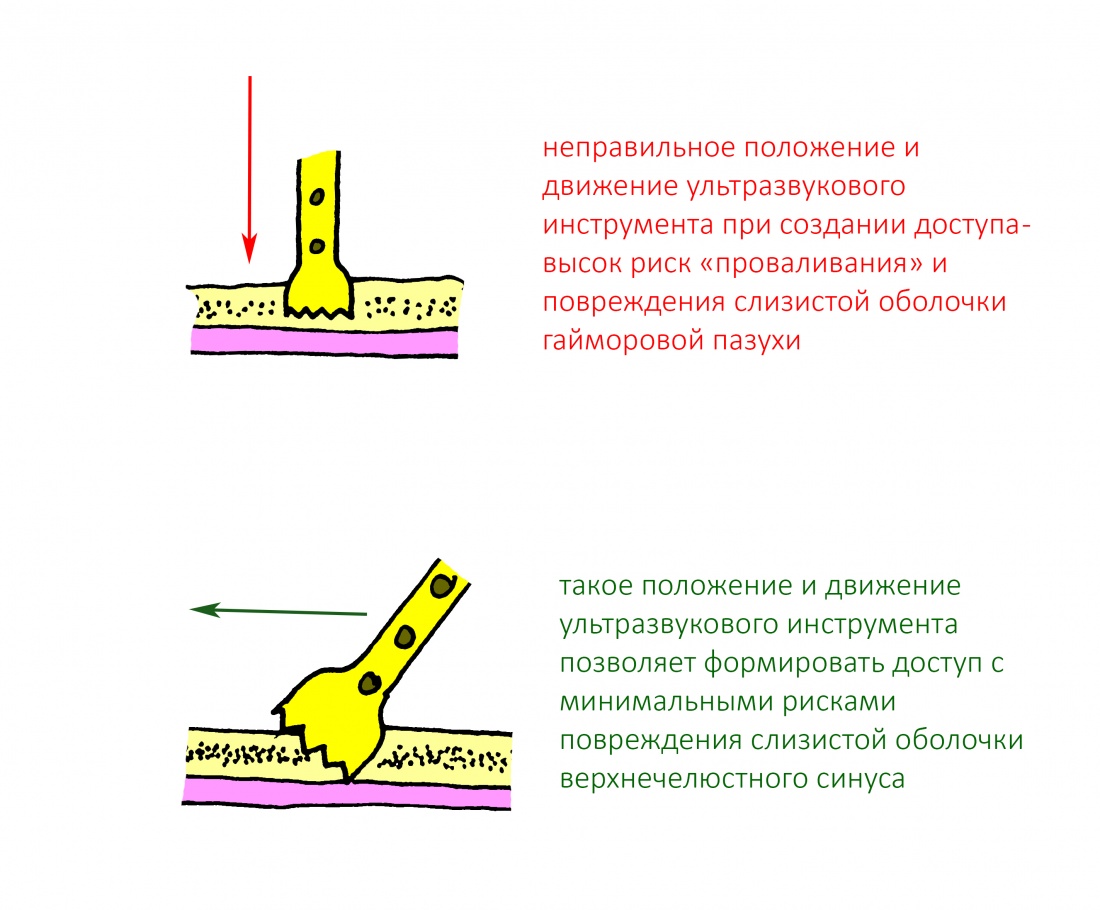
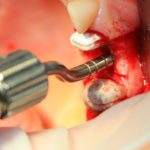
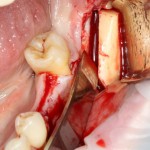
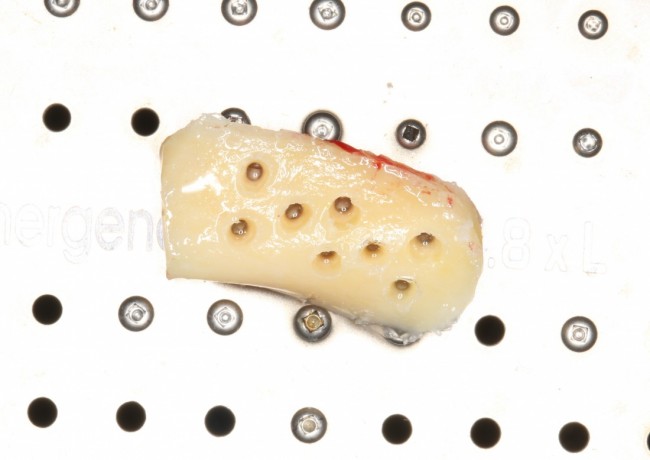
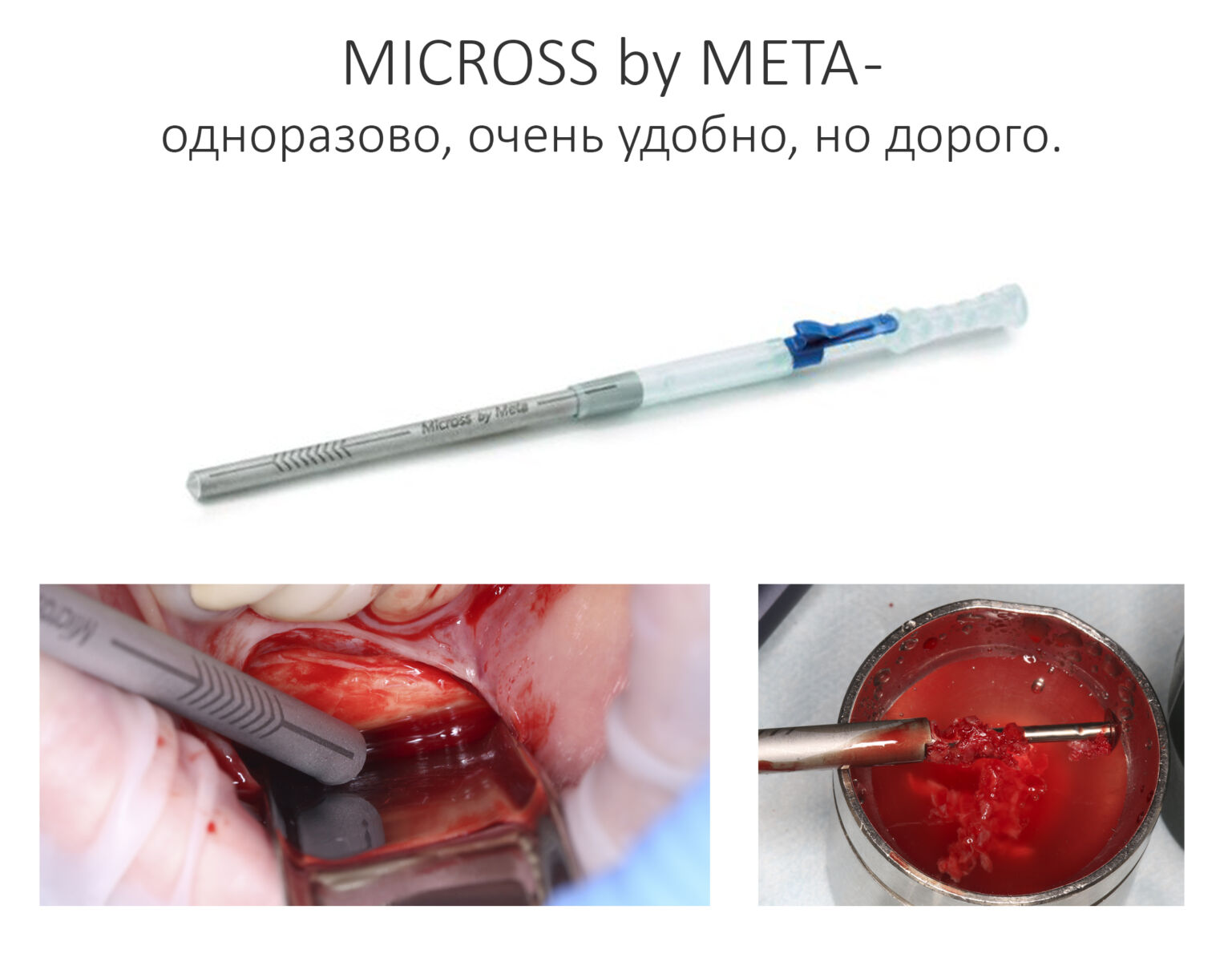
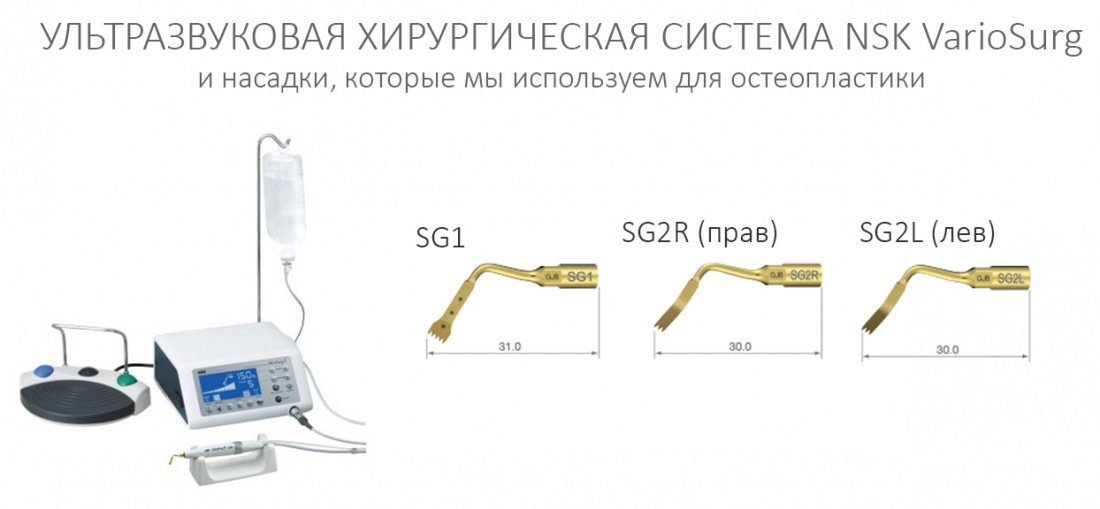
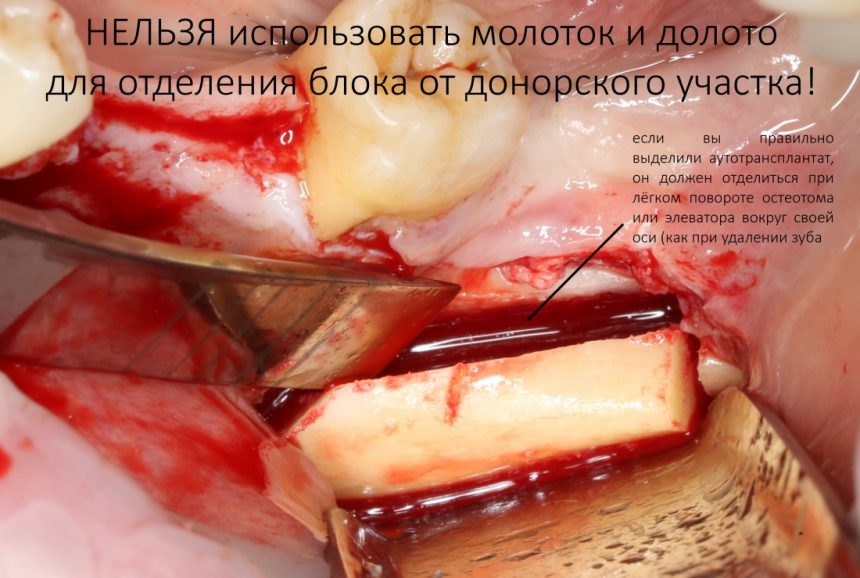
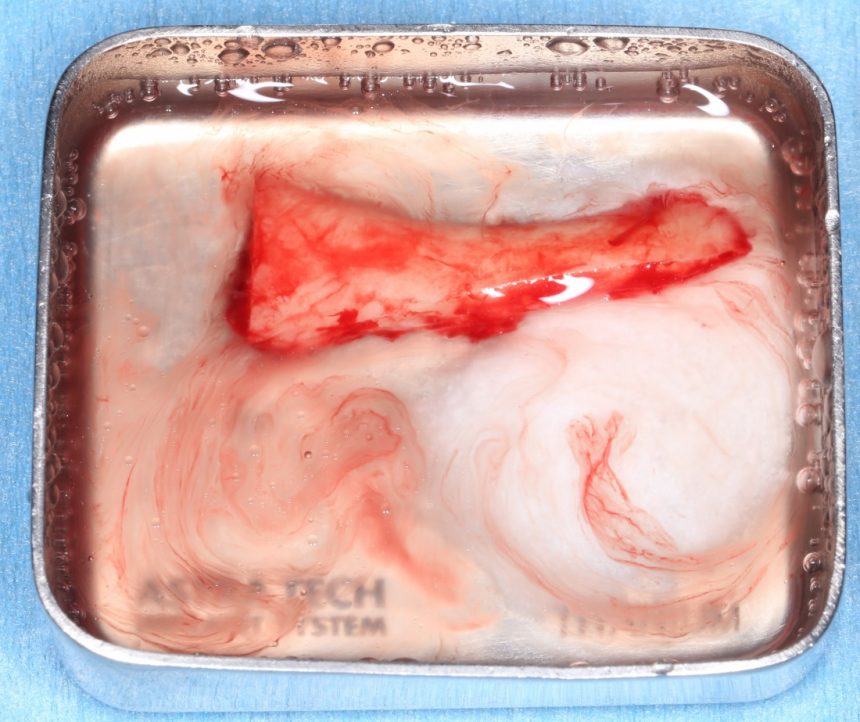
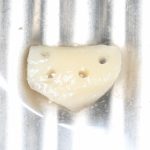
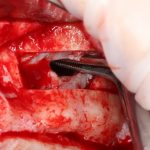
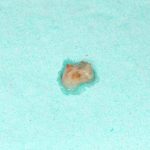
Для получения костного блока мы использовали ультразвуковую пьезохирургическую систему. Это самый удобный и безопасный инструмент для проведения подобных манипуляций. С помощью него мы сформировали и выделили костный блок. Он должен отделяться легким движением остеотома или элеватора. Как это сделать правильно — читай здесь>>
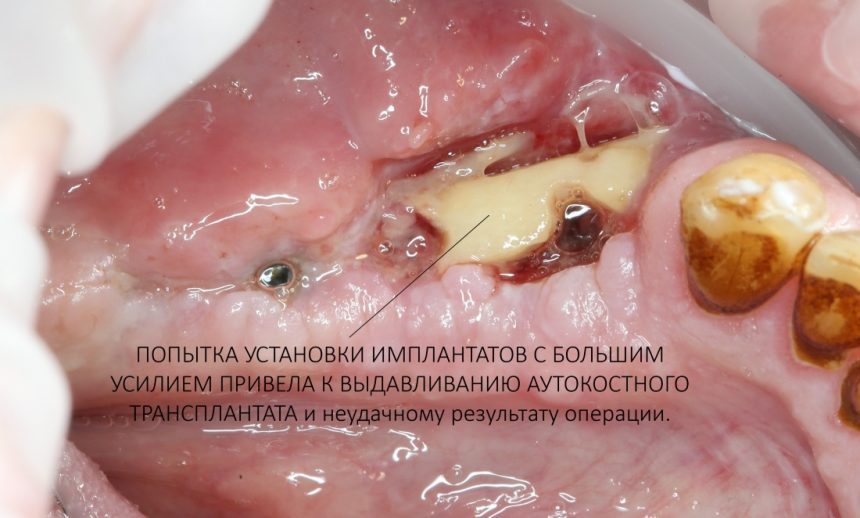
Кстати, если костный блок не отделяется от костного ложа легким движением элеватора, значит он неправильно сформирован или не до конца выделен. Вообще, любое чрезмерное усилие в хирургии — это всегда следствие рукожопия. Если тебе что-то приходится делать с усилием (установка имплантата, удаление зуба и т. д.) — значит ты делаешь это неправильно. Остановись и подумай, что именно.
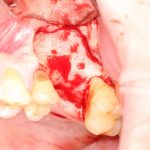
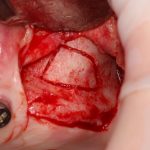
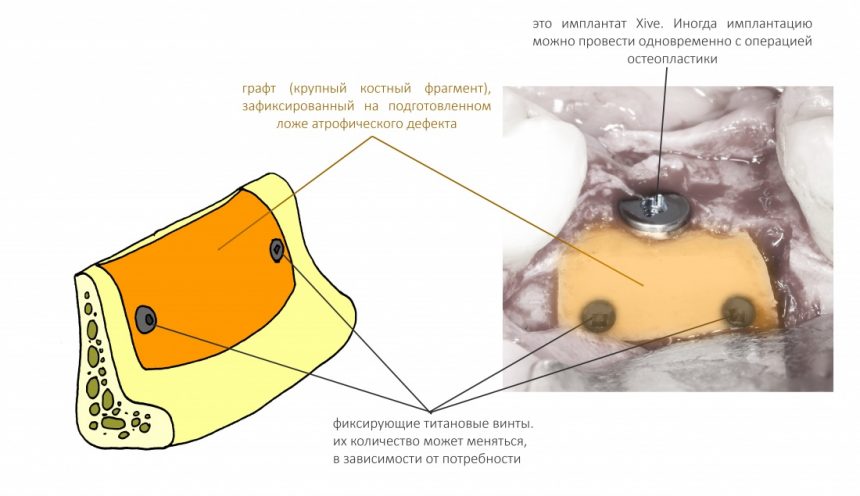
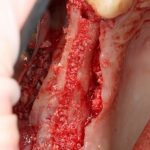
Подготовка костного ложа и фиксация аутотрансплантата
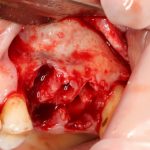
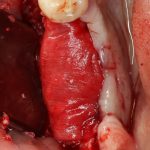
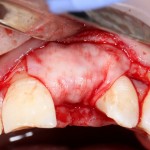
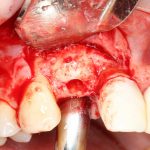
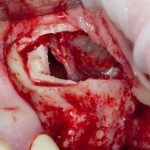
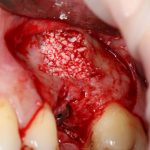
Возвращаемся к основной операционной области. Еще раз посмотрим на альвеолярный гребень, поофигеваем от его ширины и моих грандиозных планов:
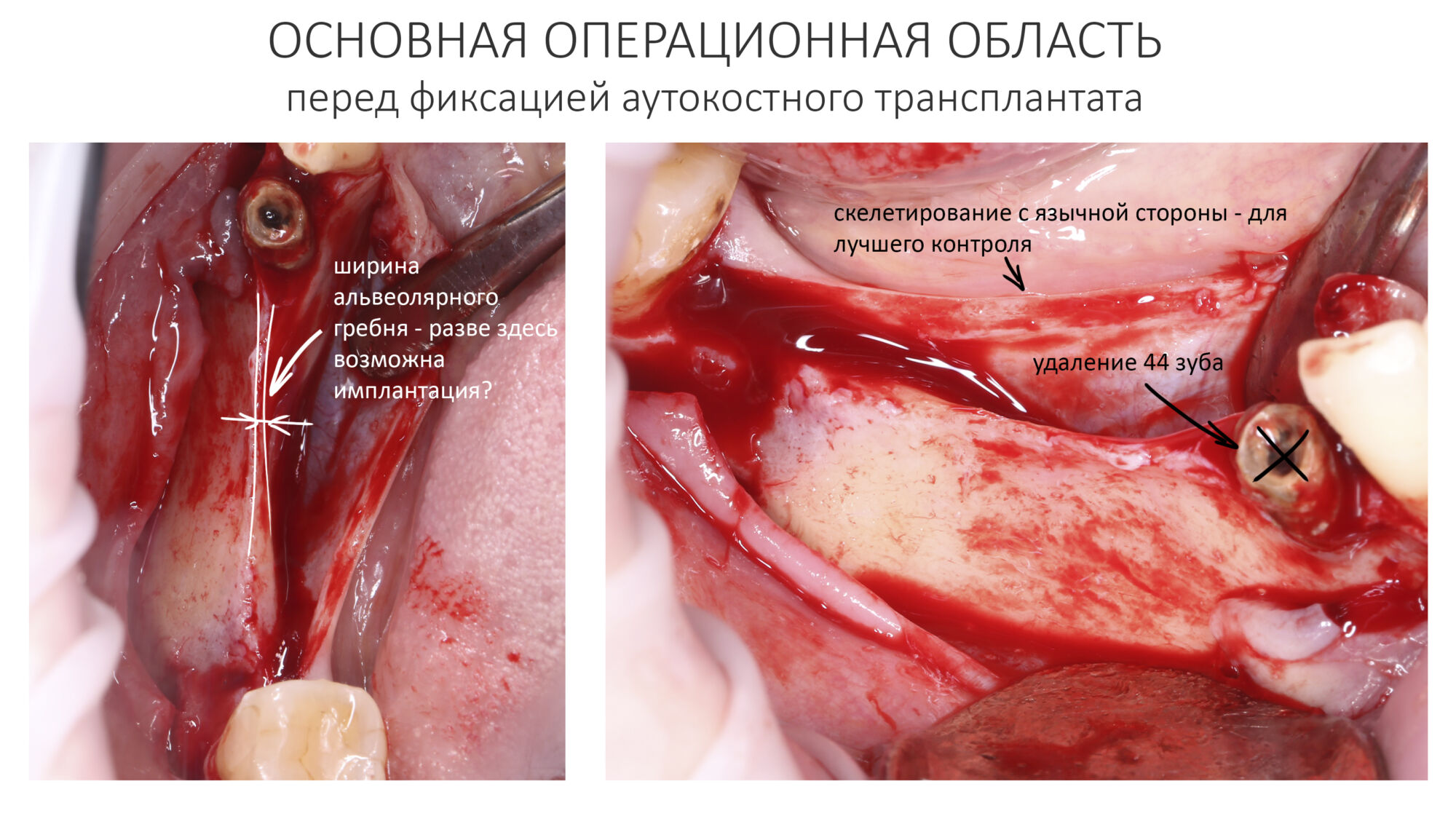 На этом месте мне следует дать некоторые пояснения.
На этом месте мне следует дать некоторые пояснения.
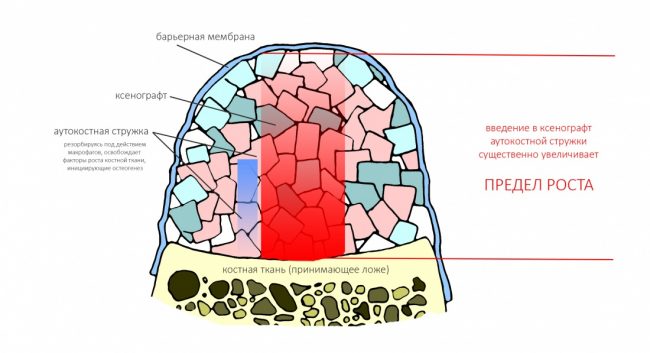
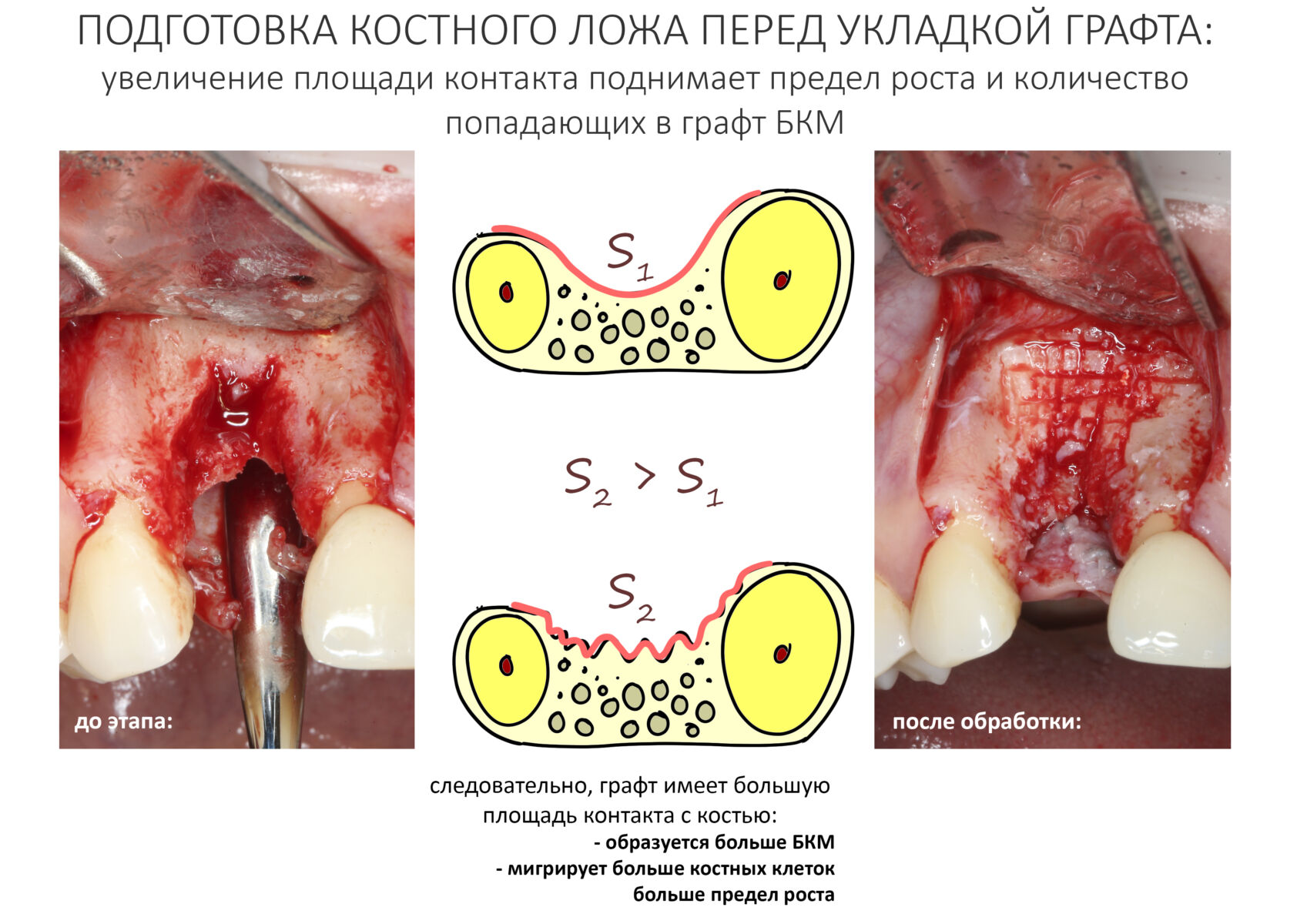
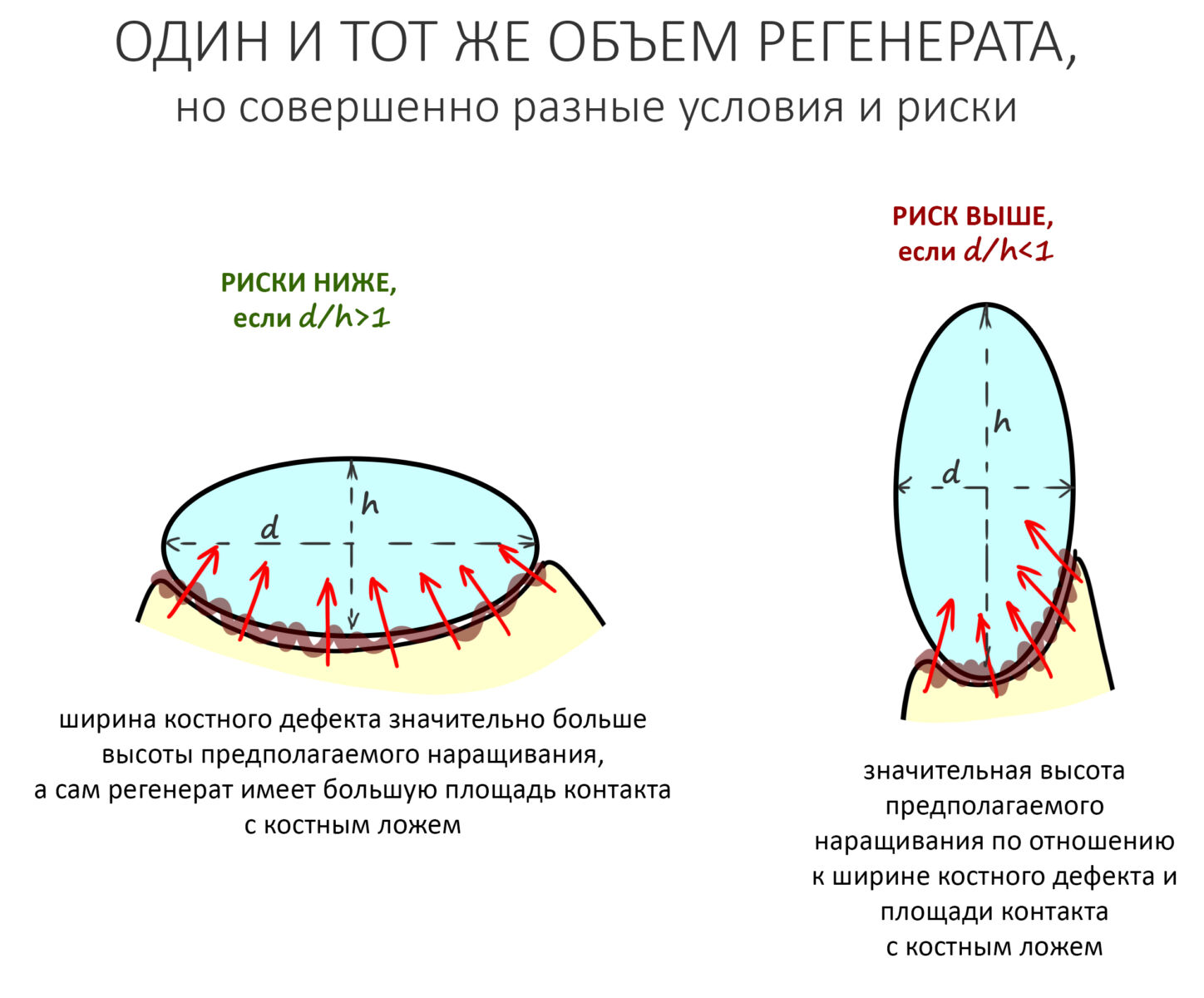
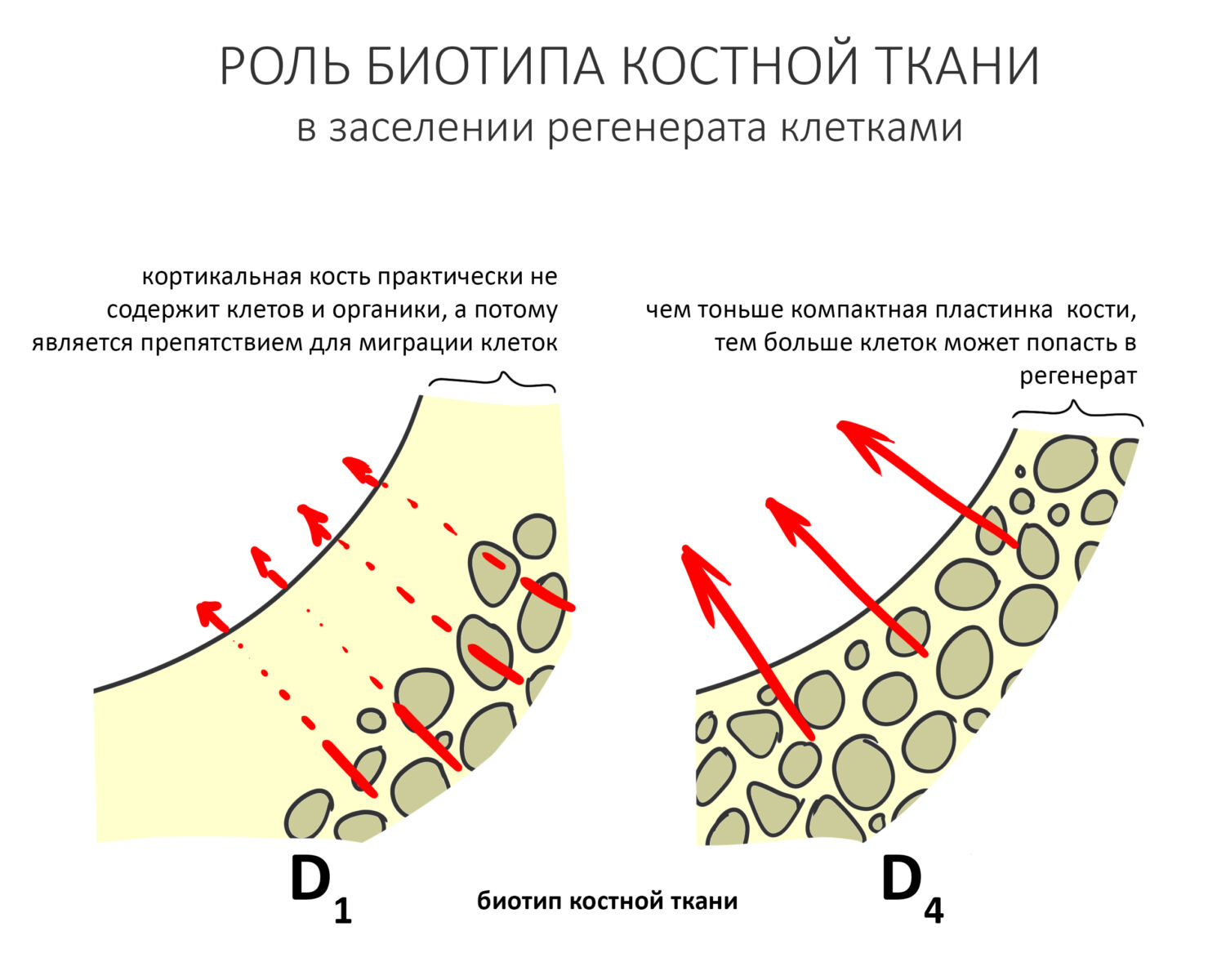
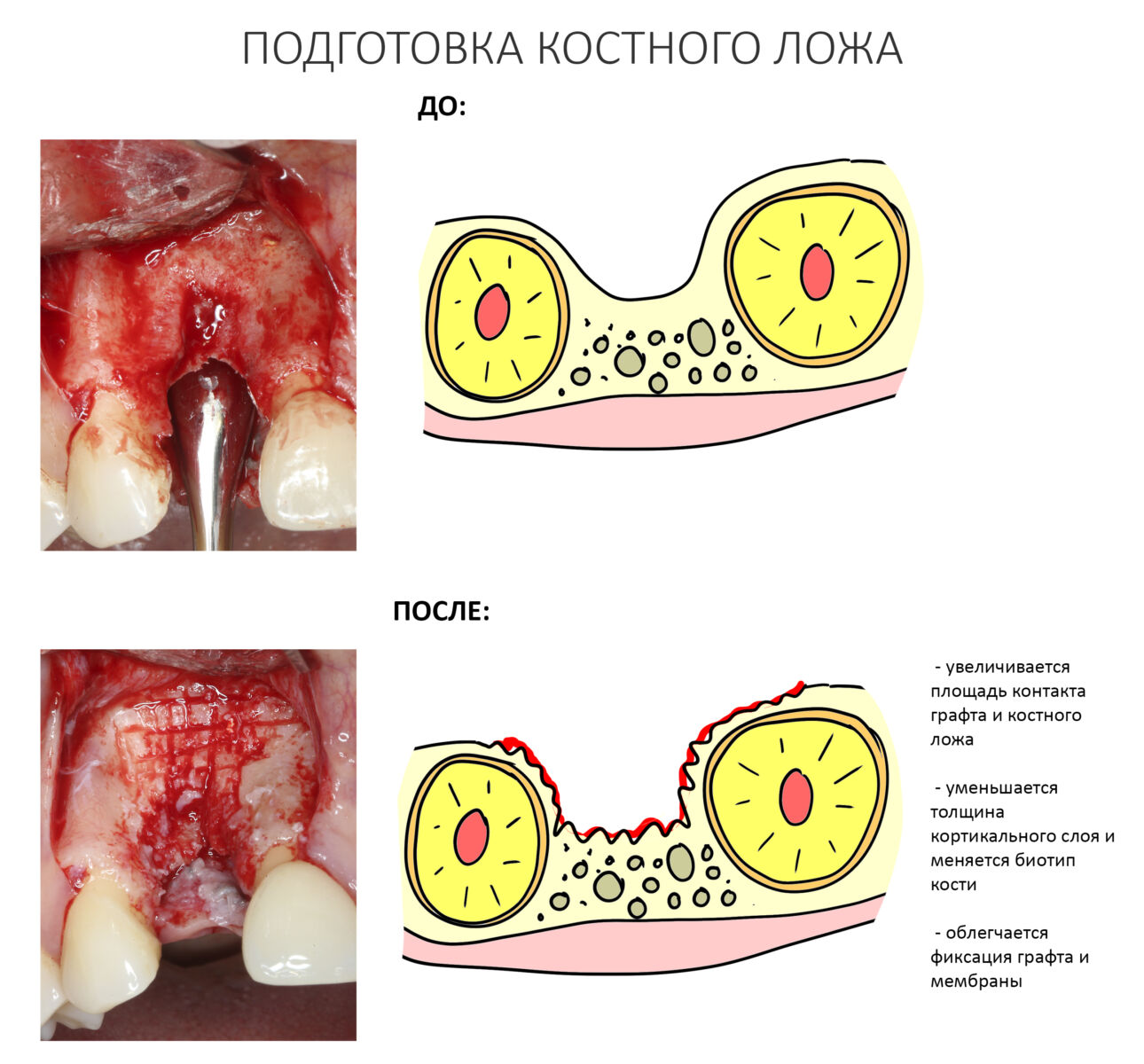
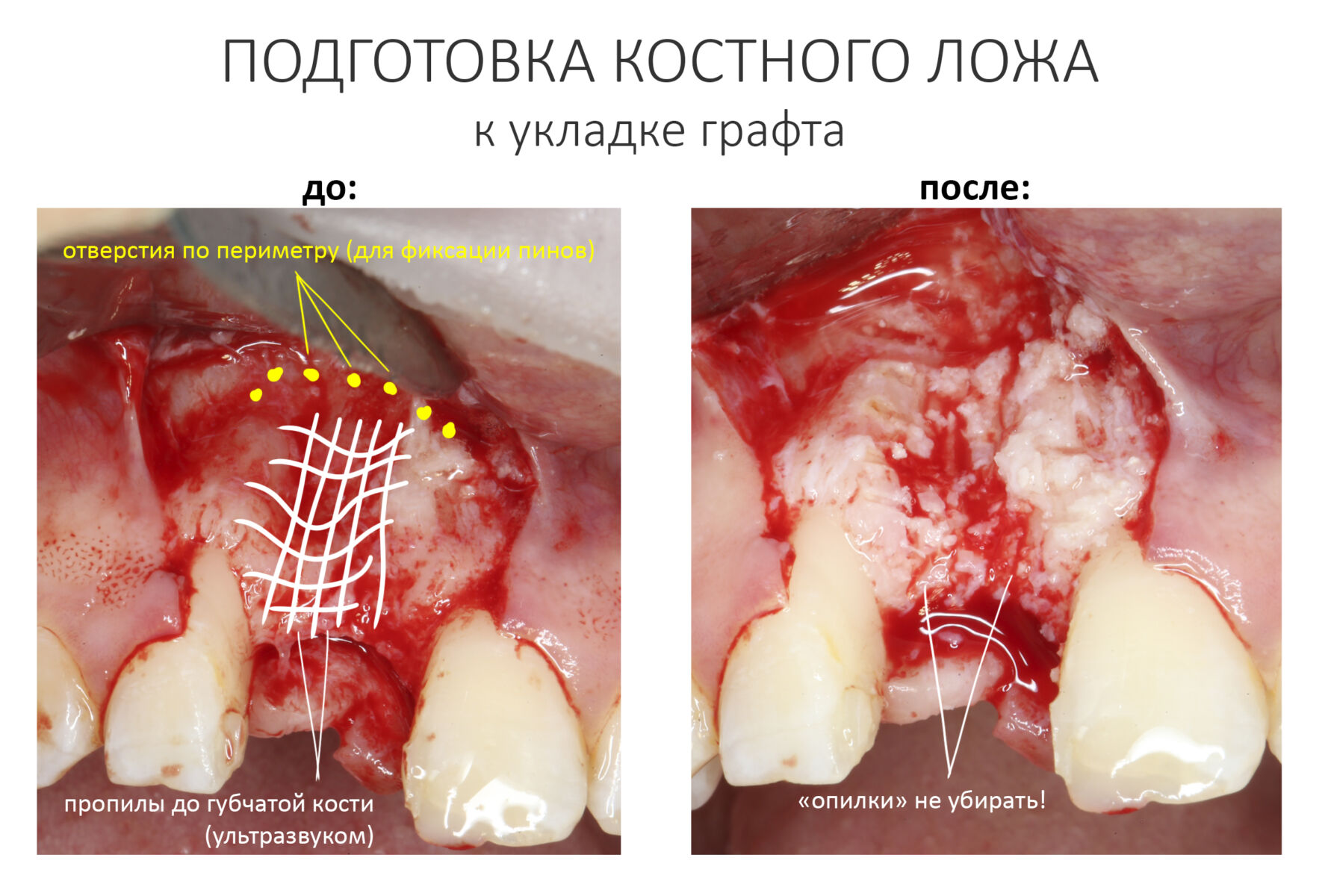
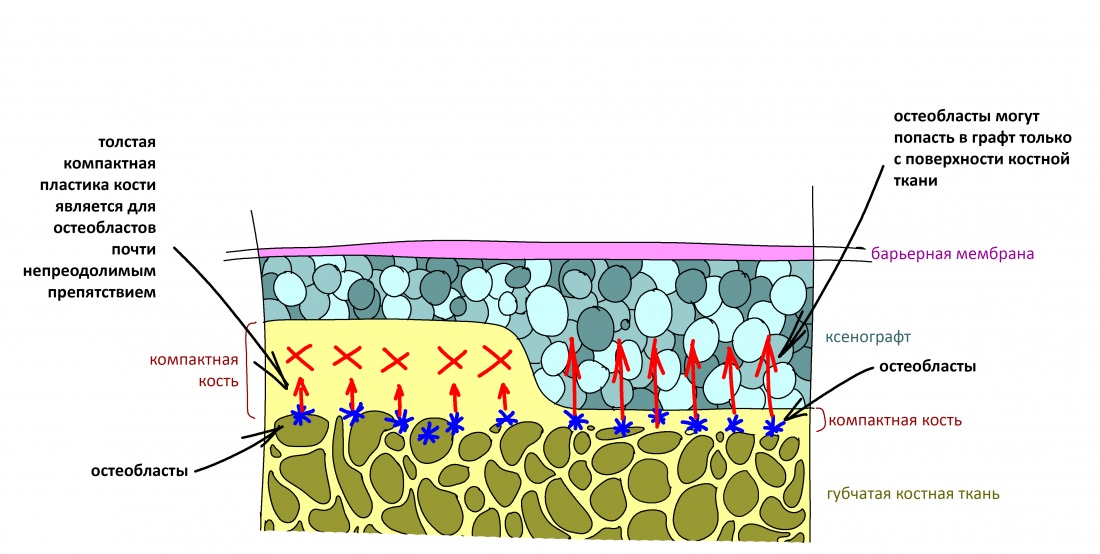
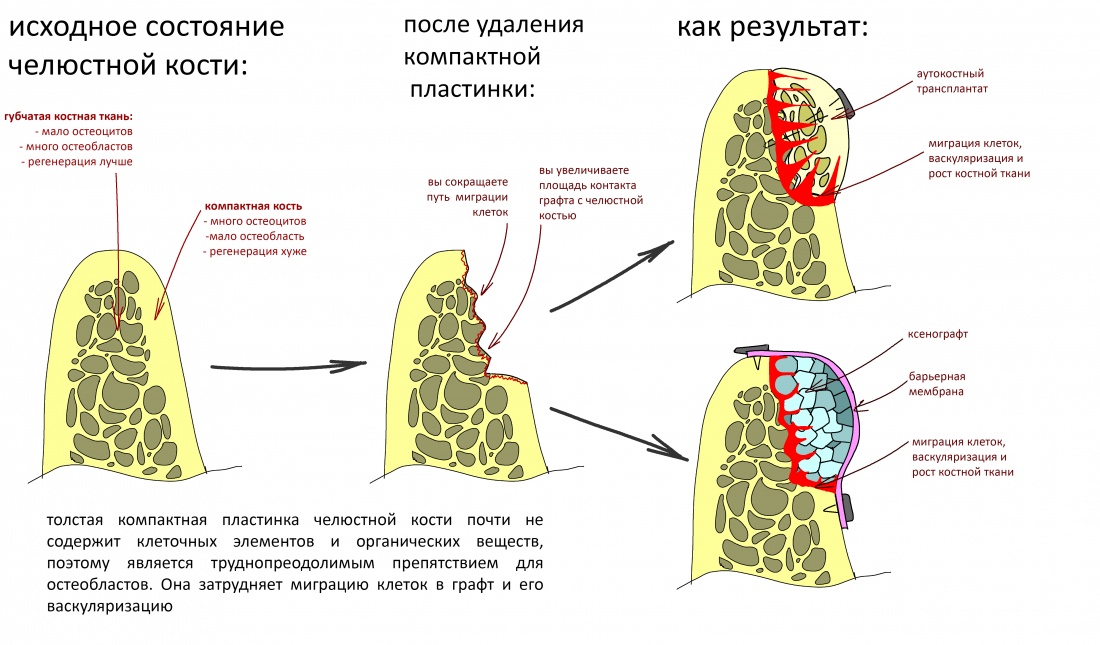
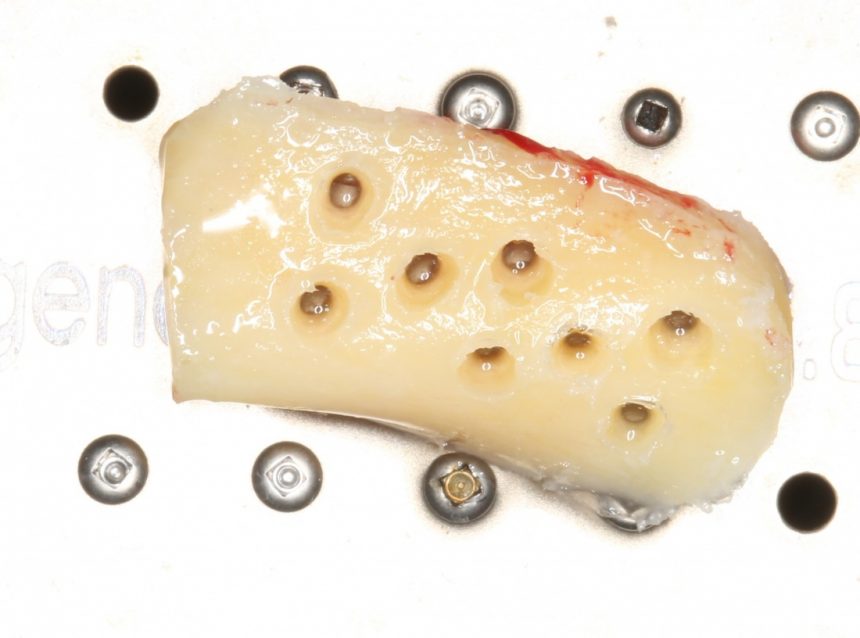
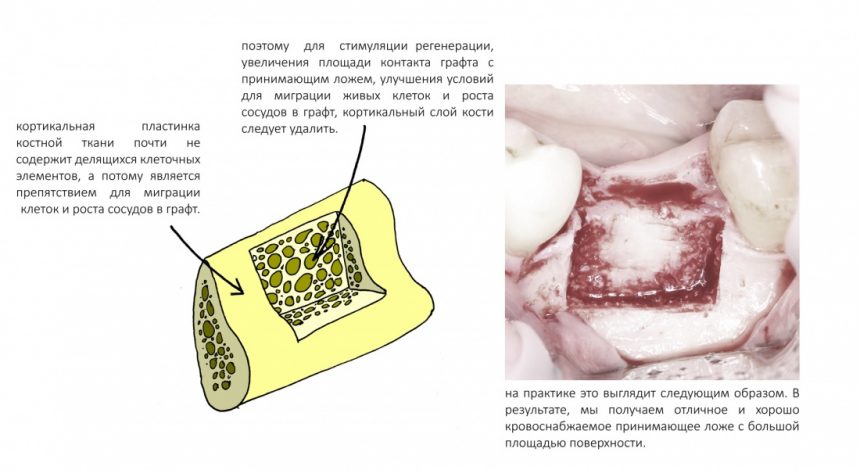
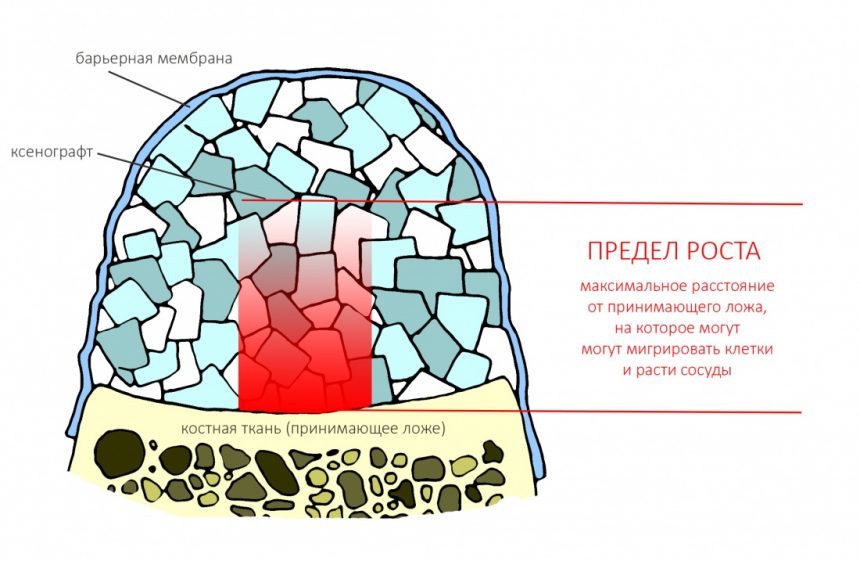
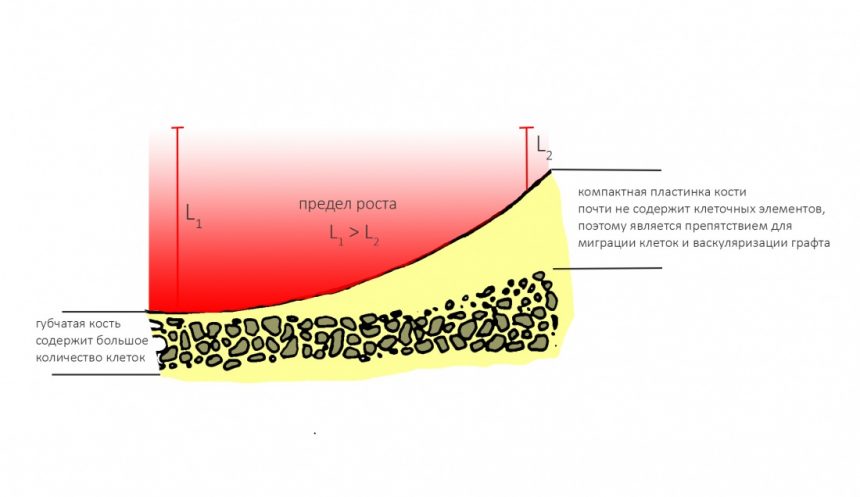
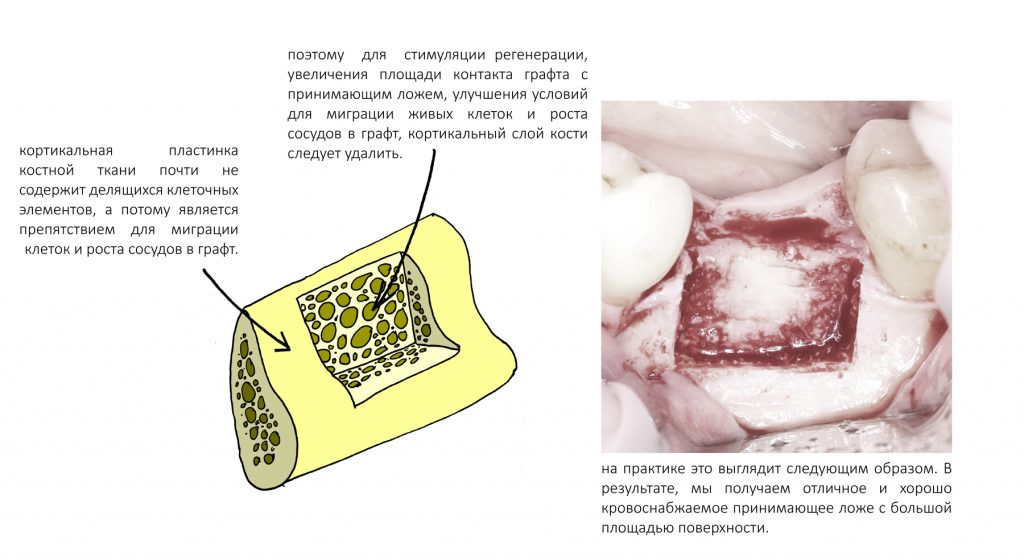
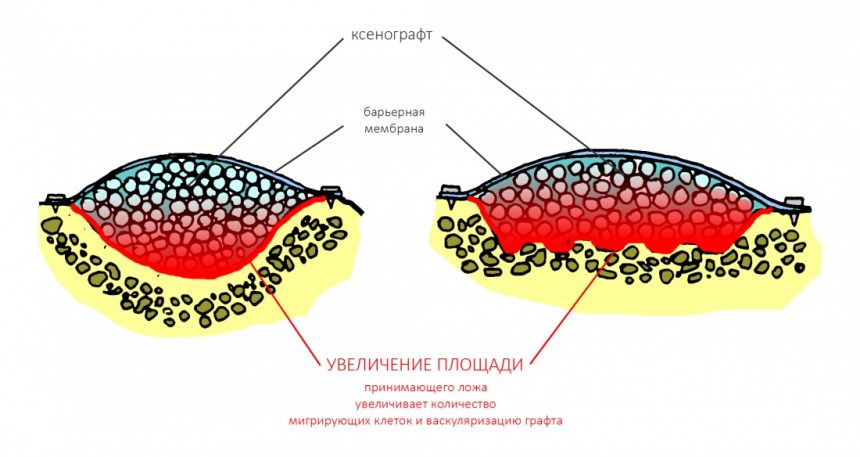
Если ты читал мои предыдущие публикации, посвященные остеопластике, то наверняка знаешь, что костное ложе перед фиксацией графта (любого графта) требует некоторой подготовки. В основном она заключается в полном или частичном удалении кортикального слоя и, применительно к АТККФ — адаптации не только блока под ложе, но и ложа под пересаживаемый костный блок. Подробности здесь>>
Ежу понятно, что к необходимости этих манипуляций мы пришли не сразу. А тогда был 2013 год… и у меня были мысли, что подготовка костного ложа нужна не всегда и не всем. Здесь я понадеялся на размер костного дефекта и большую площадь контакта между костным аутотрансплантатом и принимающим ложем. Конечно, сейчас я сделал бы немного по-другому.
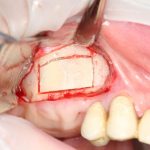
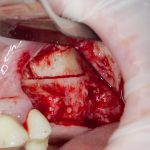
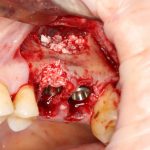
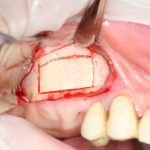
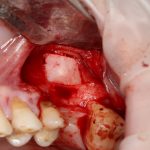
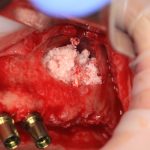
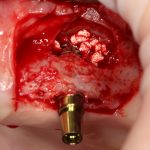
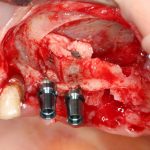
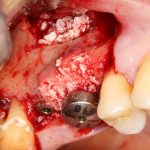
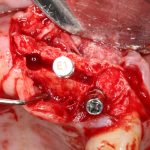
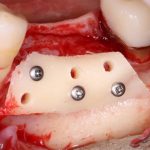
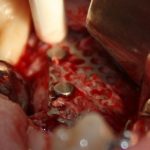
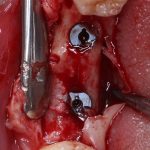
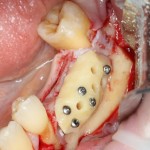
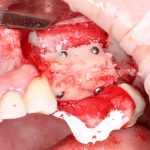
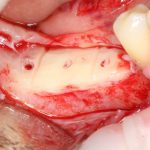
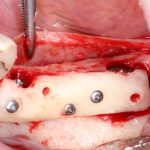
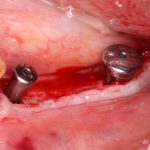
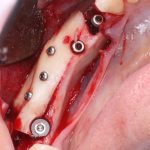
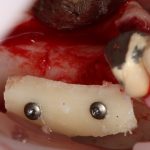
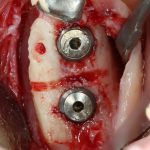
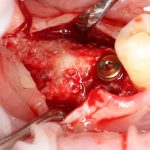
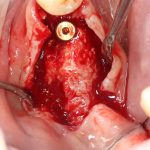
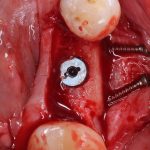
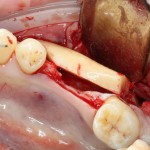
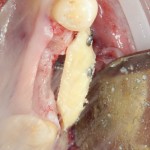
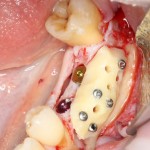
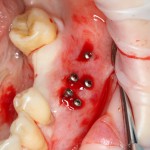
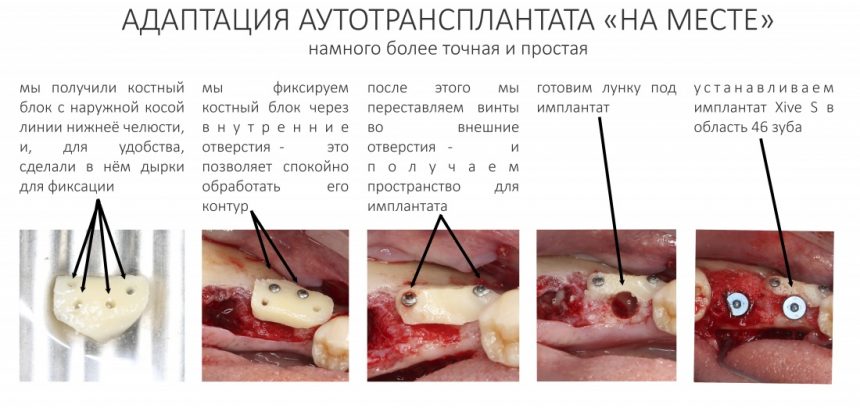
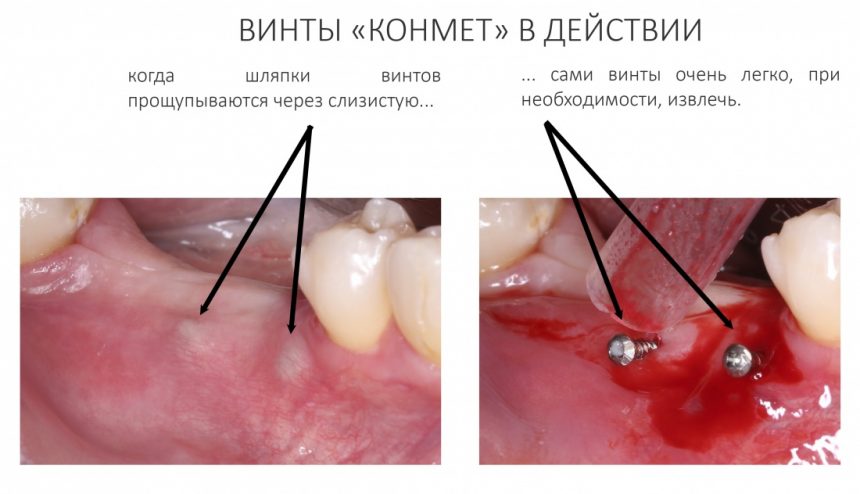
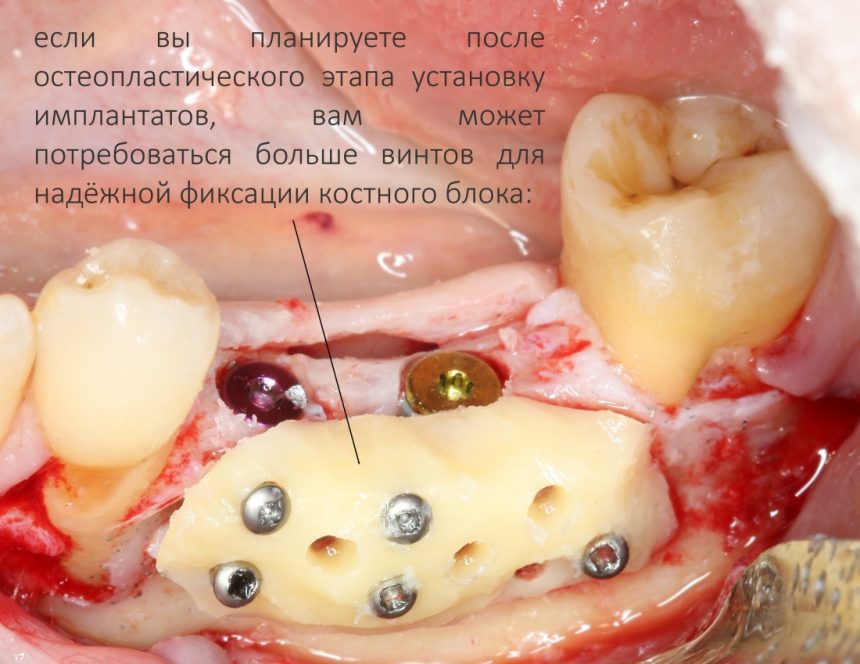
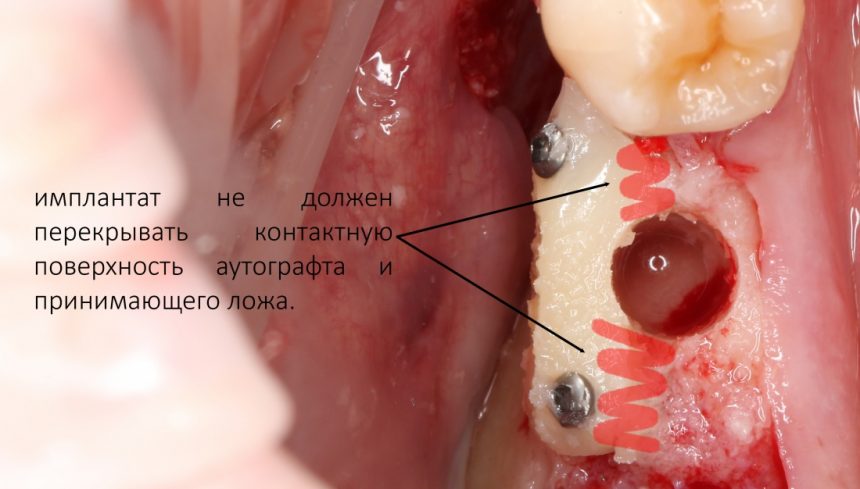
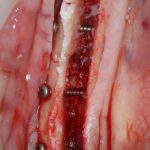
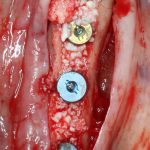
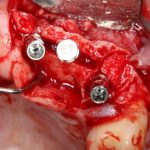
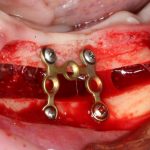
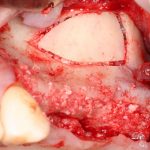
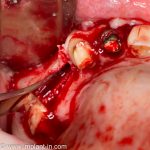
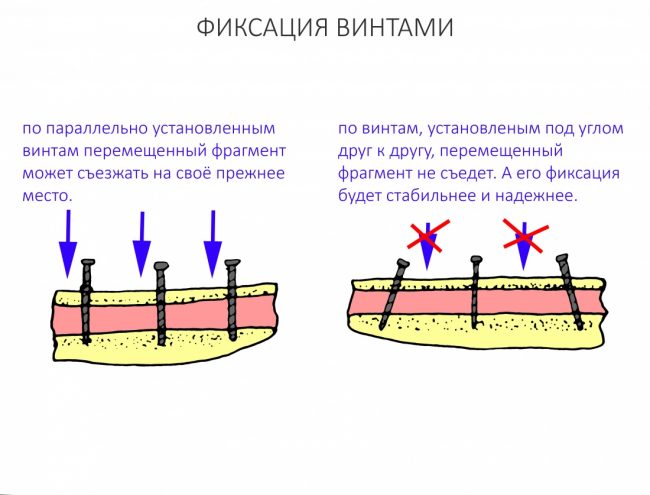
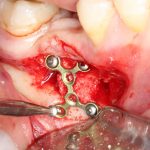
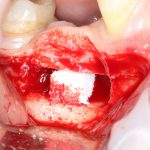
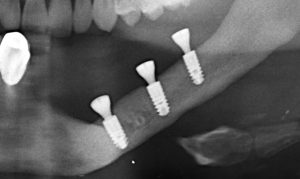
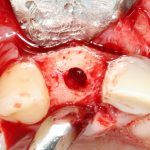
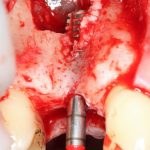
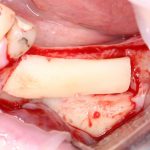
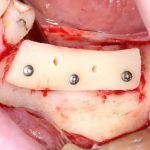
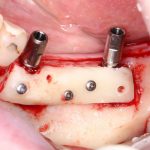
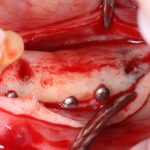
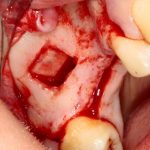
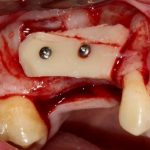
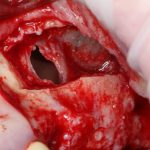
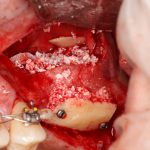
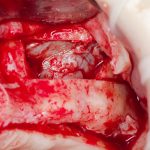
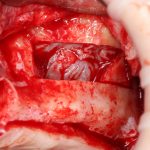
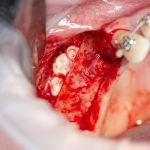
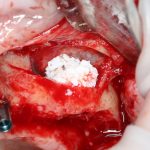
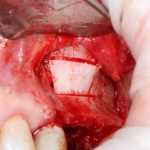
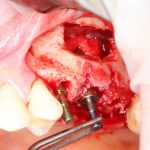
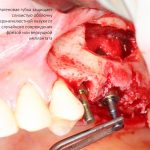
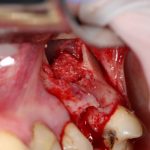
Я зафиксировал костный блок практически без адаптации на несколько винтов. Обрати внимание, что винты находятся в зоне, где не планируется установка имплантатов. Фиксация должна быть надежной, поскольку мне еще предстояла подготовка лунок для имплантатов. Трех винтов для этого вполне достаточно.
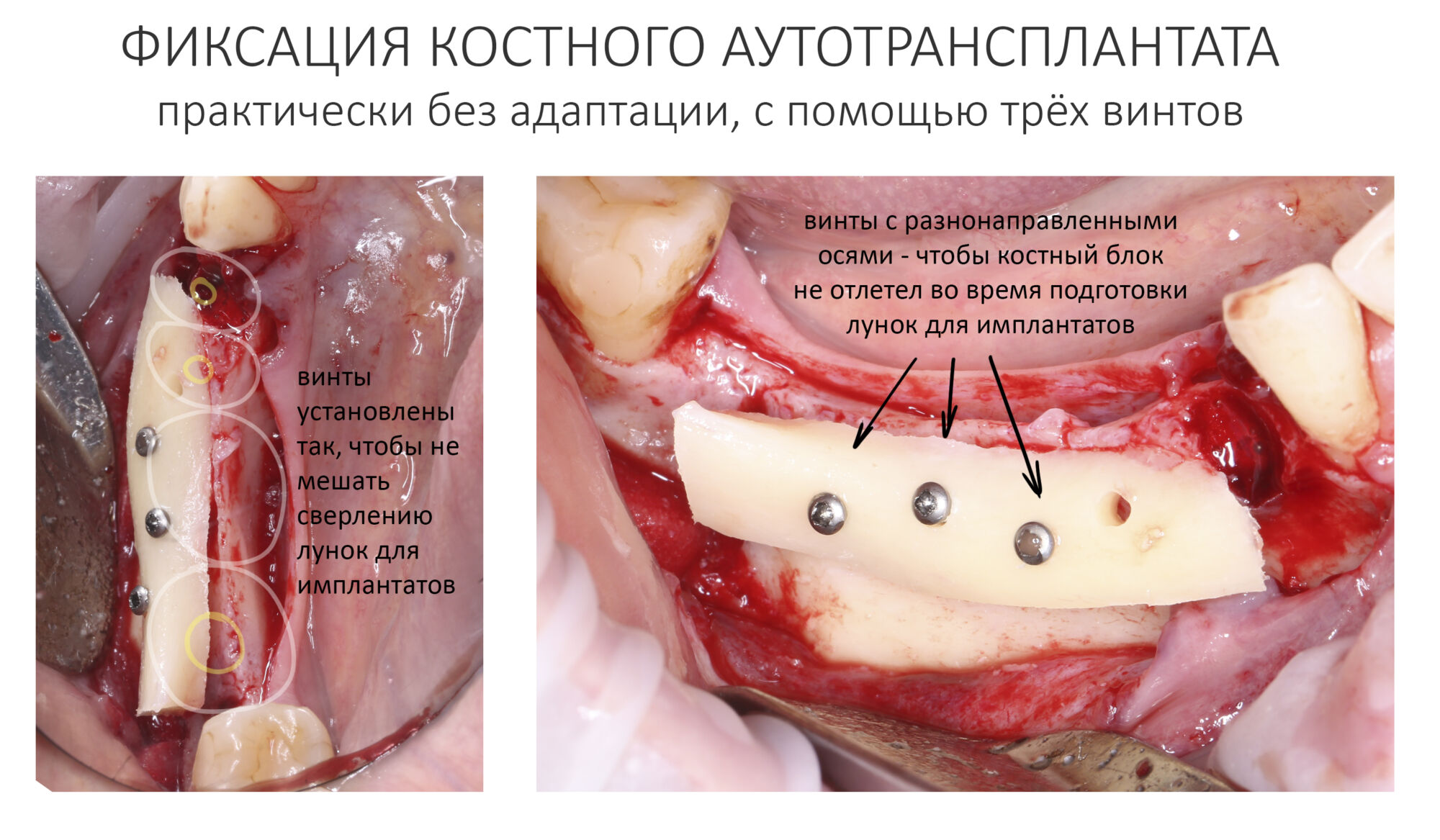 Дальнейшая адаптация костного блока свелась к сглаживанию острых краев. После чего я приступил к подготовке лунок и установке имплантатов.
Дальнейшая адаптация костного блока свелась к сглаживанию острых краев. После чего я приступил к подготовке лунок и установке имплантатов.
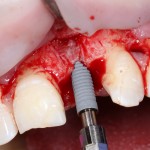
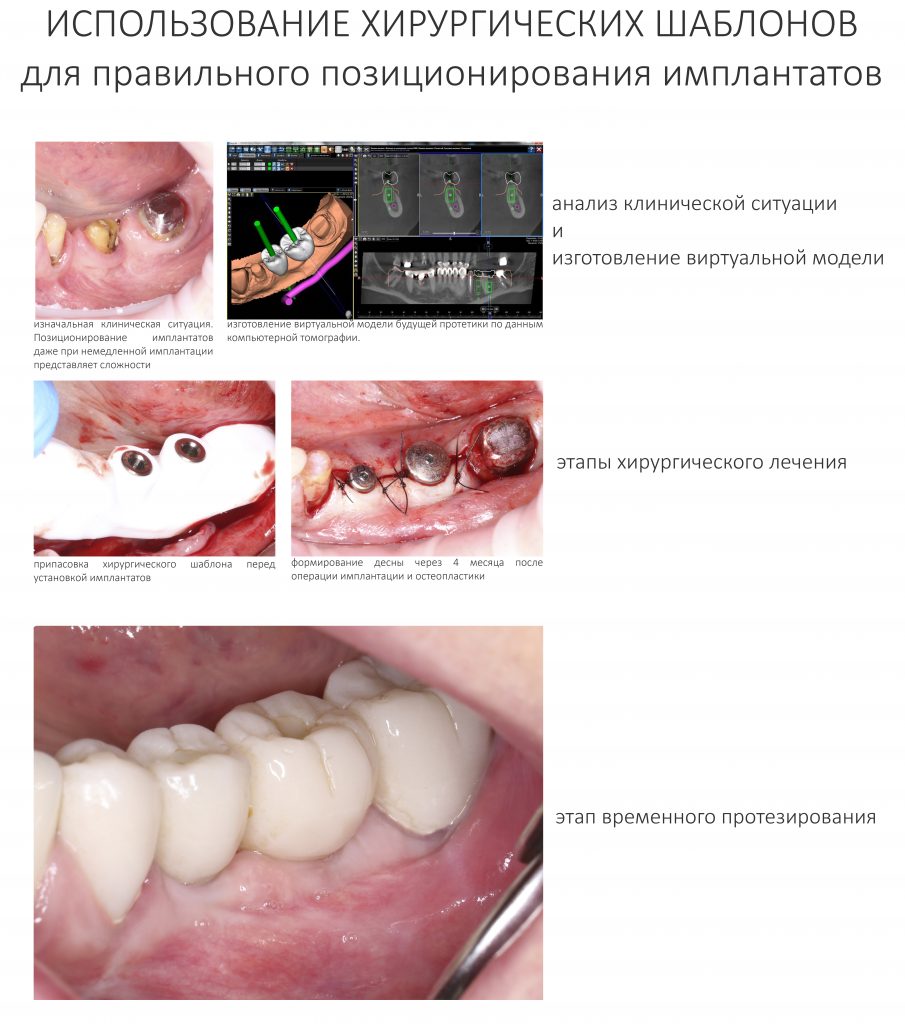
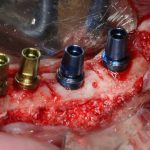
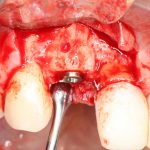
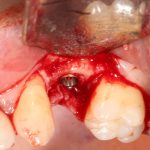
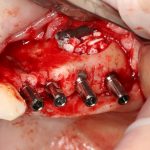
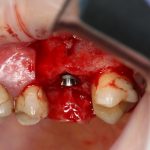
Установка имплантатов.
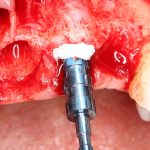
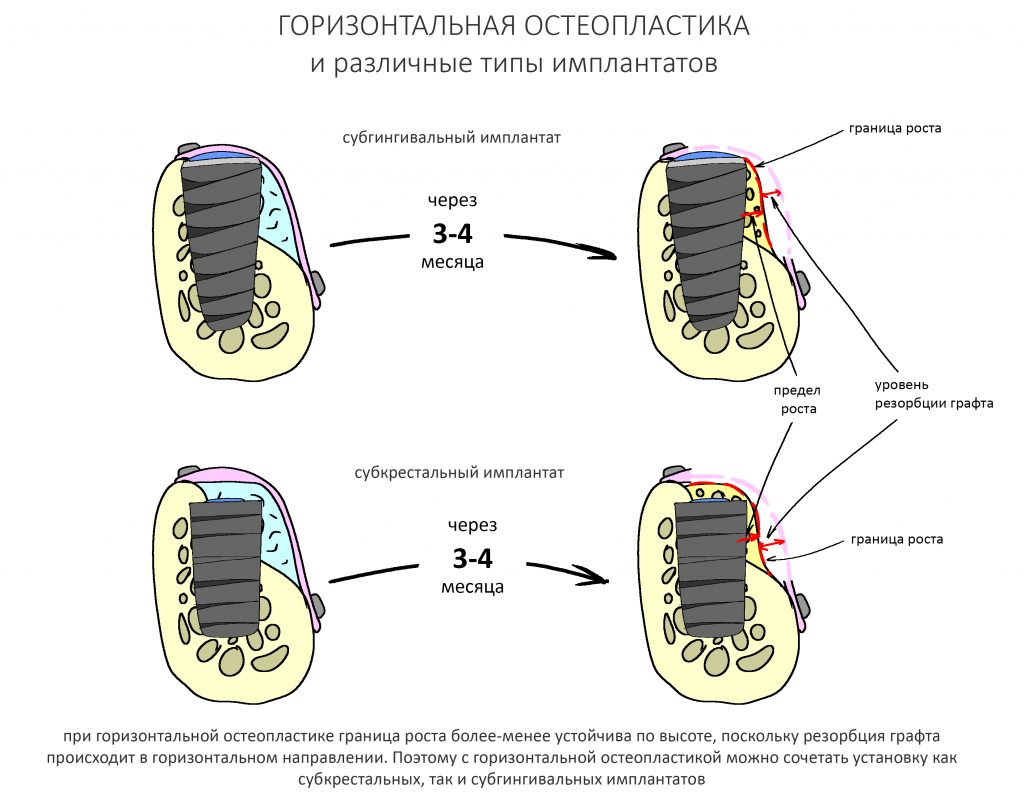
Напомню, что для этой работы я выбрал субкрестальные имплантаты Ankylos C/X. Они прекрасно сочетаются с любым методом остеопластики.
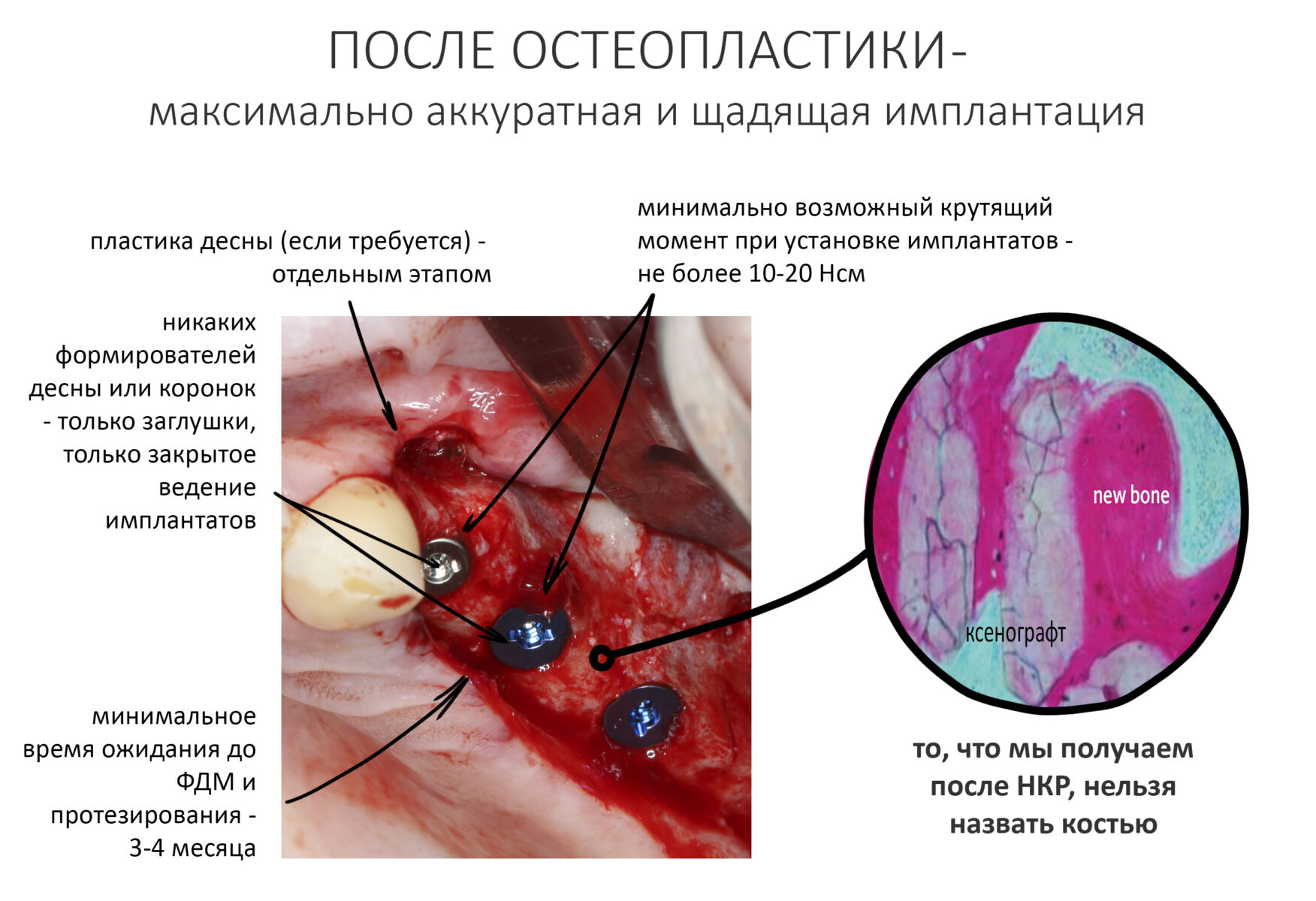
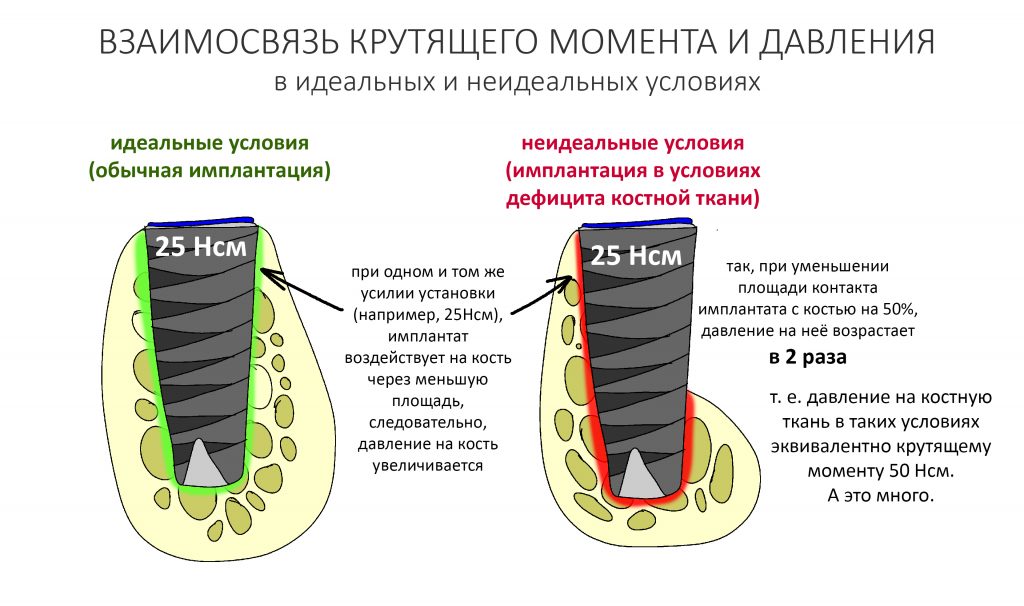
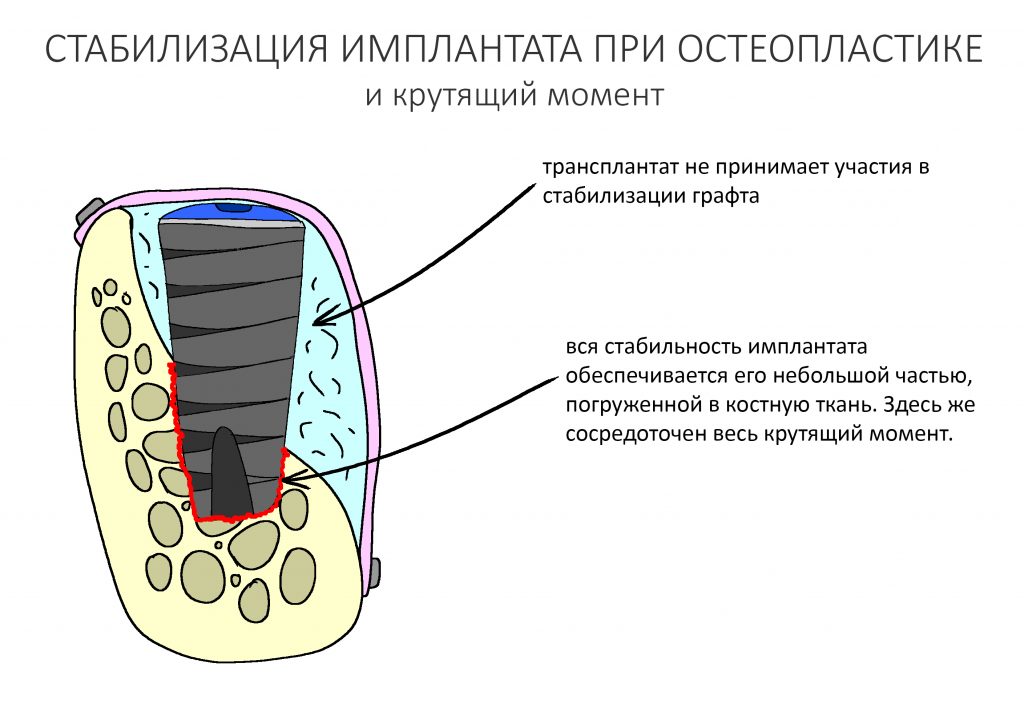
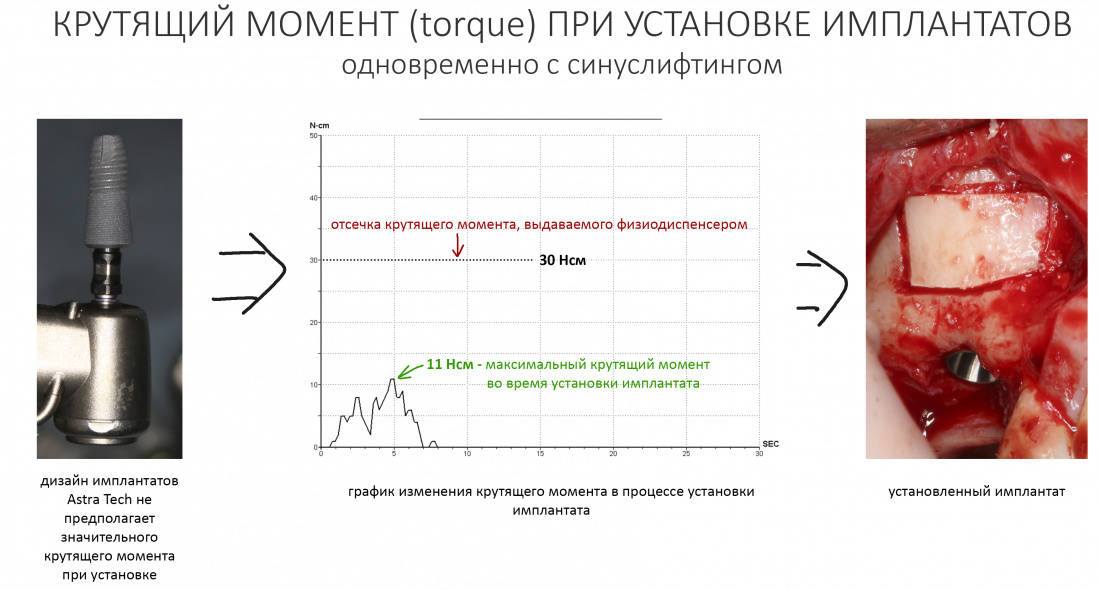
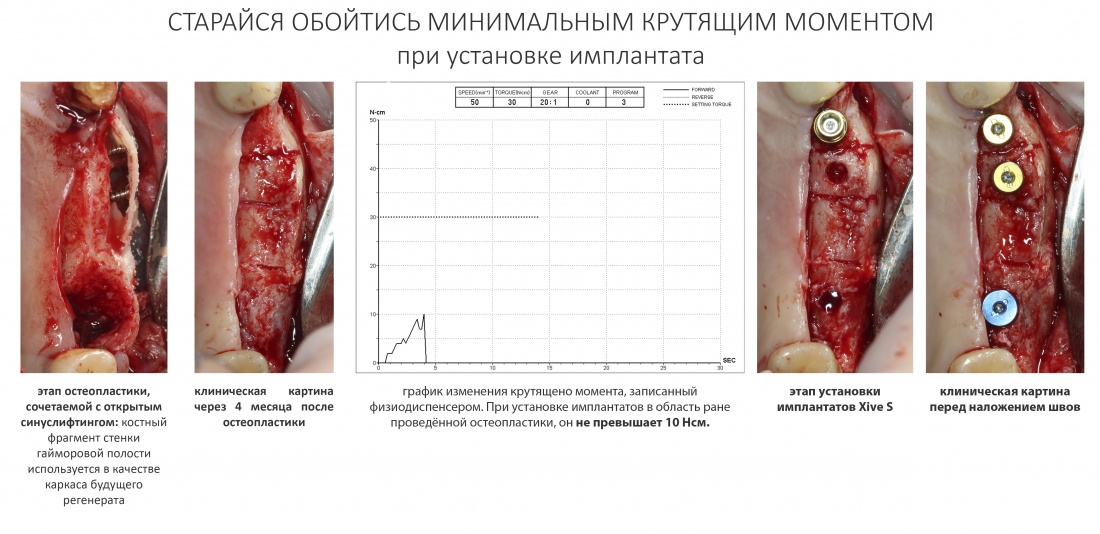
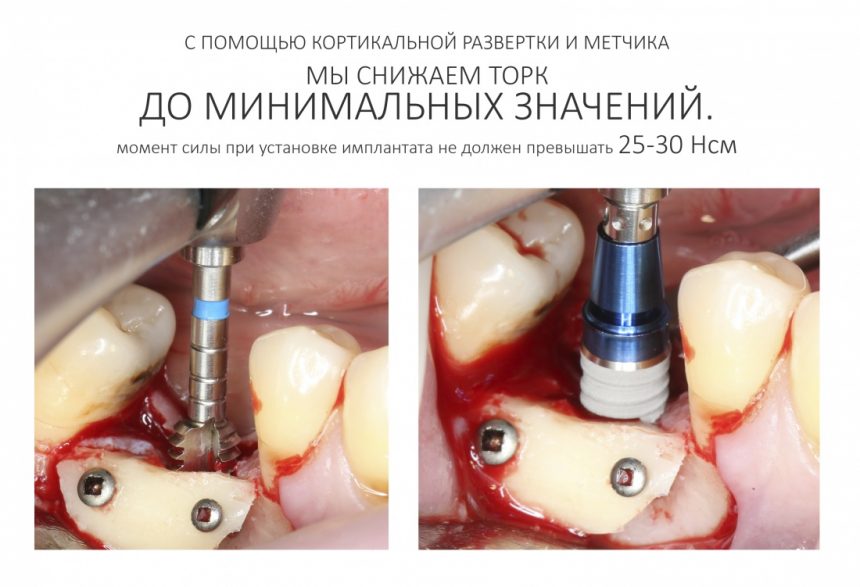
Я не планирую установку супраструктур или коронок, поэтому на уровень первичной стабильности можно положить болт. Даже наоборот — чем меньше крутящий момент при установке, тем лучше. Для имплантатов Ankylos и подобных им, это особенно важно. В общем, момент силы при установке — не более 10-15 Нсм.
Ремарка: имплантаты с предустановленными имплантодержателями хороши тем, что с ними легко контролировать позиционирование имплантатов. В случае с Ankylos С/Х - еще и крутящий момент. Имплантодержатель должен отсоединяться от имплантата с легким щелчком. Если его клинит, и тебе приходится прикладывать для этого усилия, то ты, однозначно, превысил момент силы во время установки имплантата. Следовательно, жди проблем.
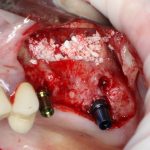
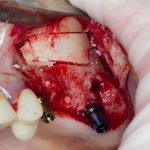
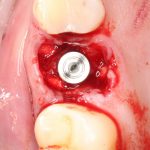
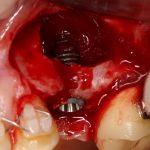
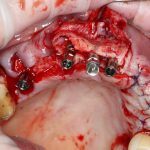
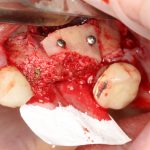
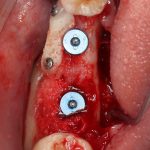
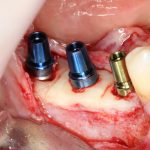
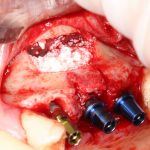
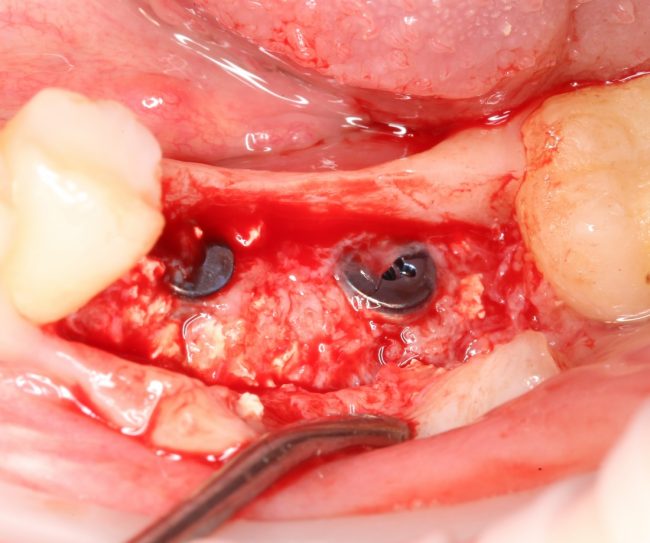
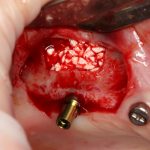
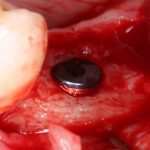
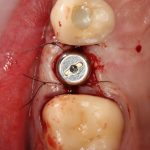
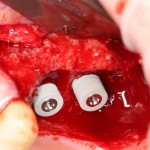
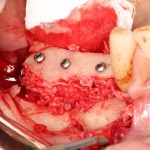
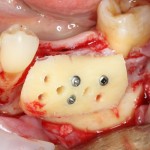
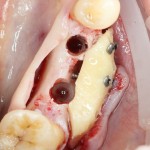
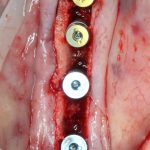
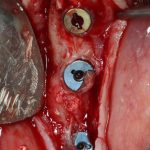
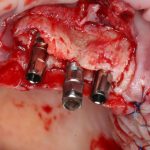
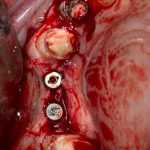
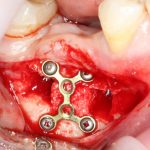
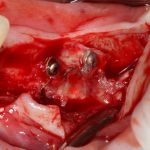
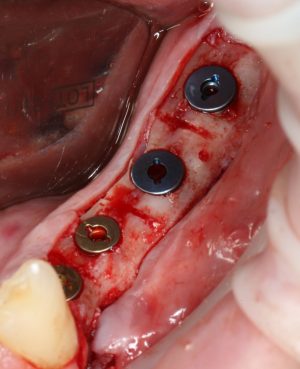
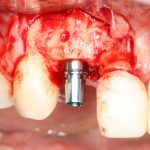
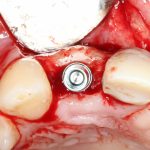
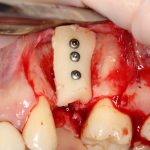
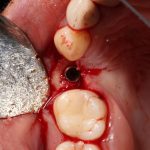
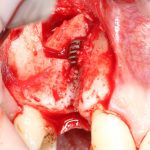
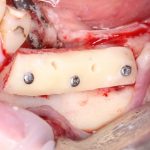
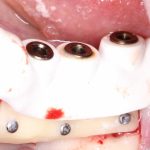
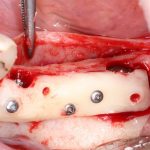
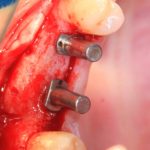
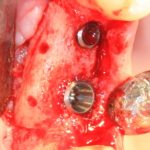
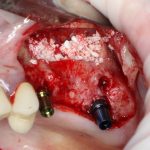
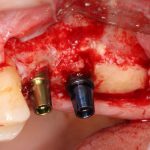
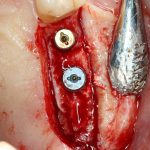
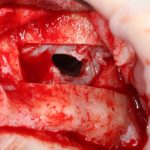
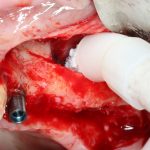
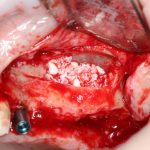
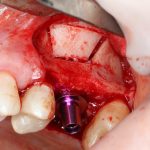
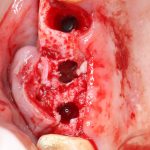
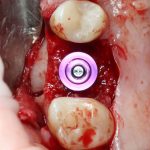
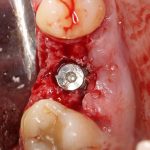
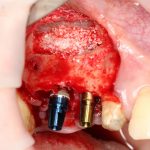
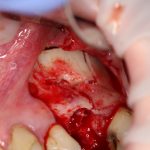
Глянем на то, что получилось:
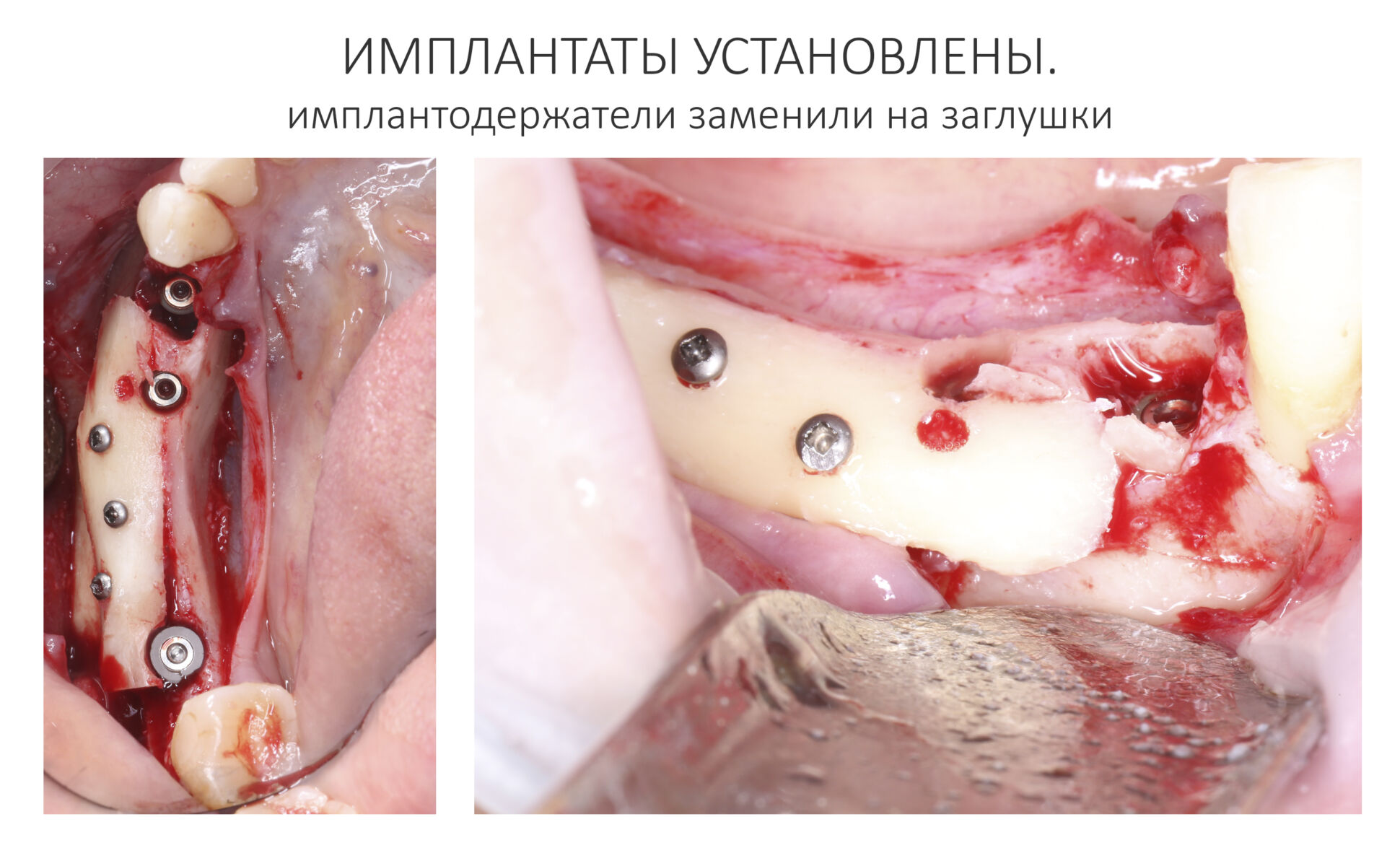 Осталось адаптировать костный блок (убрать острые края), проверить его фиксацию и, при необходимости, добавить винты. Десятисекундное дело.
Осталось адаптировать костный блок (убрать острые края), проверить его фиксацию и, при необходимости, добавить винты. Десятисекундное дело.
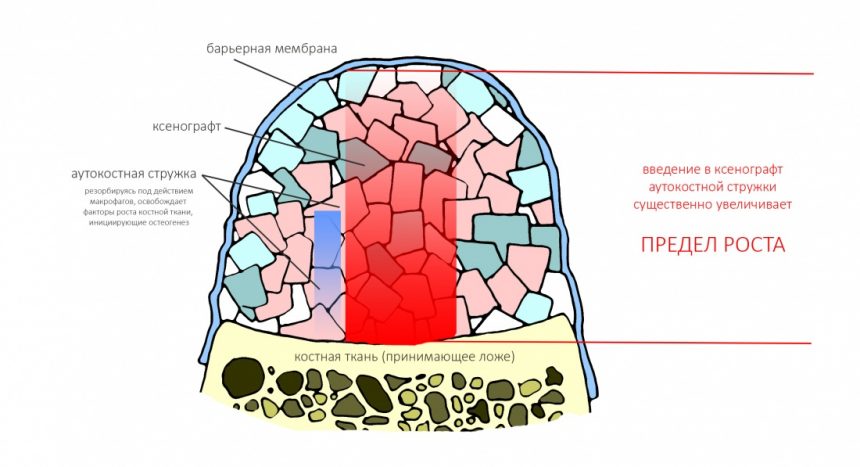
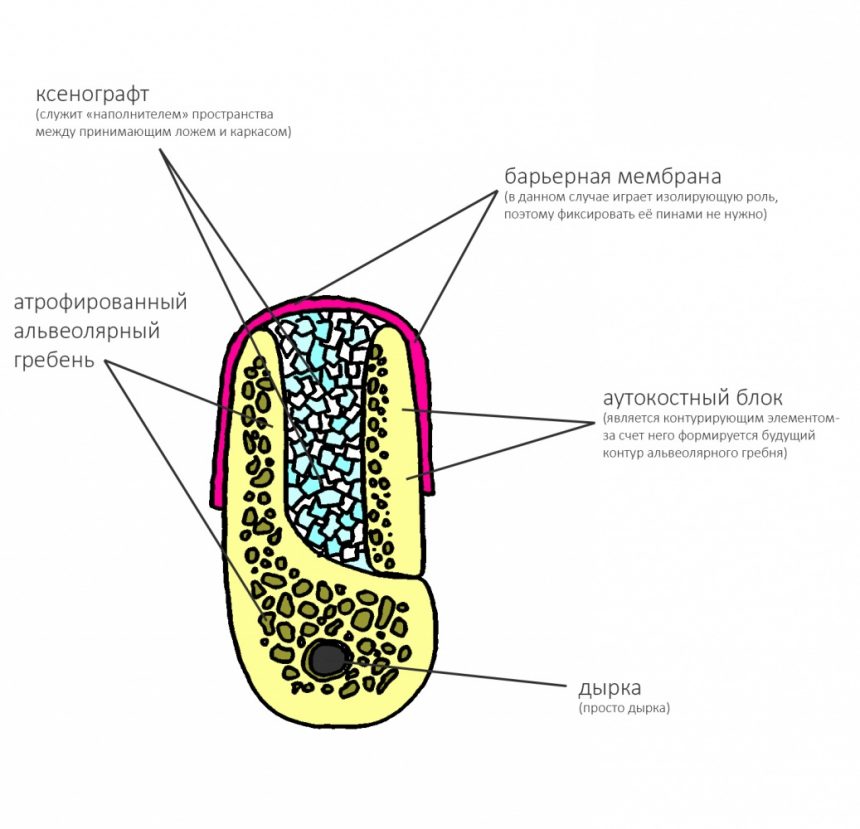
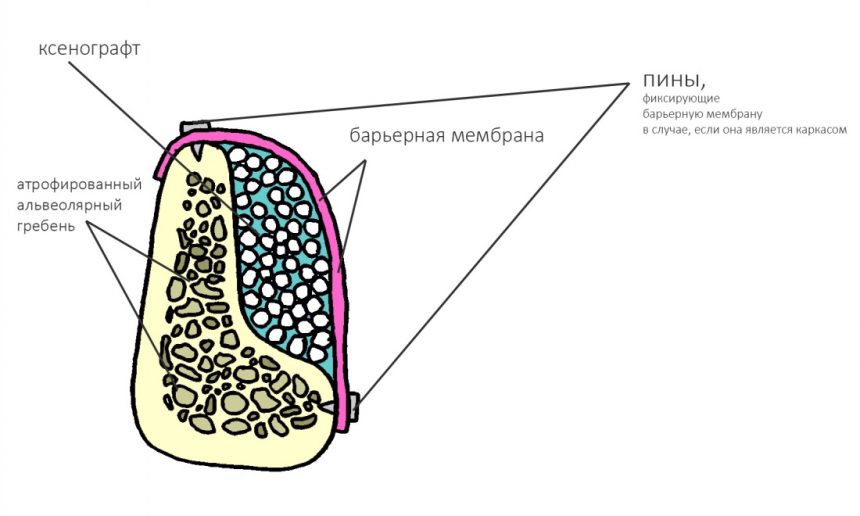
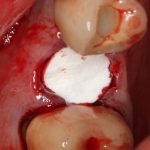
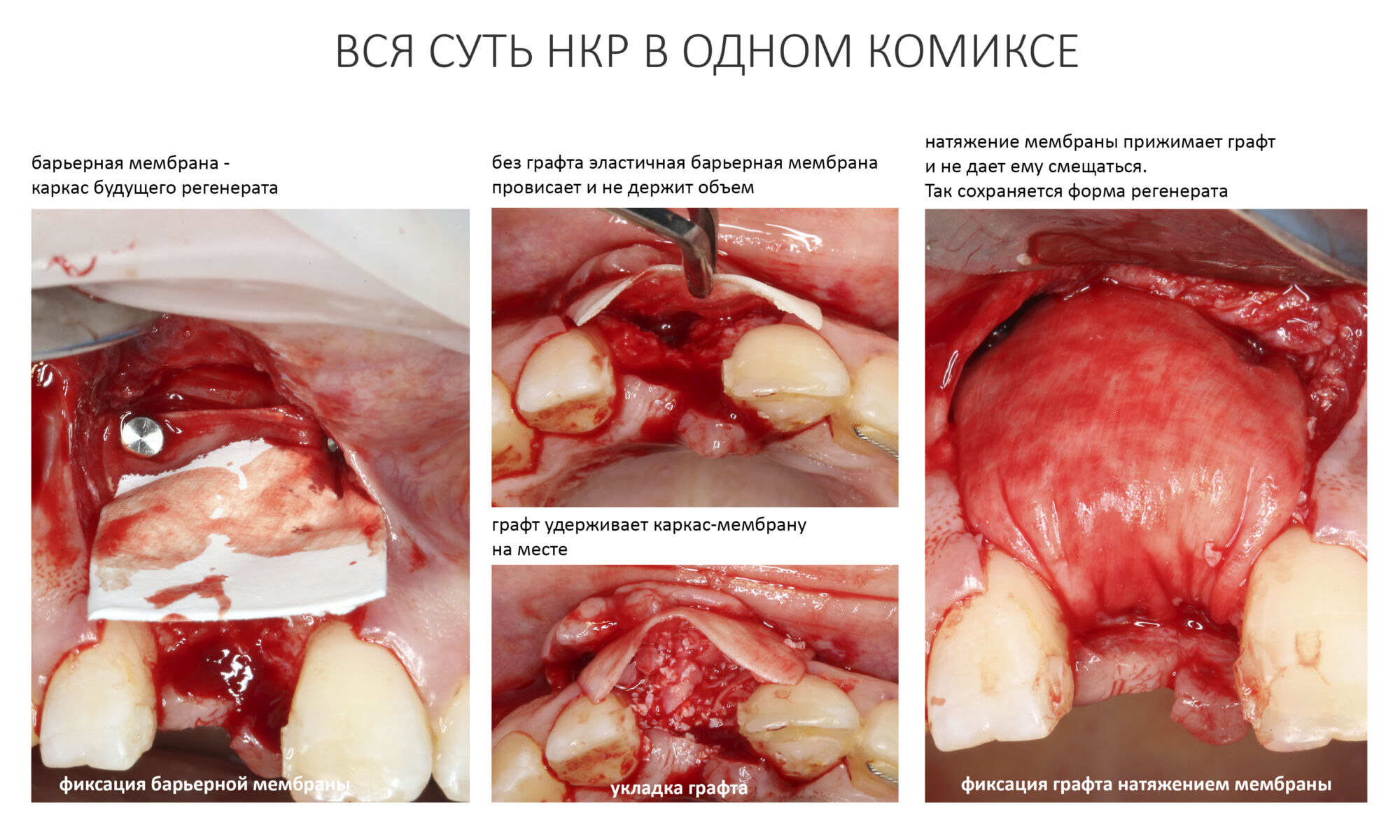
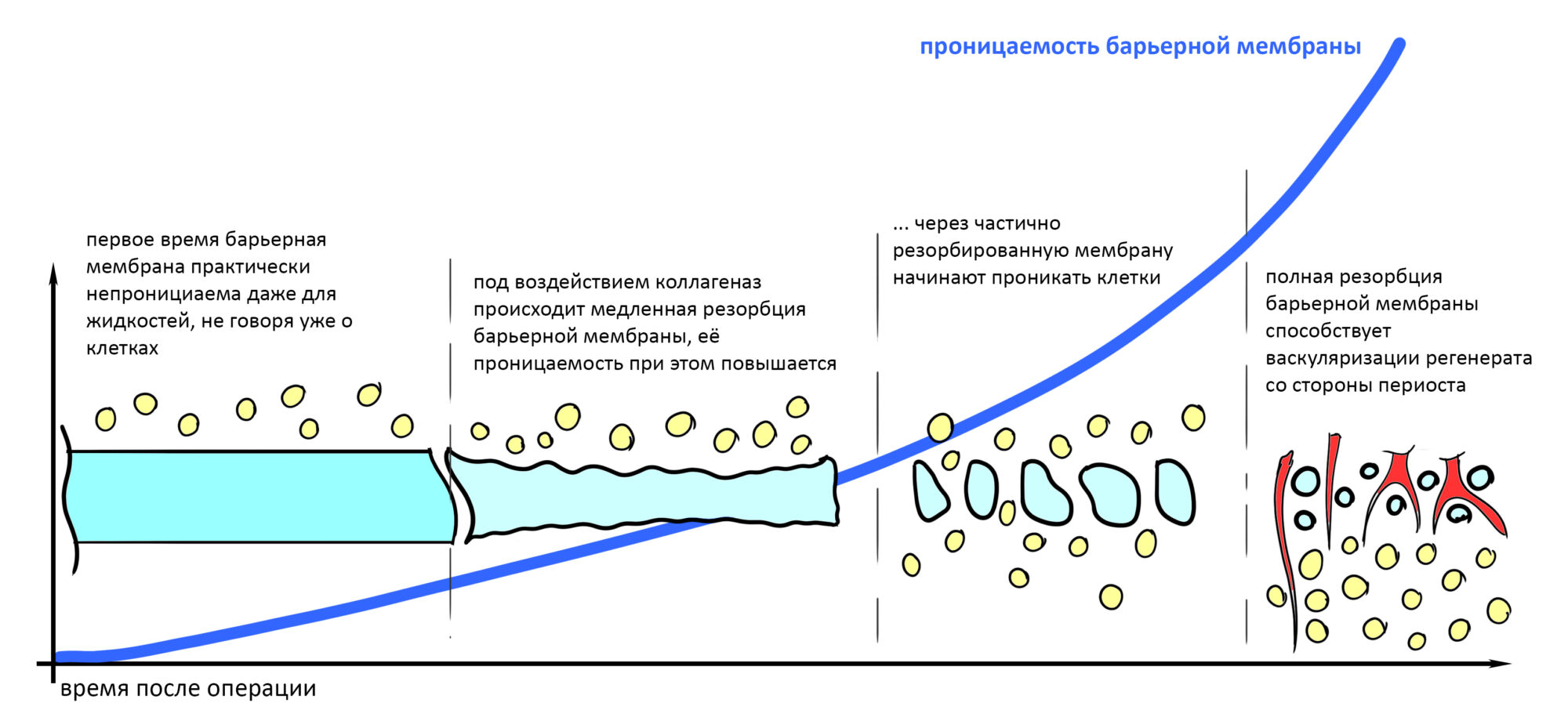
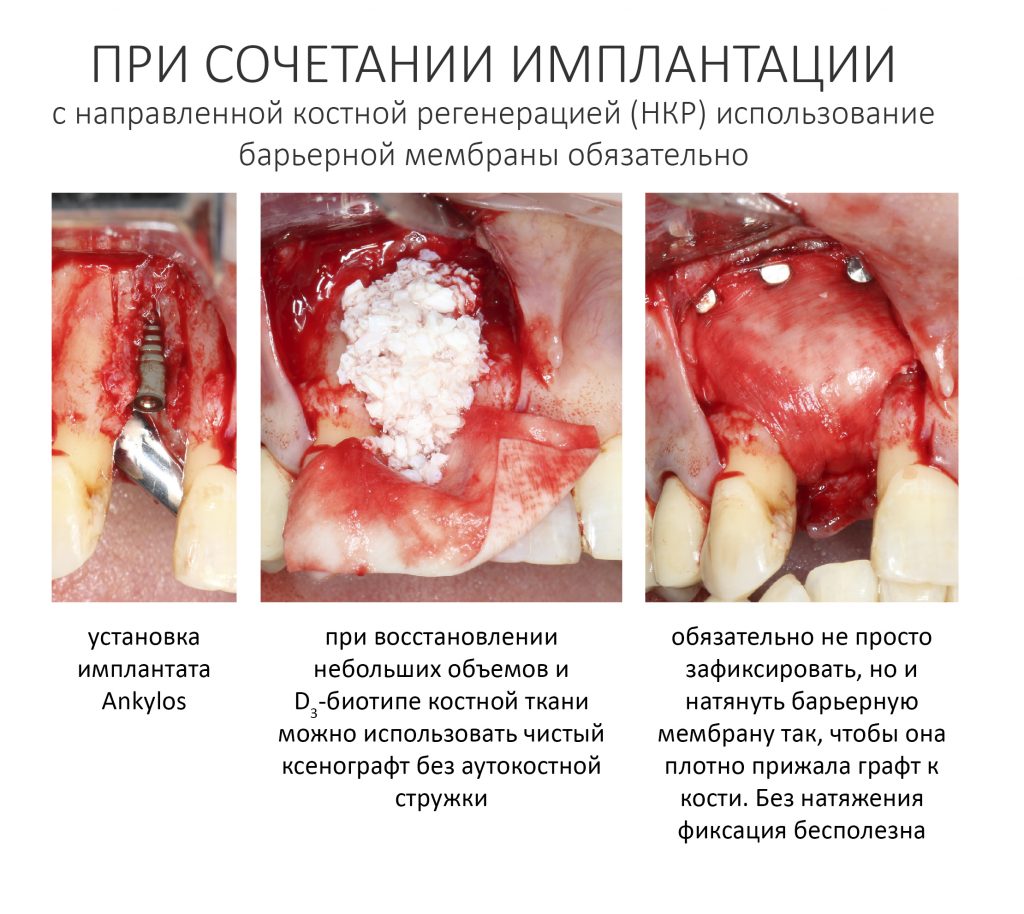
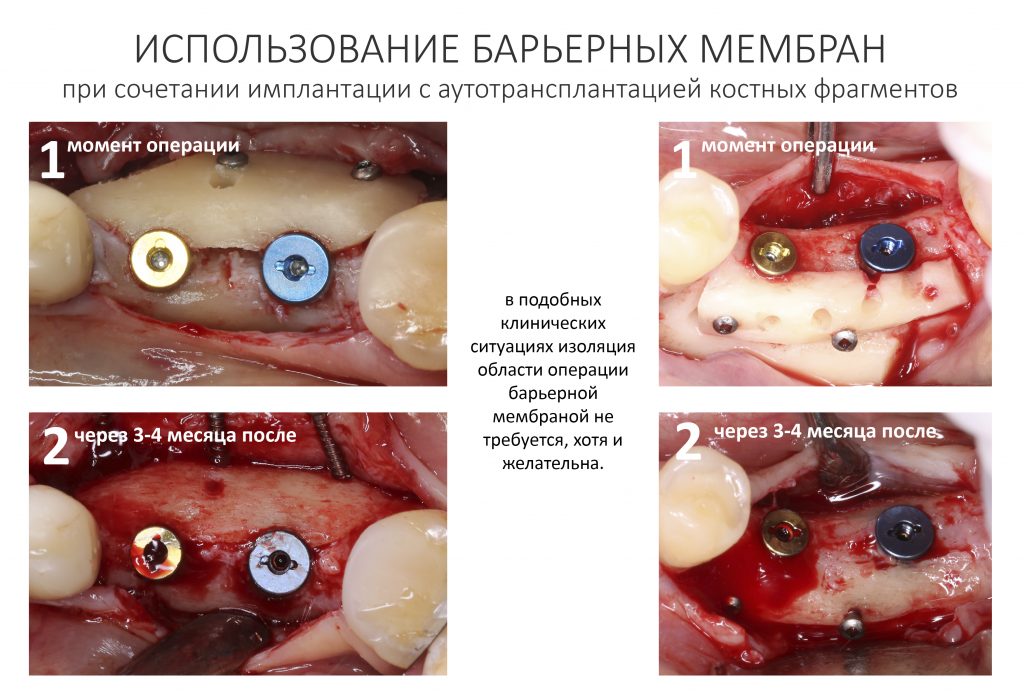
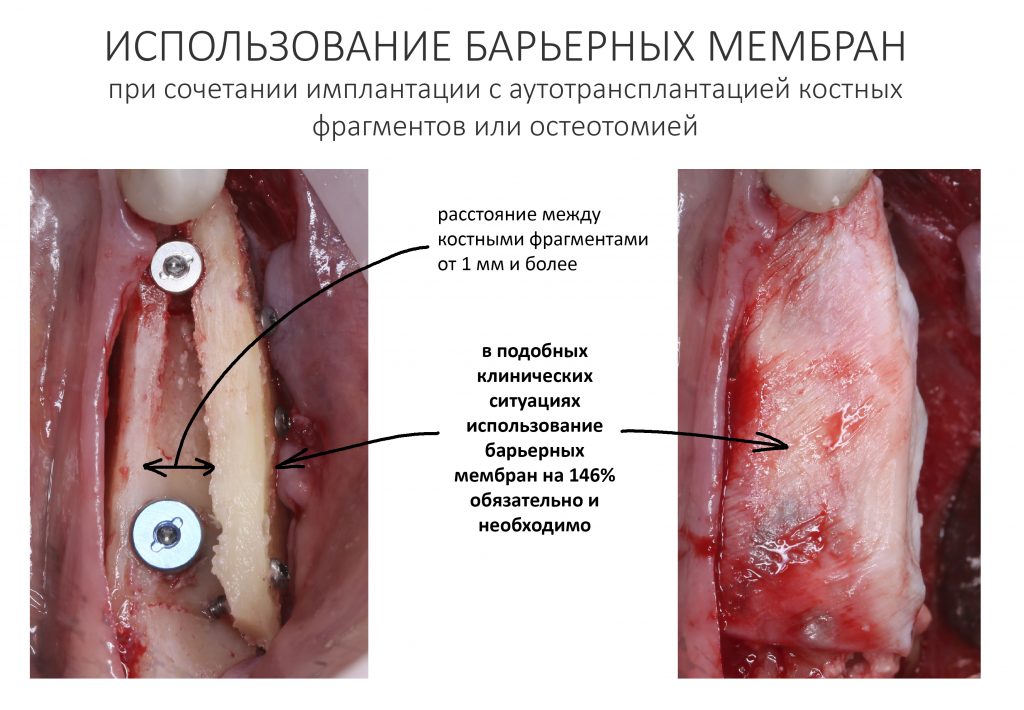
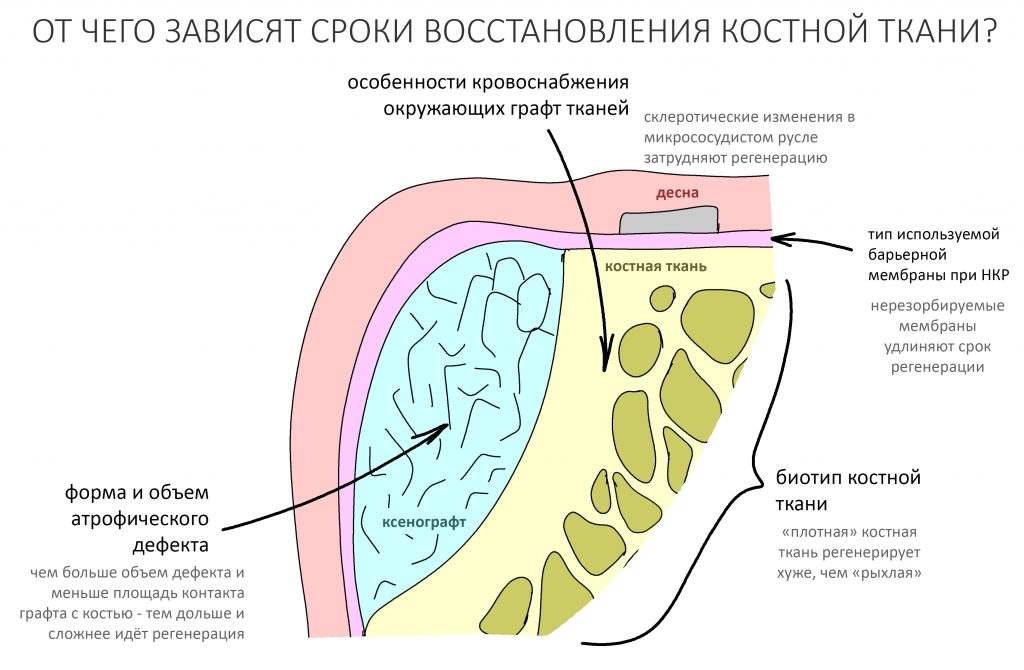
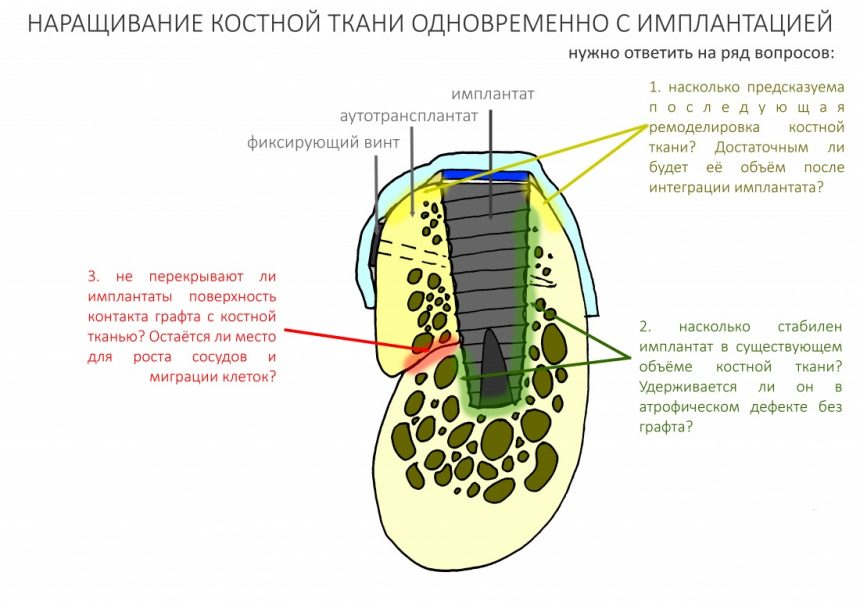
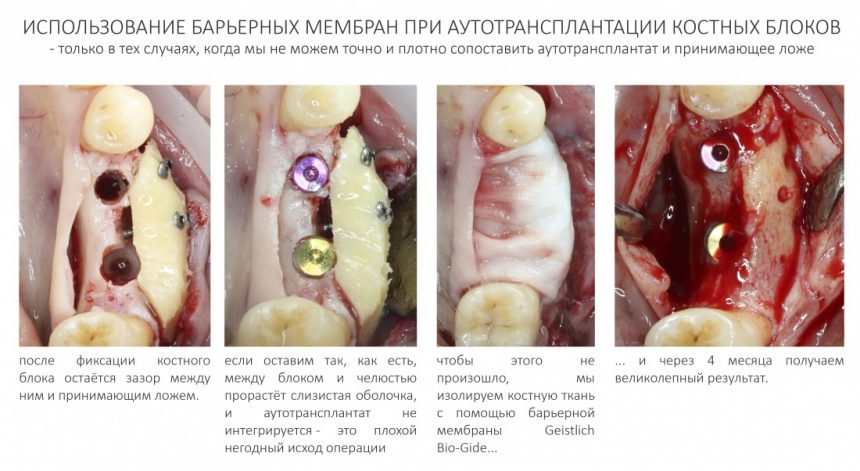
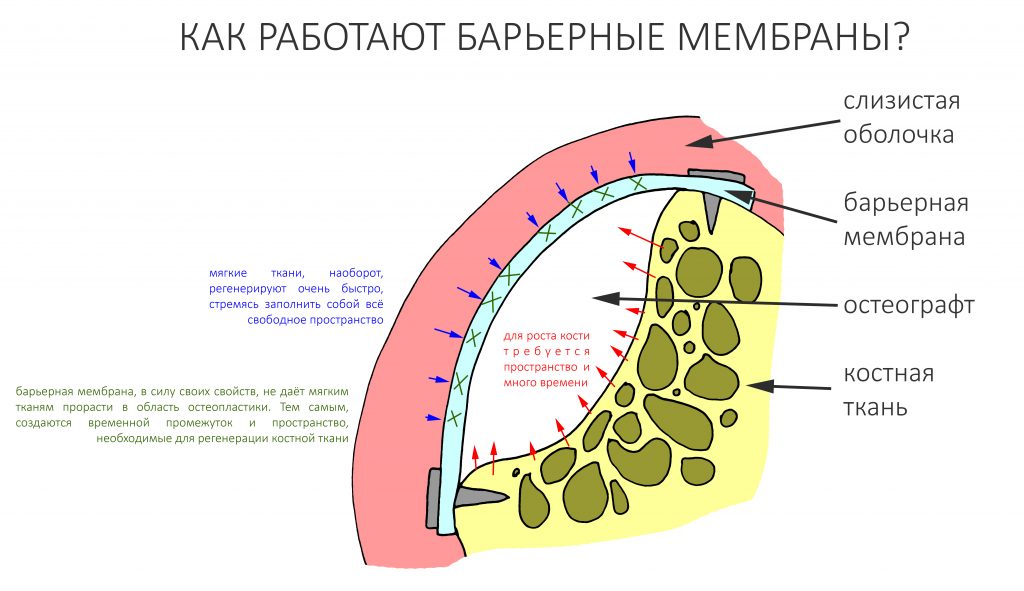
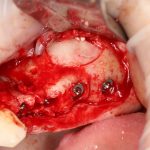
Изоляция области аутографта и имплантатов барьерной мембраной.
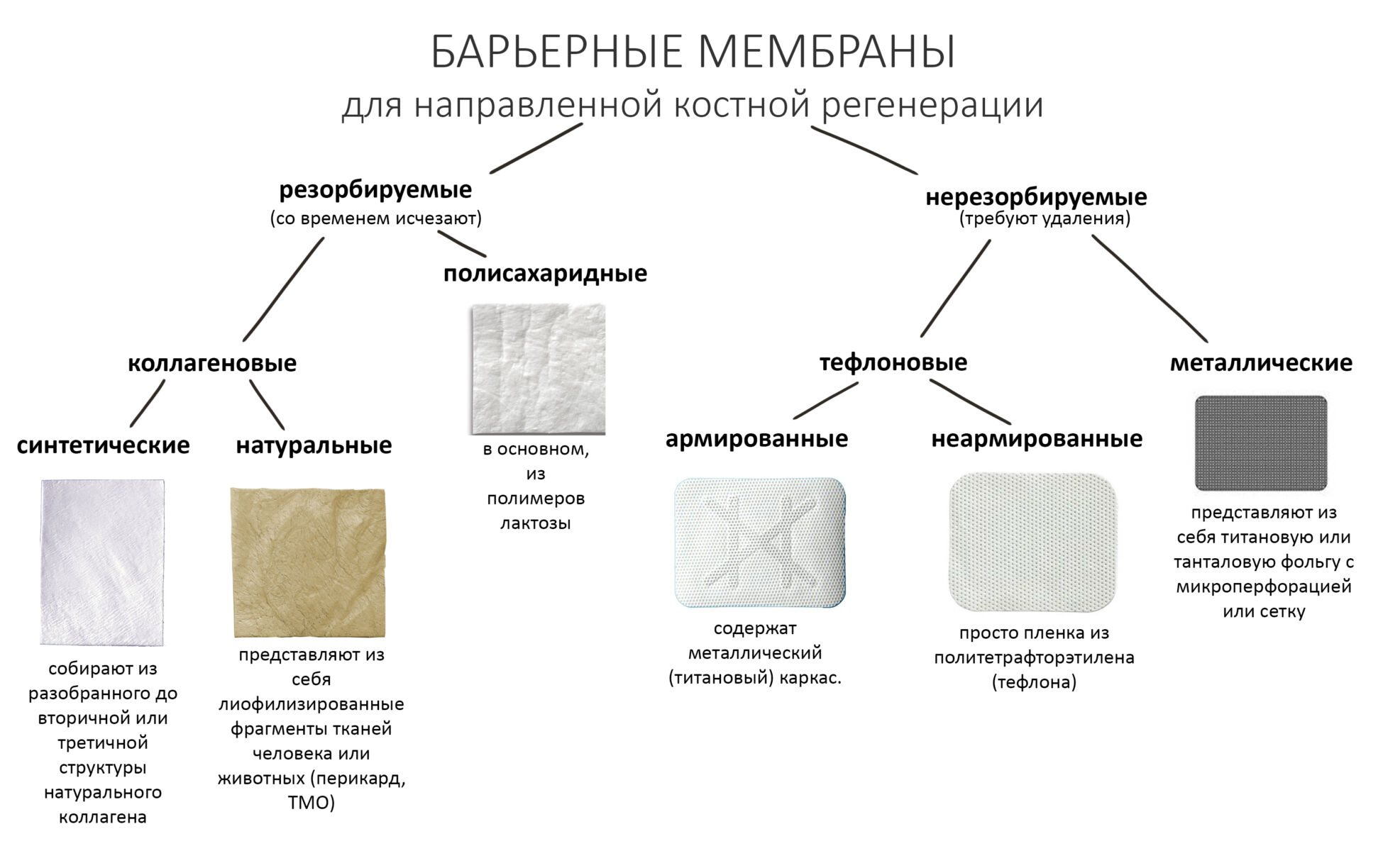
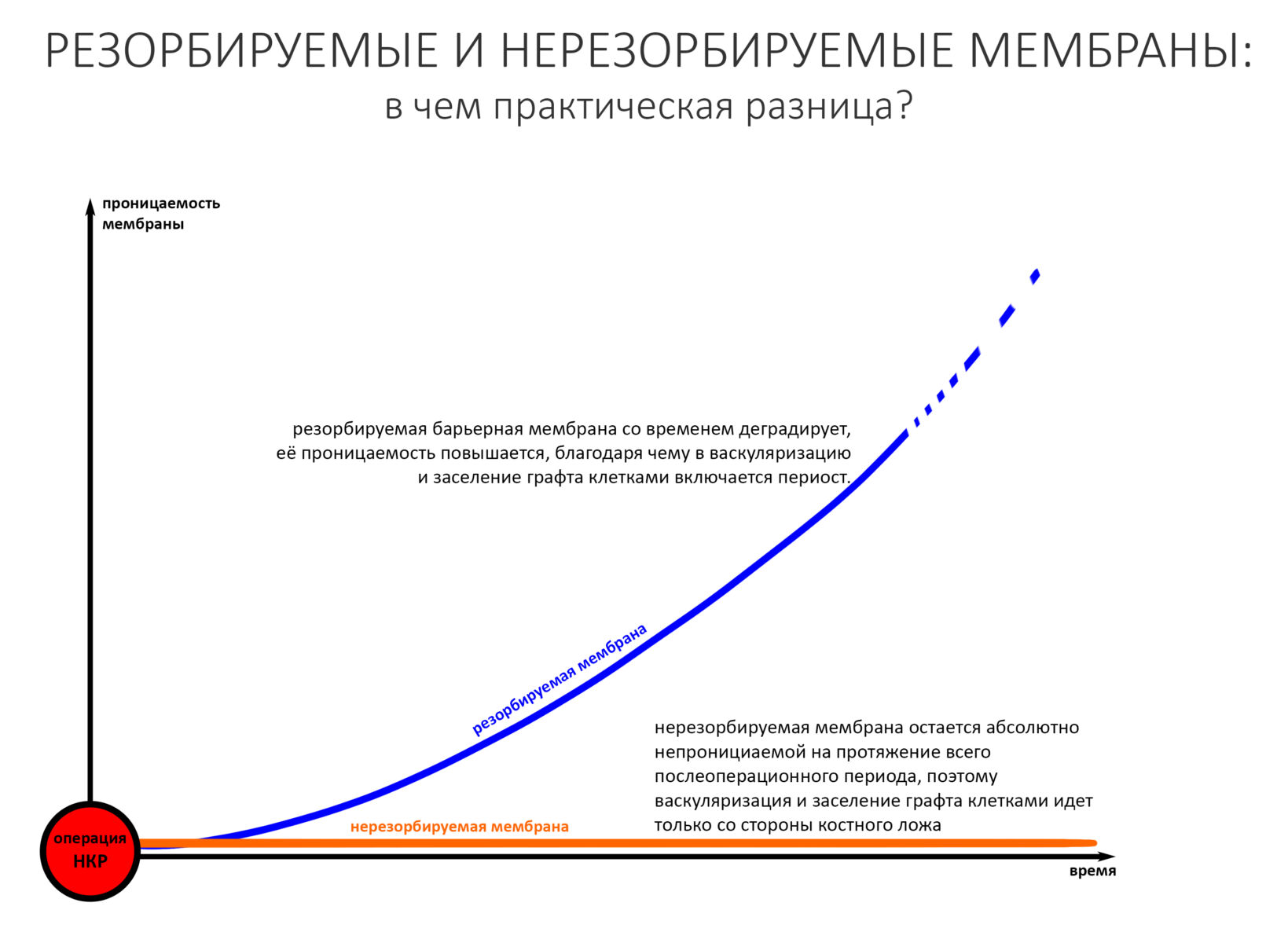
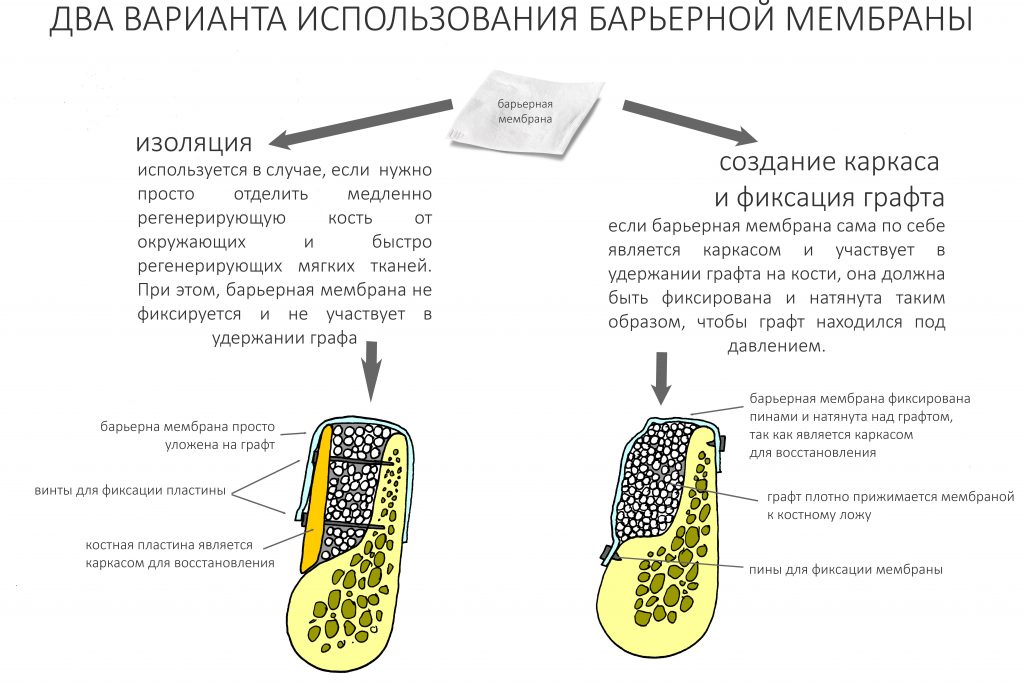
Перекрывать костный блок барьерной мембраной или оставить так? По этому вопросу есть много мнений. Между тем, в публикации по методике есть ясное показание, когда это требуется.
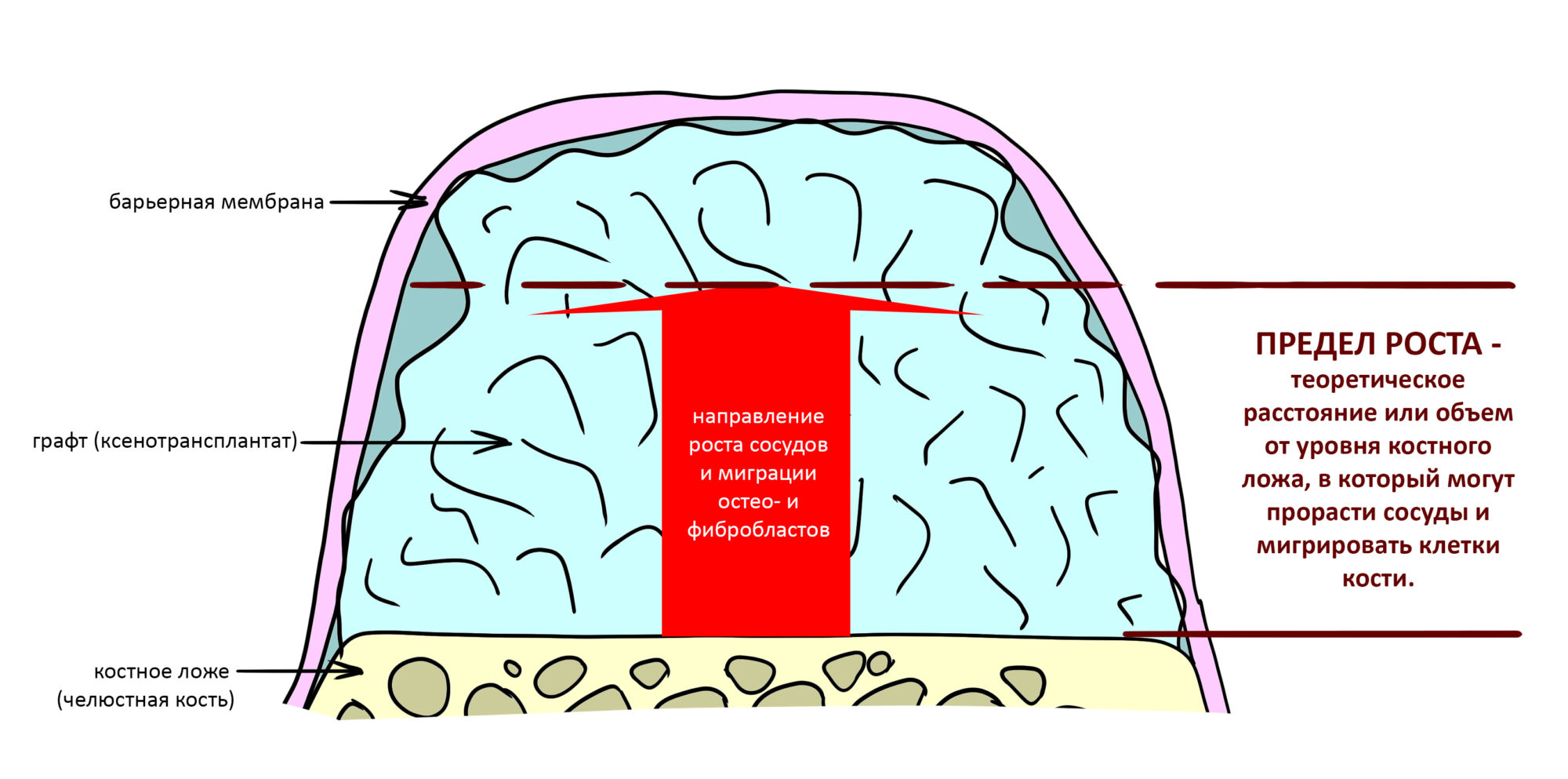
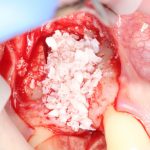
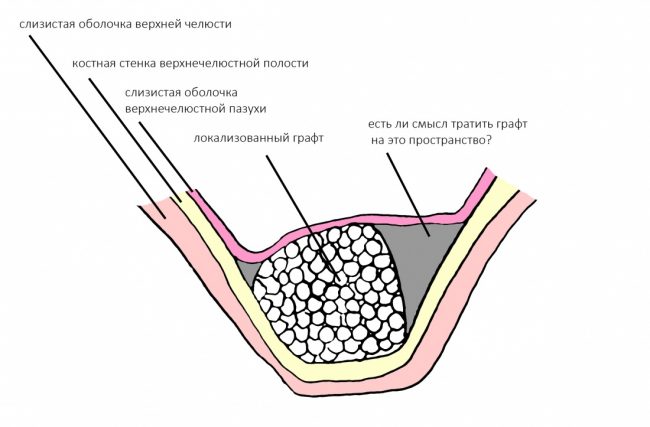
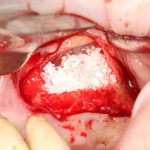
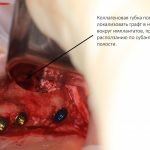
Конкретно в этом клиническом случае между костным аутотрансплантатом, ложем и имплантатами есть пустое пространство. Если его не изолировать от мягких тканей, они прорастут и осложнят интеграцию аутографта. Поэтому я решил перекрыть костный блок барьерной мембраной, пусть это делает хирургическую операцию немного дороже.
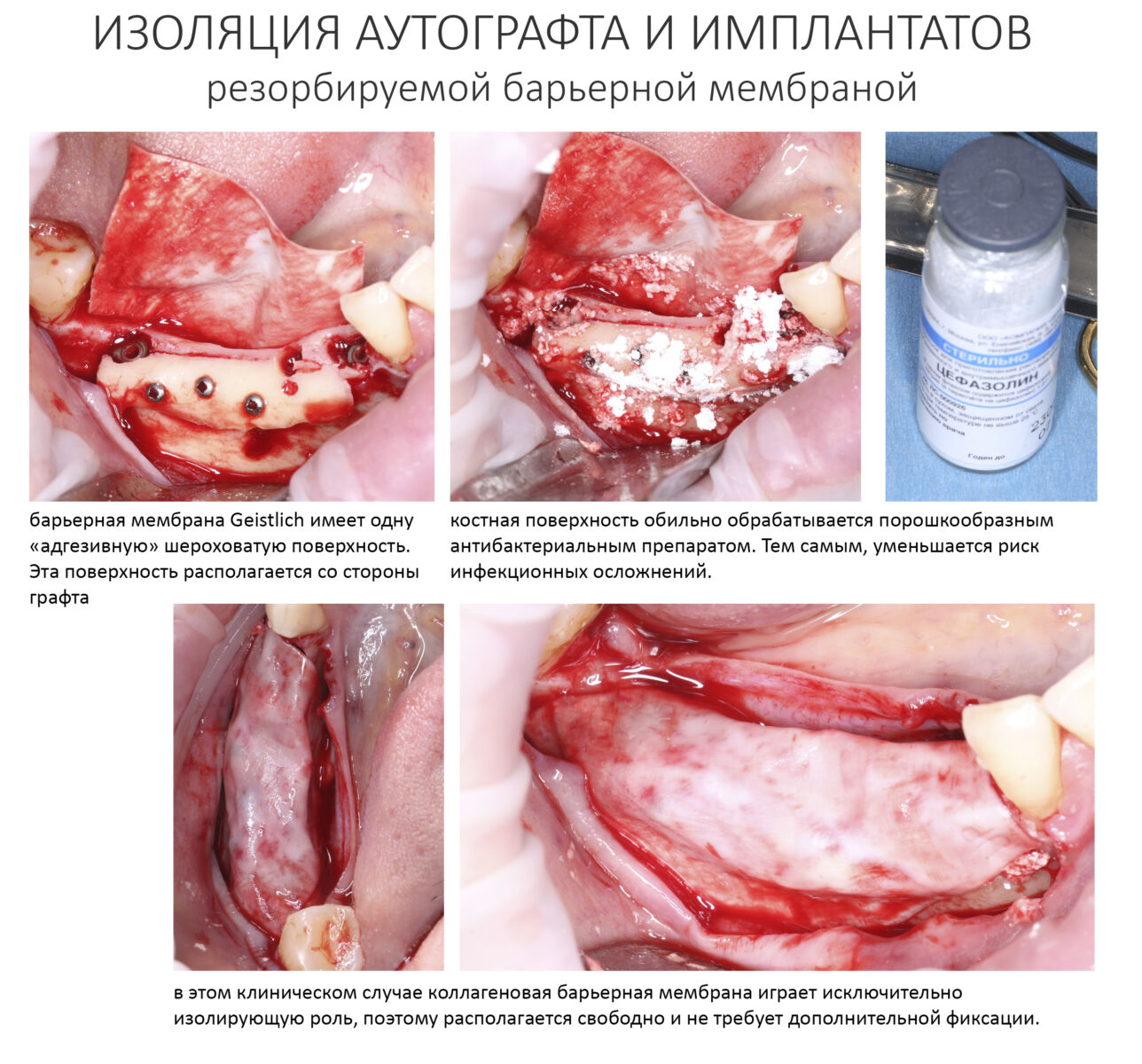 На этом этапе есть несколько нюансов, о которых я хочу рассказать отдельно.
На этом этапе есть несколько нюансов, о которых я хочу рассказать отдельно.
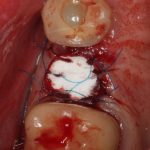
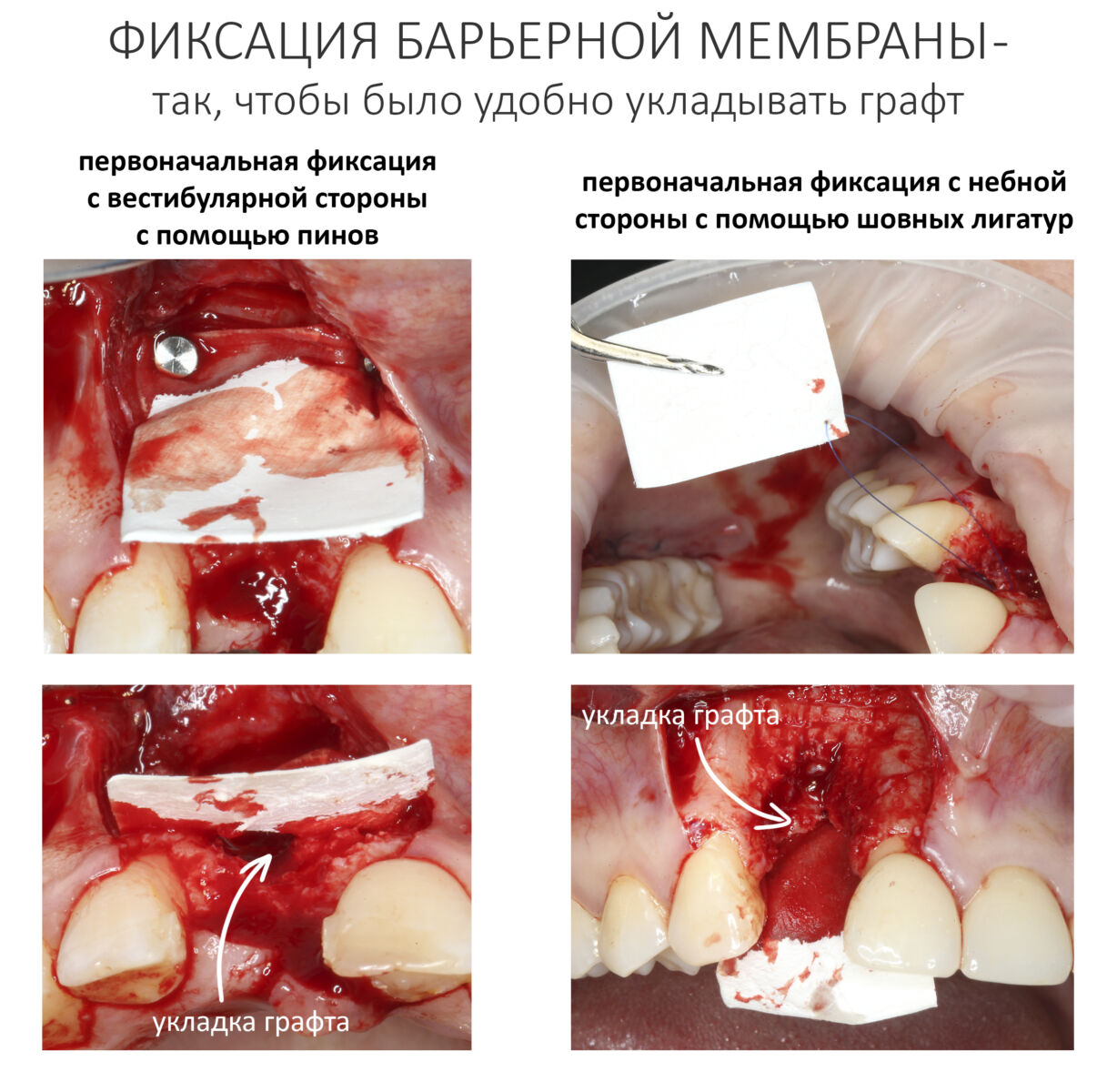
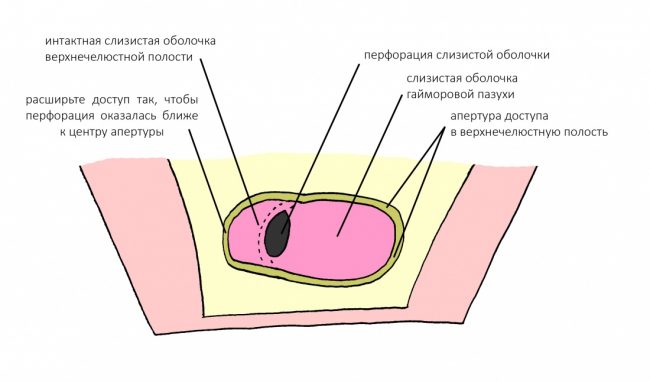
— я использовал барьерную мембрану Geistlich Bio-Gide, которая имеет две разные поверхности: с одной стороны она рыхлая «адгезивная», с другой — гладкая и прочная. Как укладывать — на результат не влияет, но в плане удобства рыхлую поверхность мы «приклеиваем» к тому, на чем требуется барьерную мембрану удержать. В данном случае хотелось бы удержать её на костной поверхности — следовательно, мы укладываем её рыхлой поверхностью к кости.
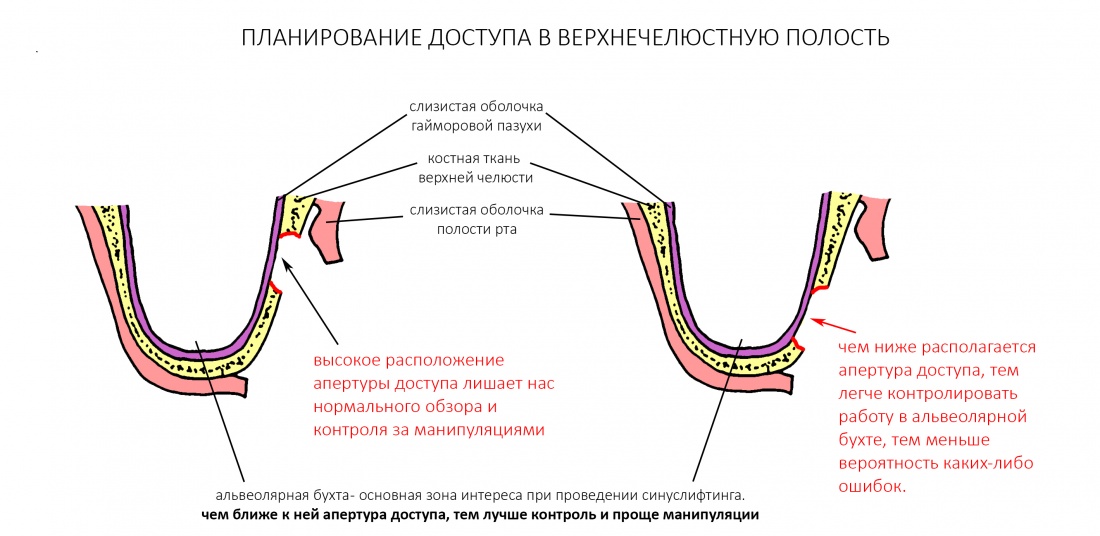
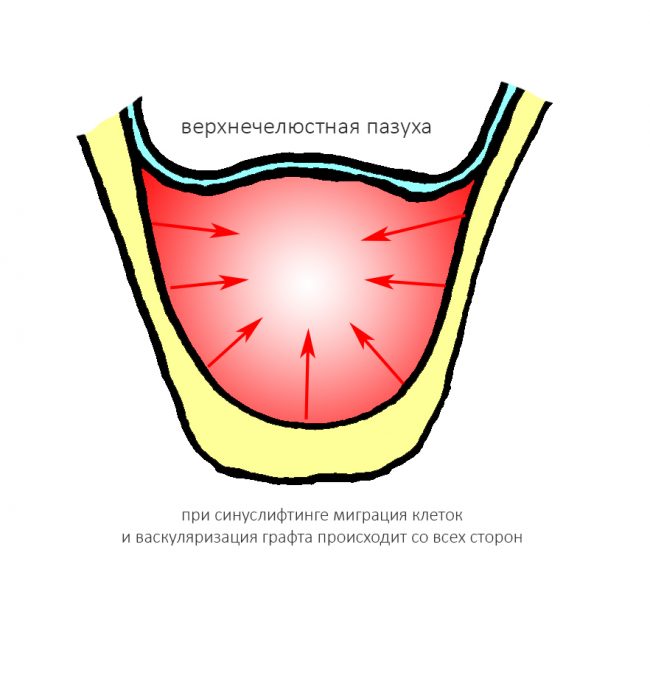
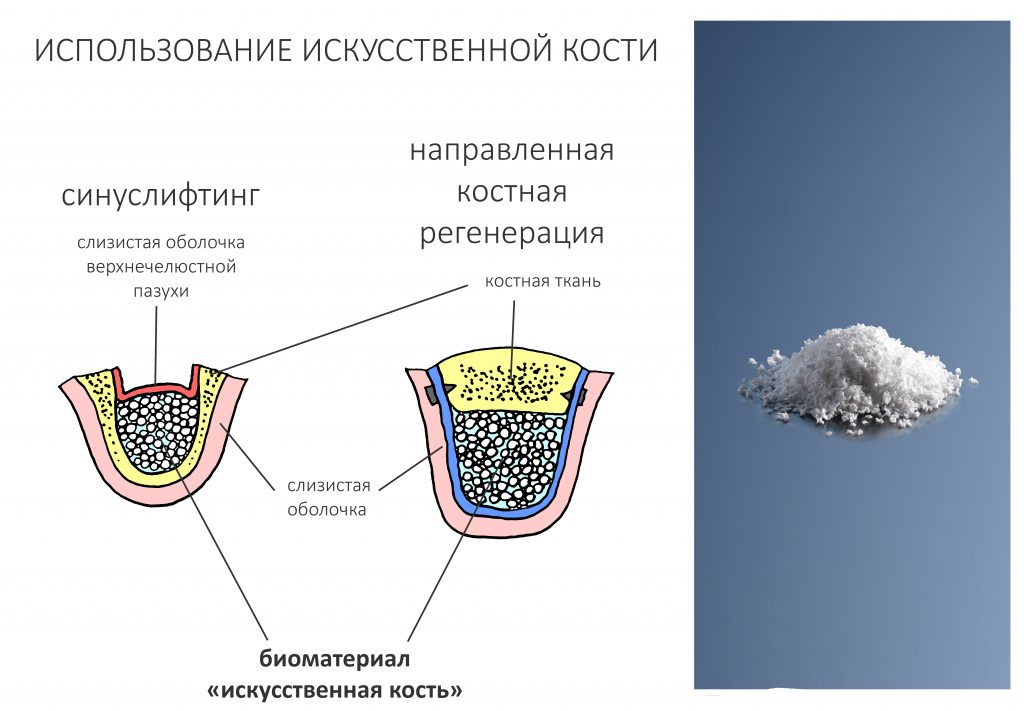
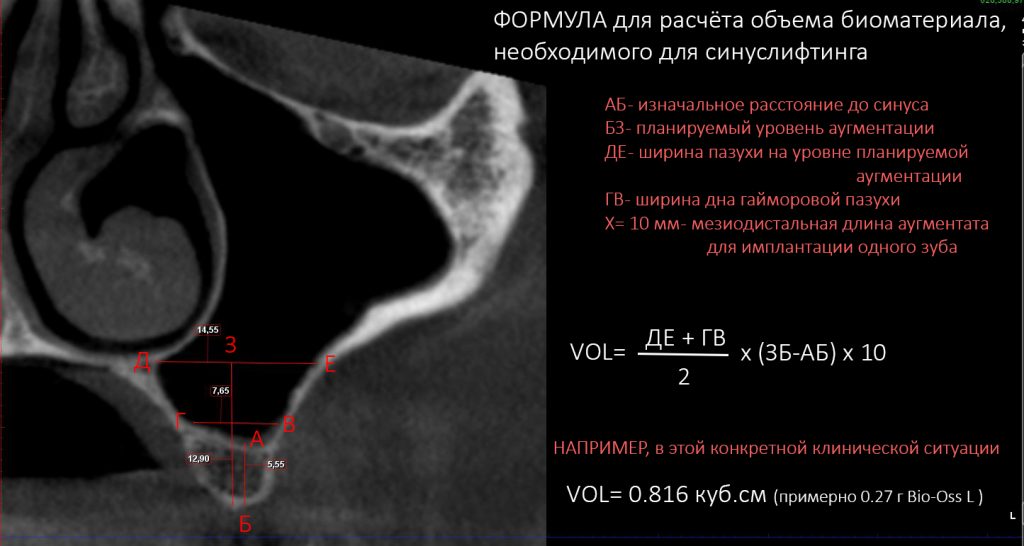
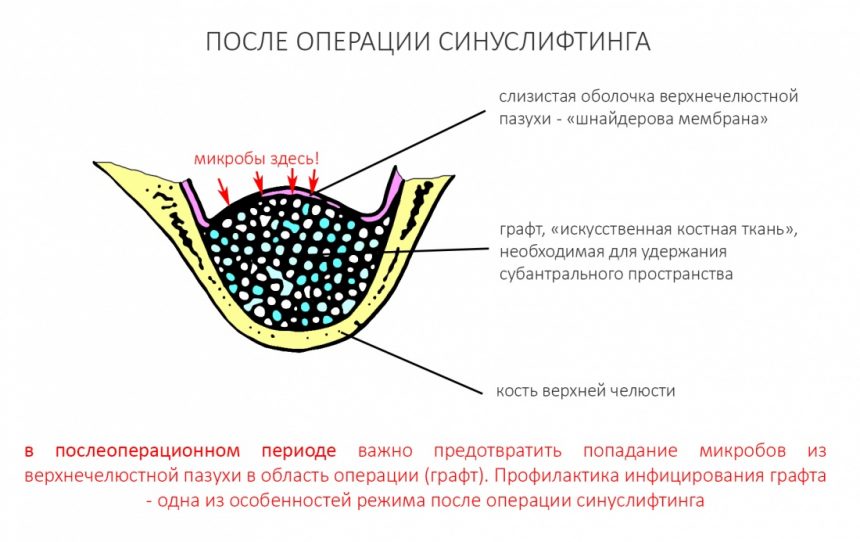
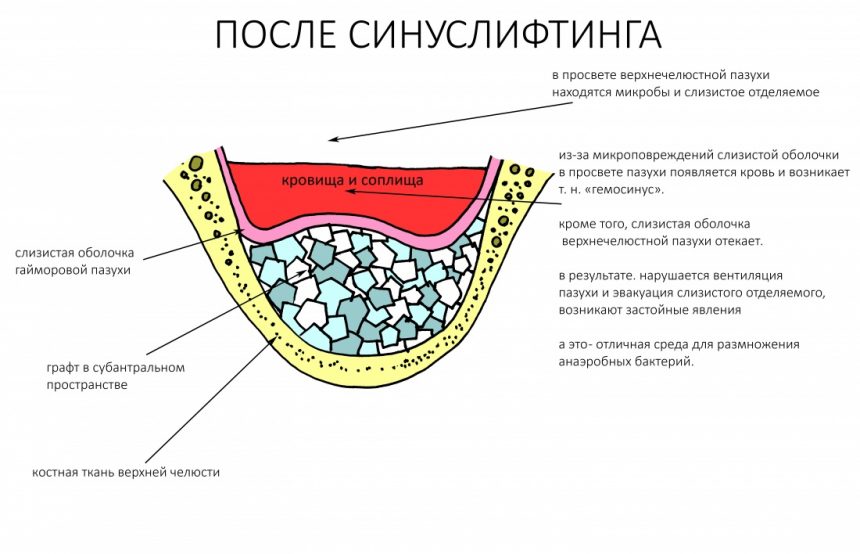
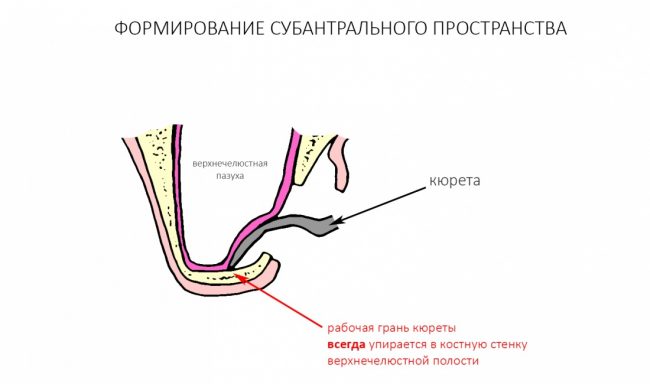
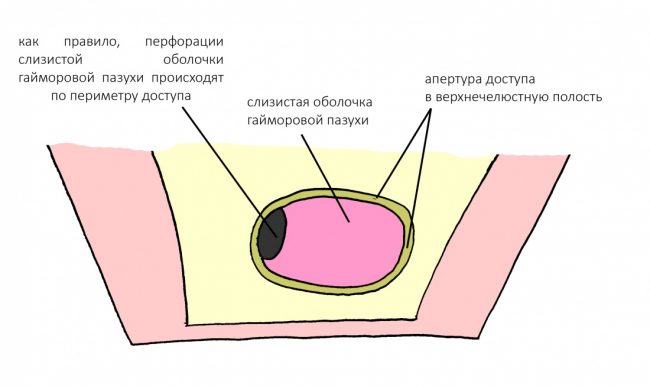
Ремарка: примечательно, что во время синуслифтинга ситуация иная - там требуется удержать барьерную мембрану на слизистой оболочке верхнечелюстной пазухи. Следовательно, рыхлая поверхность - на стороне шнайдеровой мембраны.
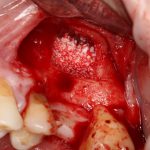
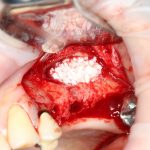
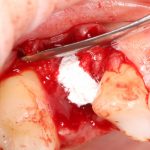
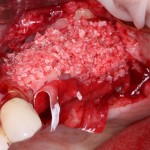
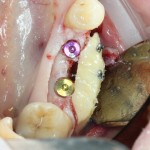
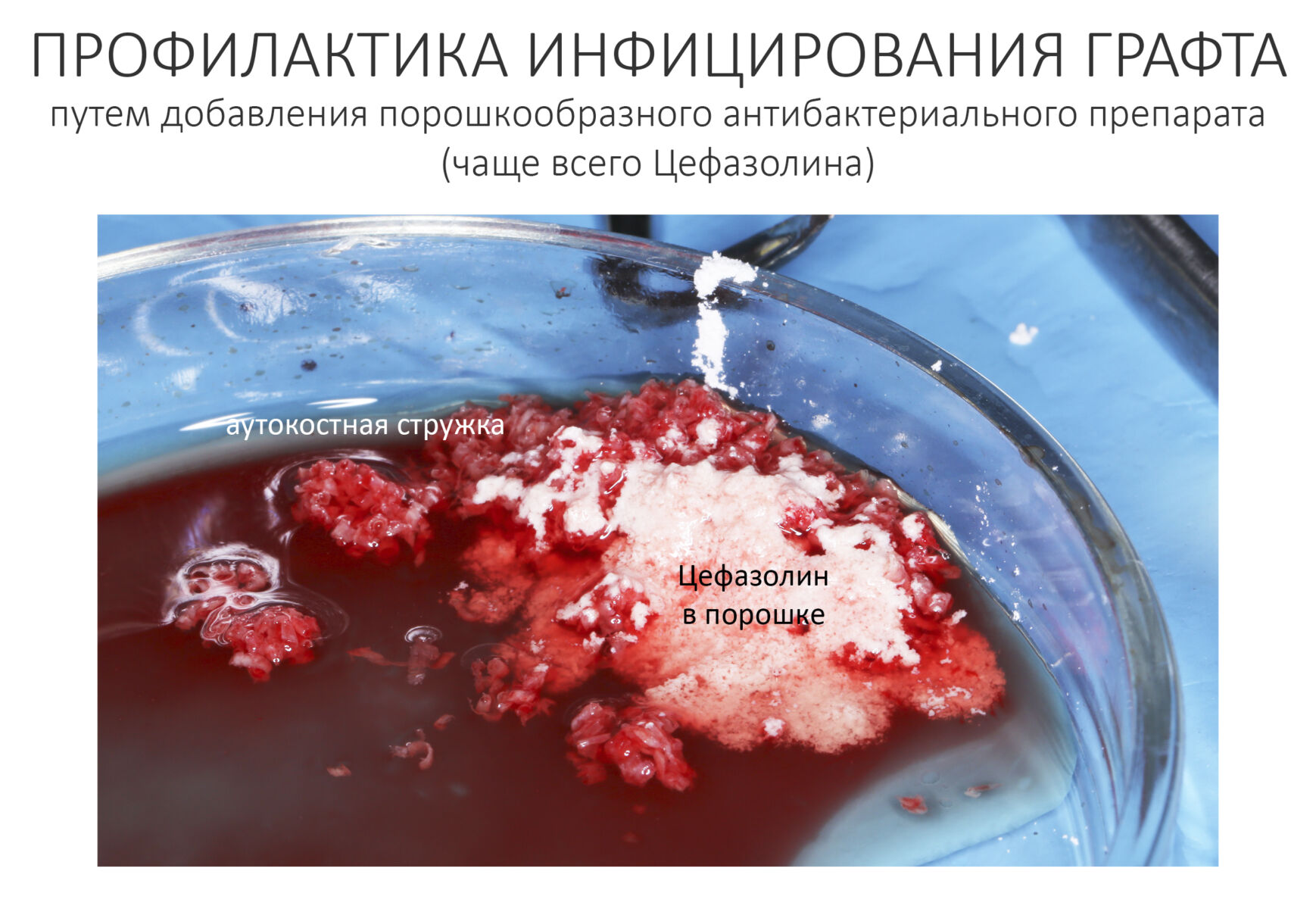
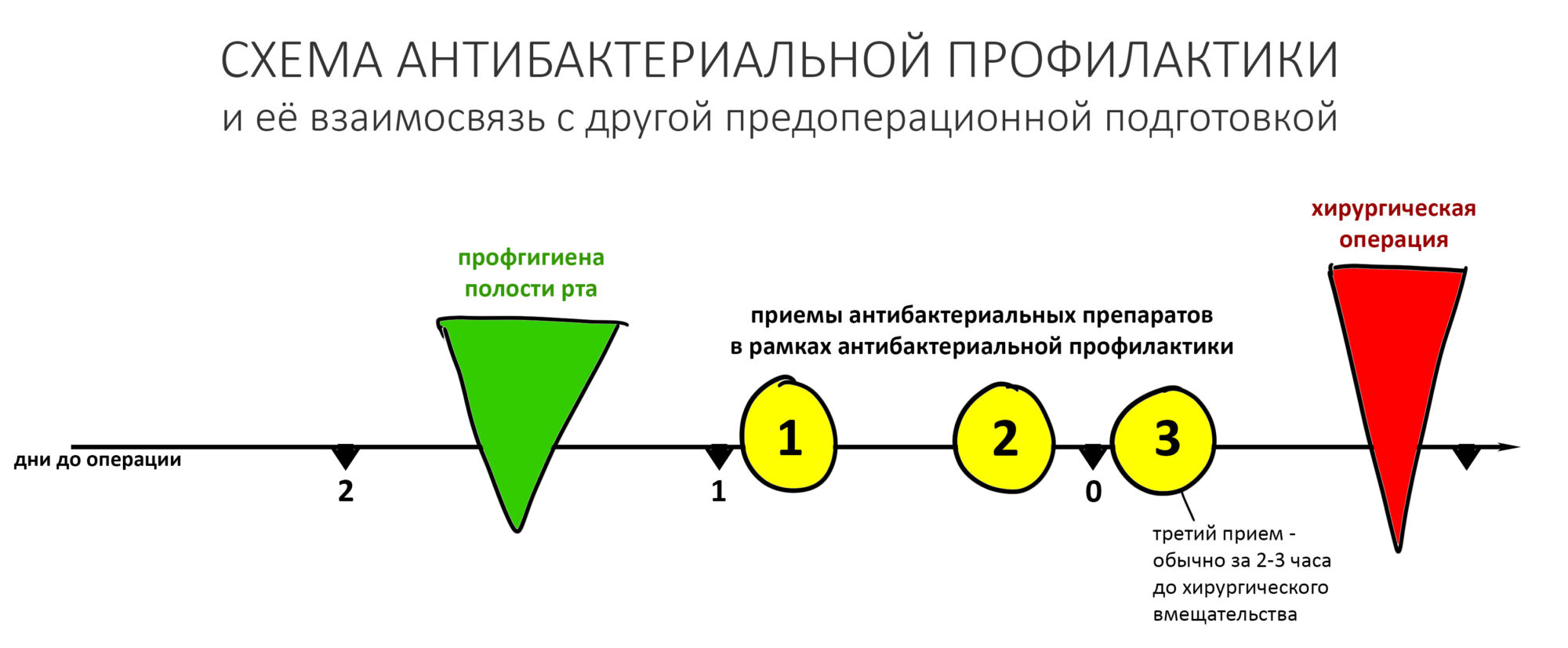
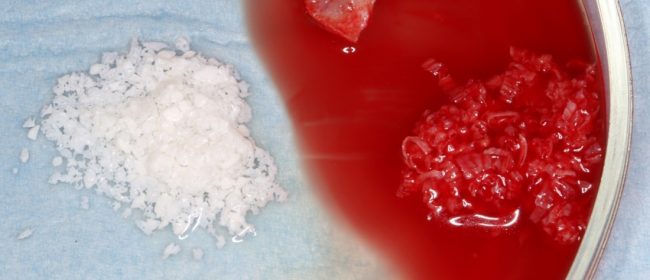
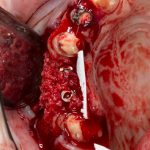
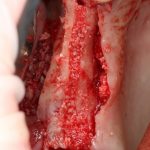
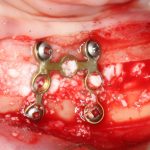
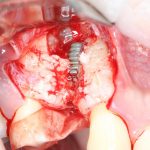
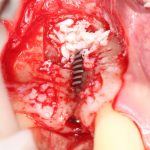
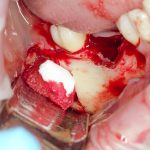
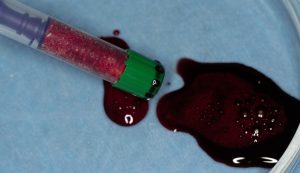
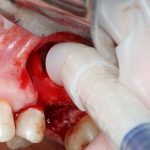
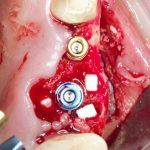
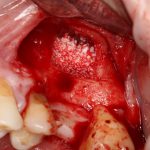
— много лет мы используем антибиотики для интраоперационной профилактики инфекционно-воспалительных осложнений. Уже в то время мы пришли к выводу, что удобнее всего — порошки антибактериальных препаратов для приготовления раствором: дешевые, стерильные, в удобной упаковке. Прямо в виде порошка их можно добавлять в графт, растворы для ирригации, либо использовать так, как показано на фото. Еще мы используем порошок антибиотика для изготовления пасты, которой обрабатываем имплантаты в процессе ревизии или при лечении периимплантита. Это удобнее и эффективнее, чем интраоперационное использование жидких форм антибактериальных препаратов.
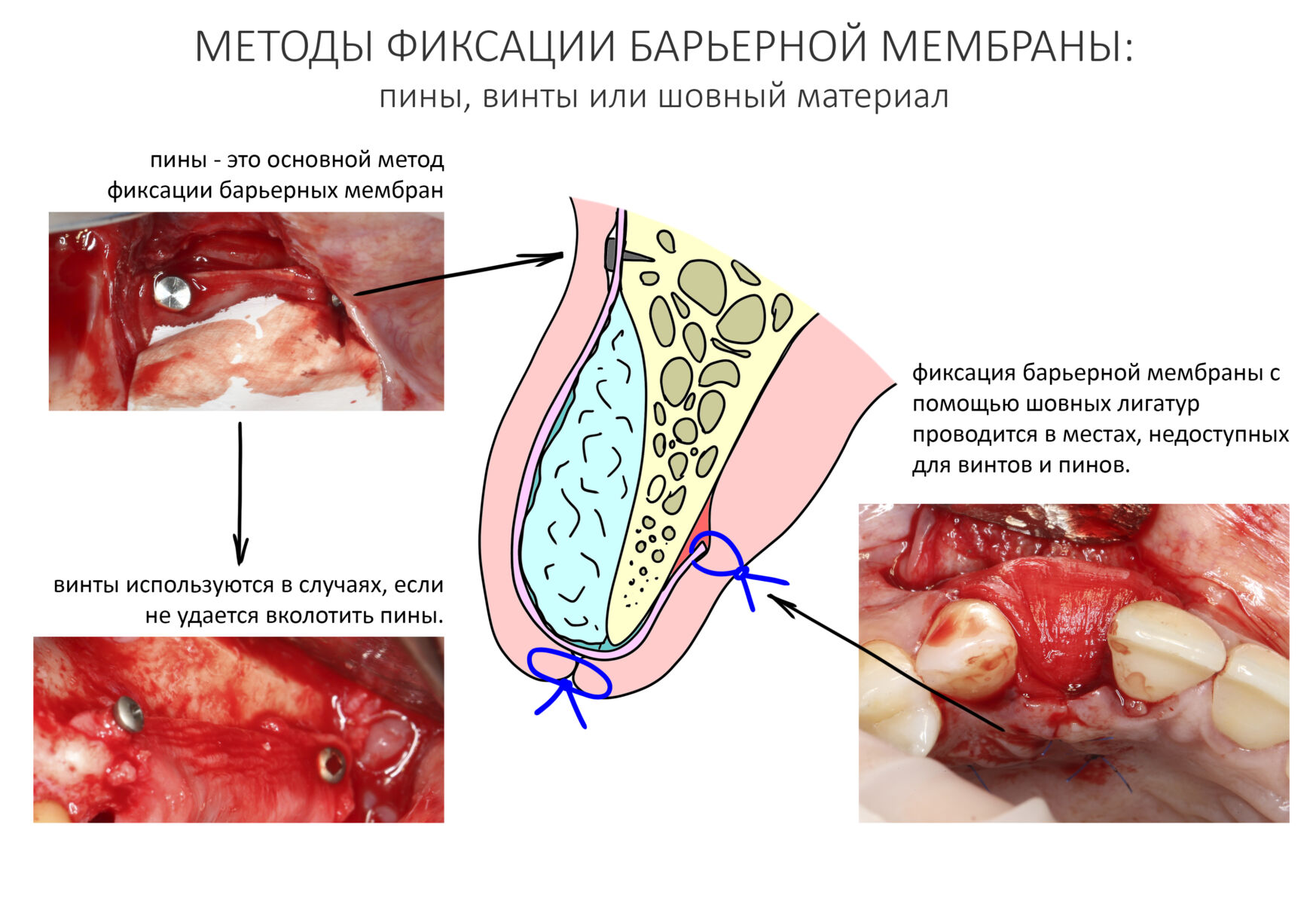
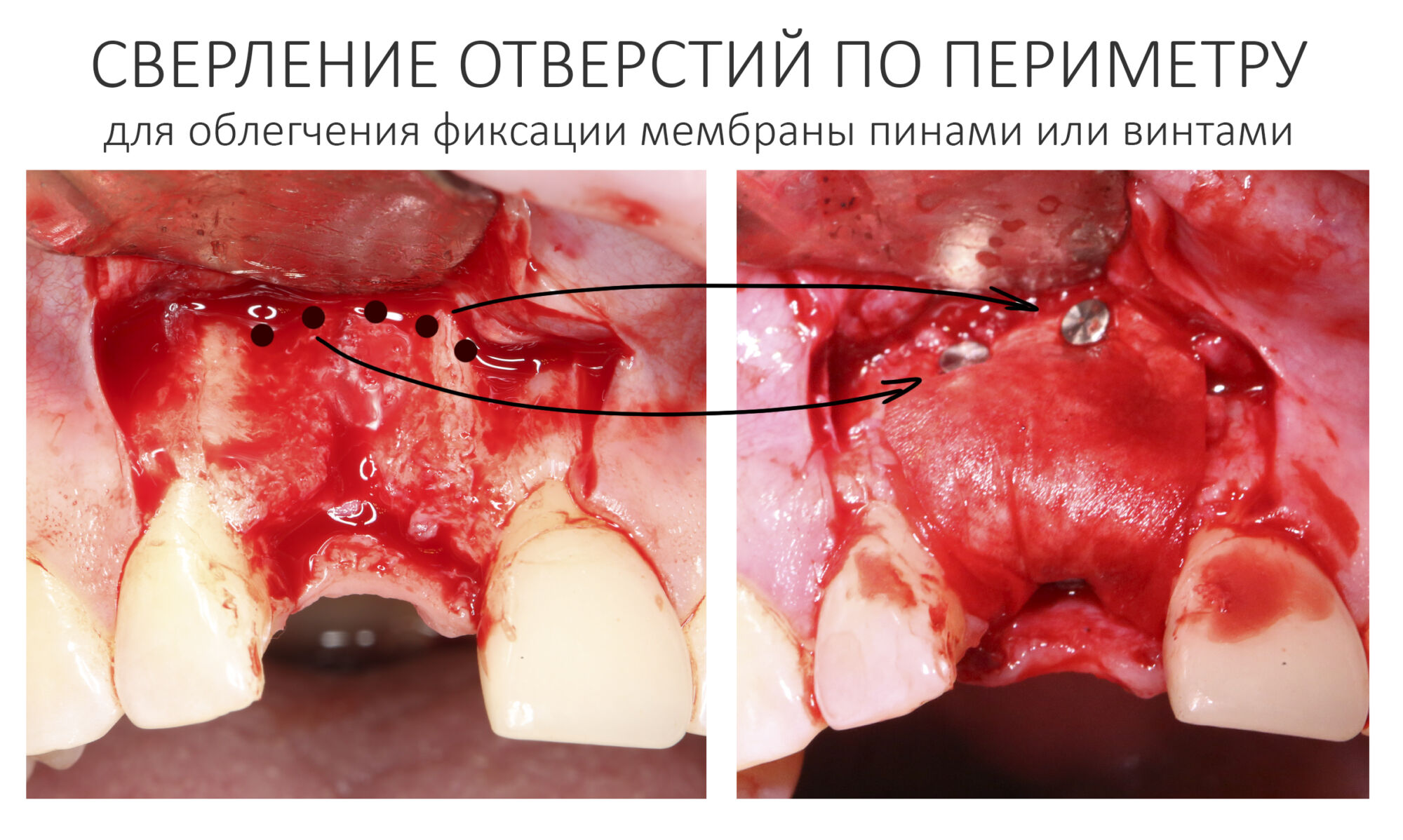
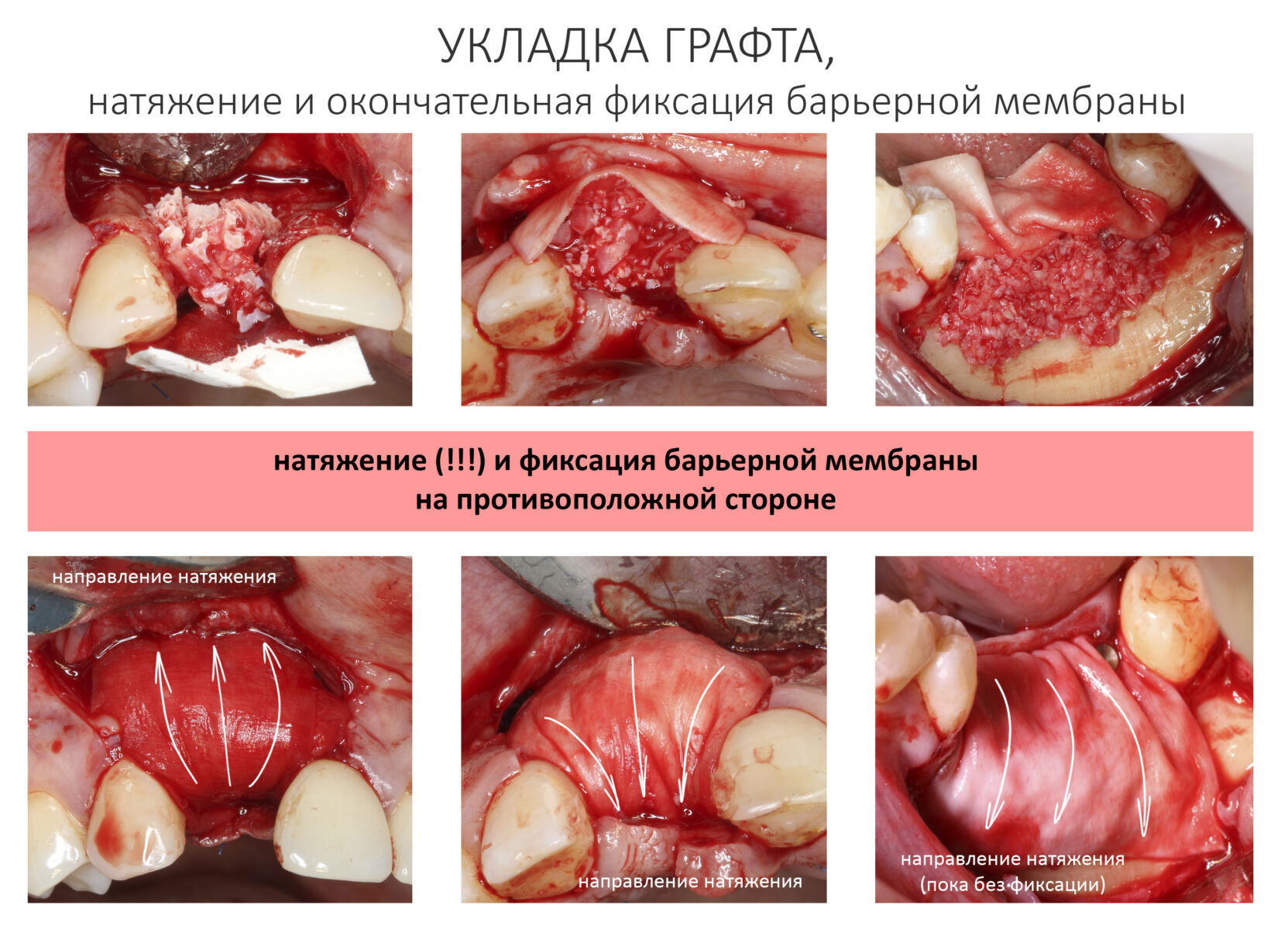
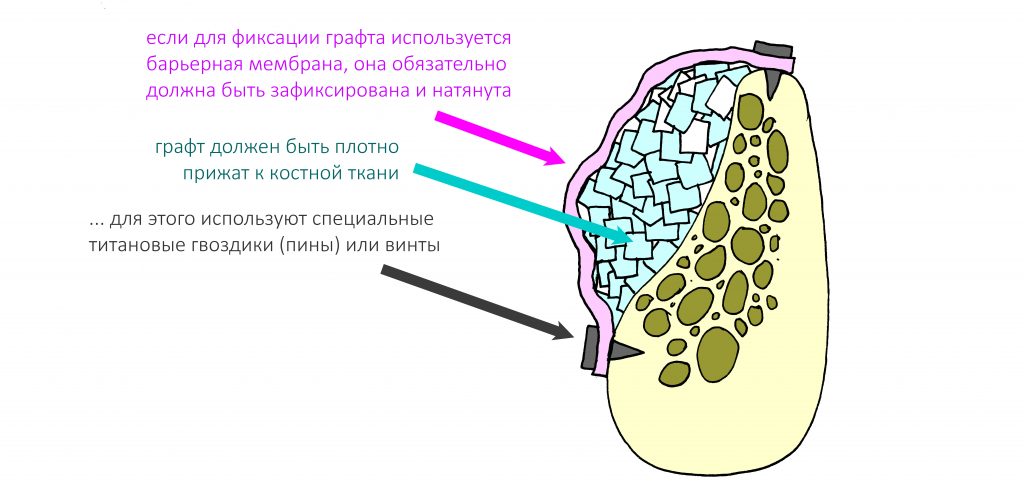
— ты знаешь, что барьерная мембрана может выполнять две функции, каркасную и изолирующую. Первая функция требует обязательной фиксации и натяжения, вторая — нет. В нашем случае «каркасом» регенерата является костный блок, а барьерная мембрана нужна только для изоляции. Поэтому она не требует натяжения и фиксации пинами.
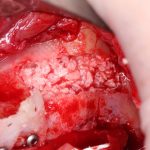
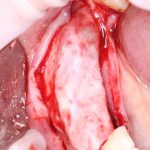
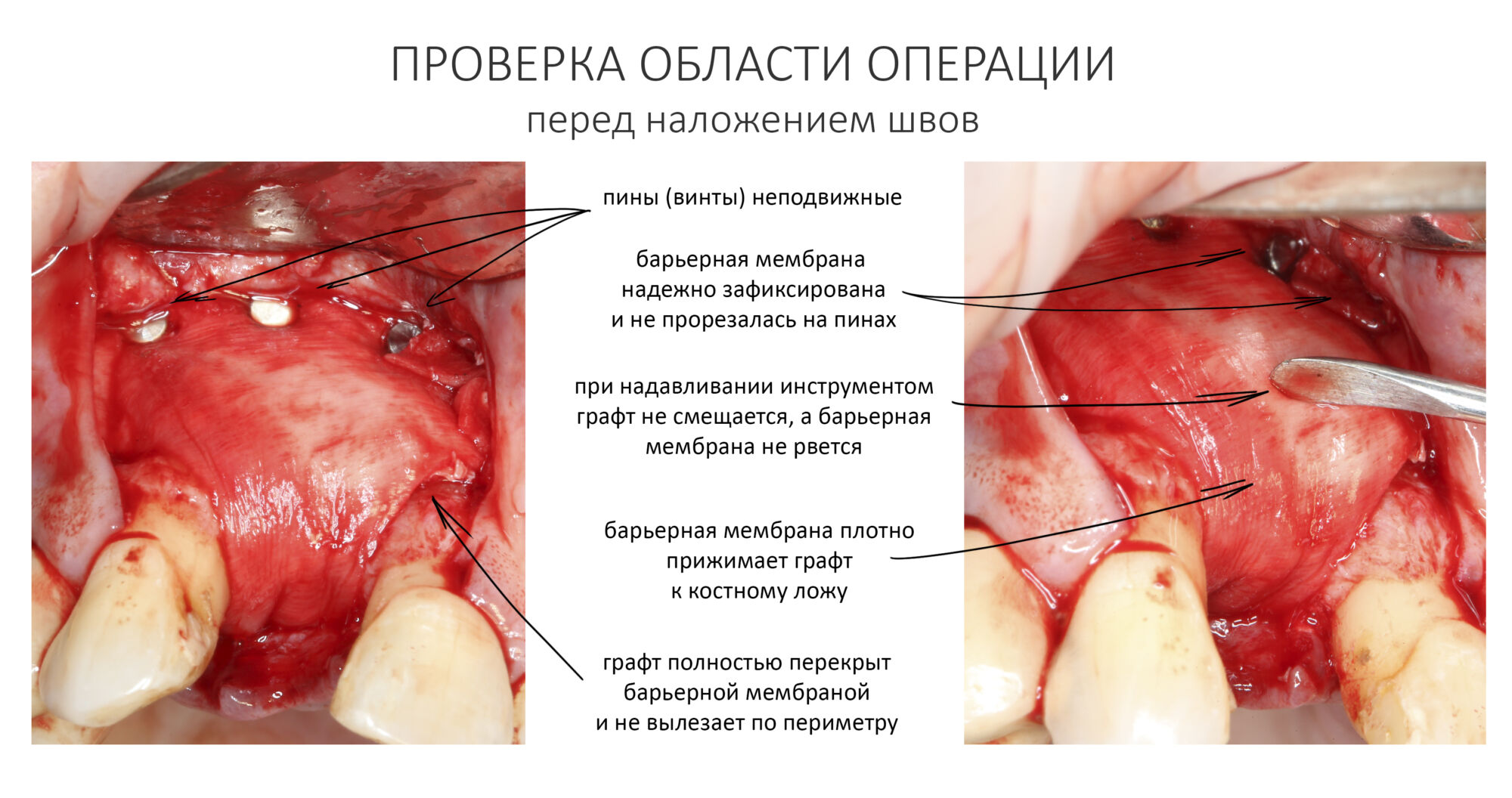
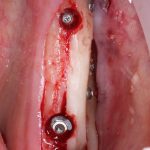
После я внимательно проверил, что костный блок и имплантаты полностью перекрыты. Теперь рану можно ушивать.
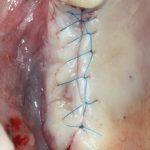
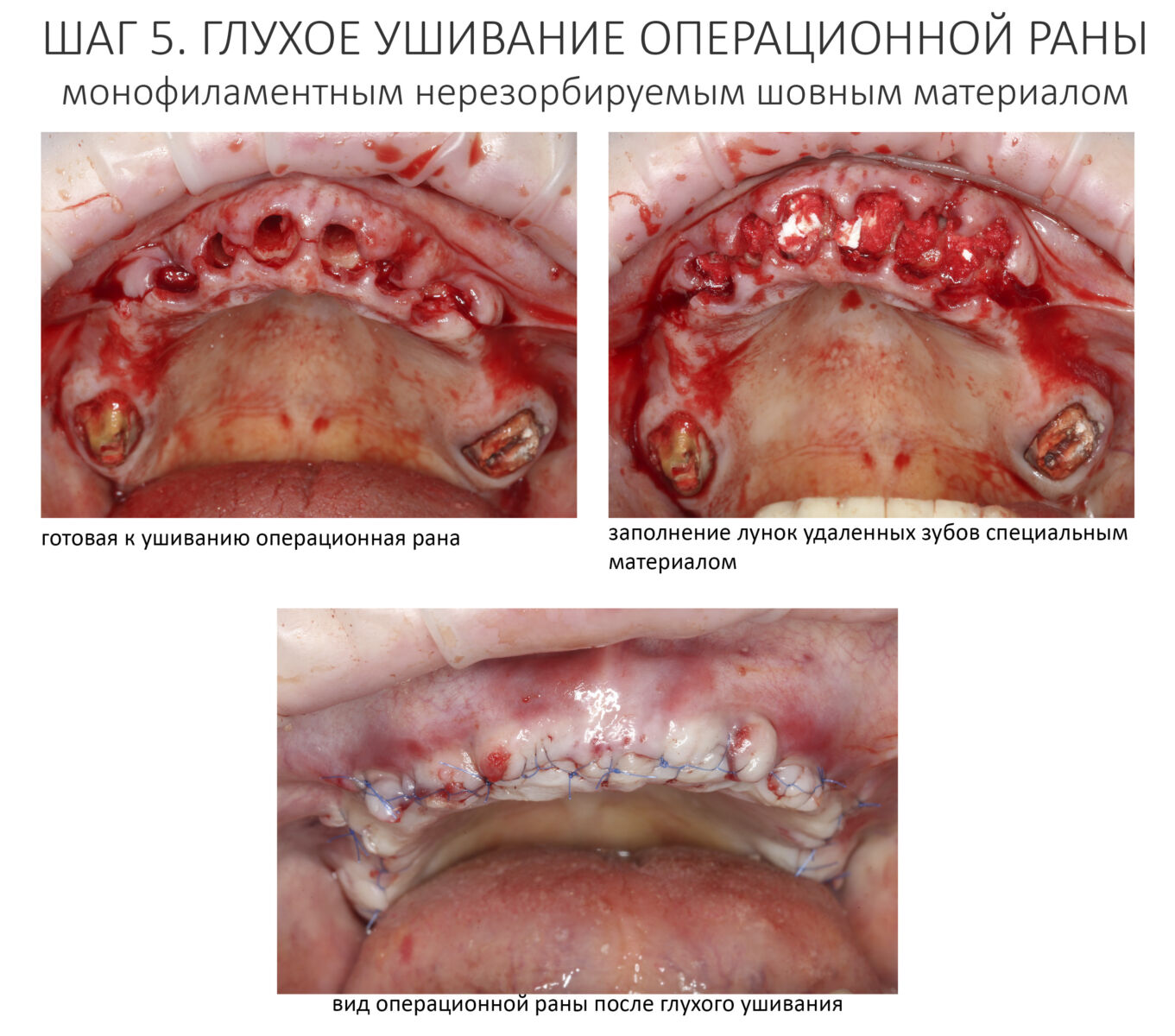
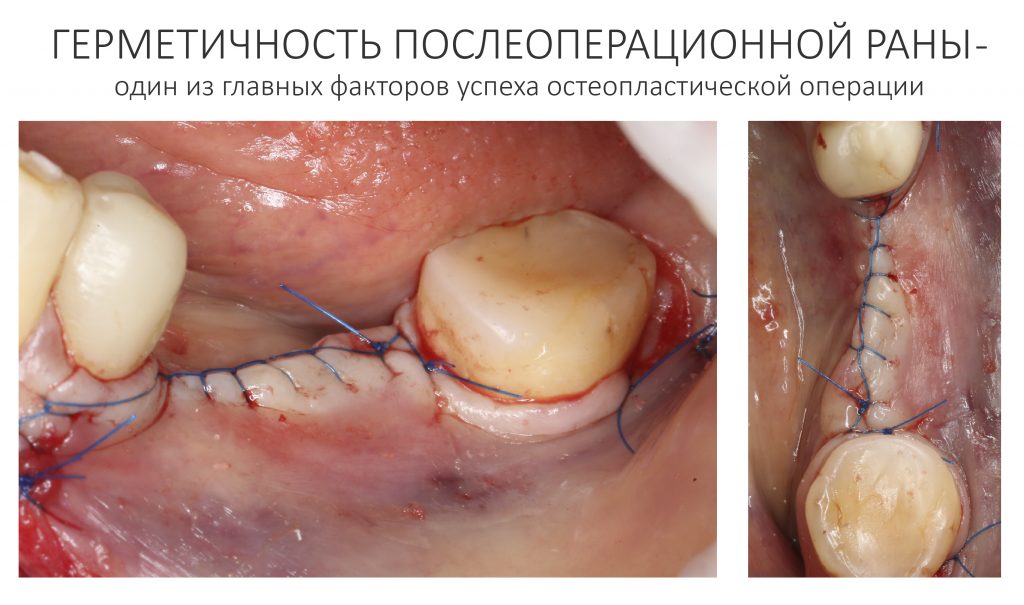
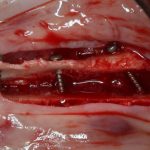
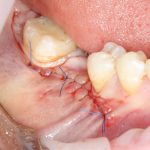
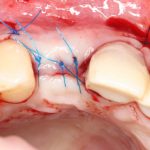
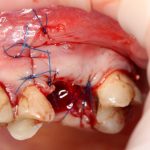
Наложение швов.
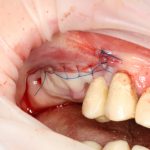
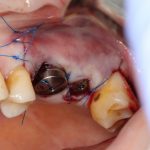
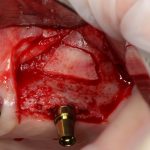
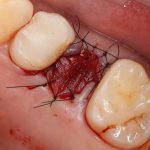
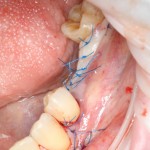
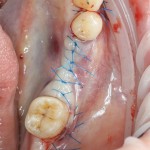
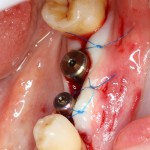
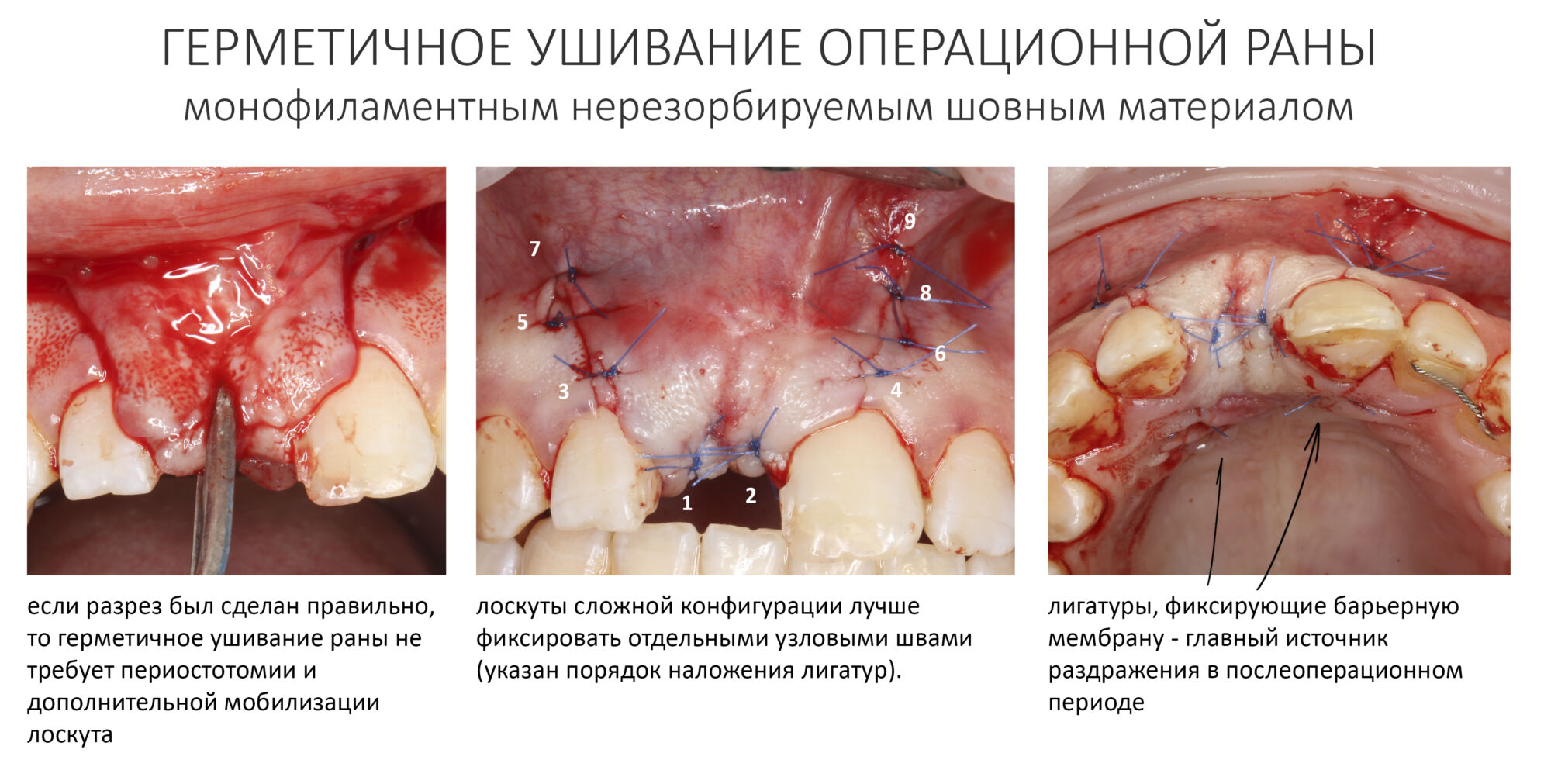
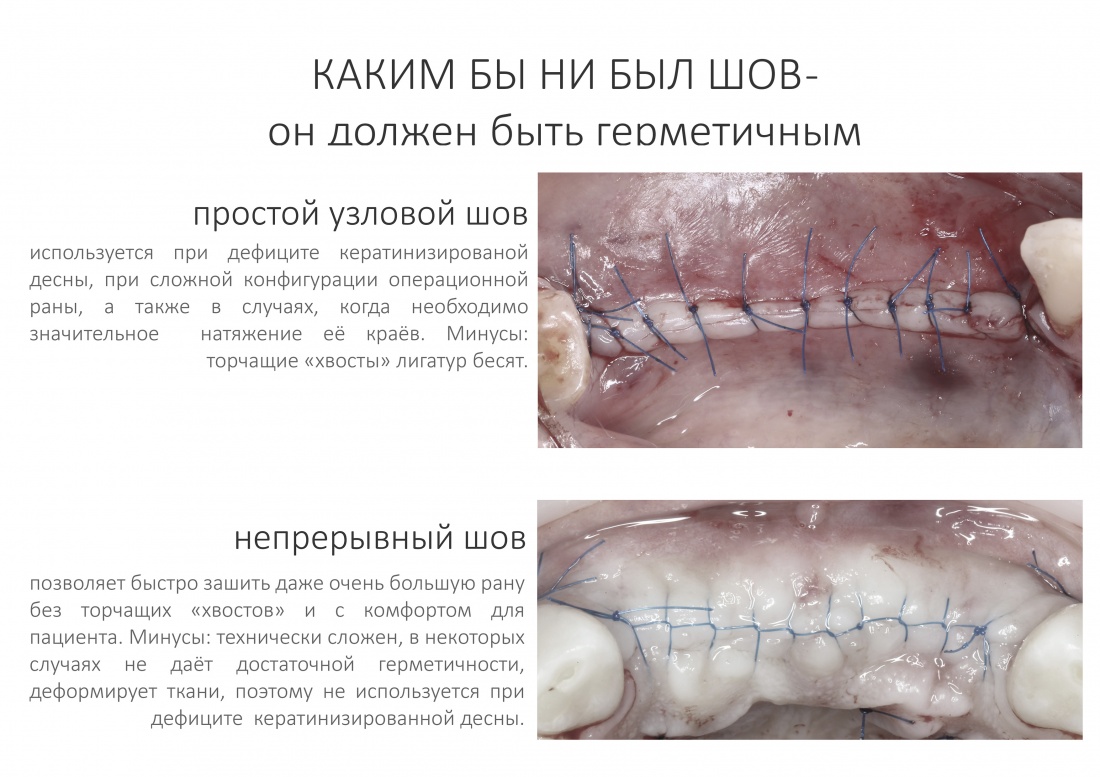
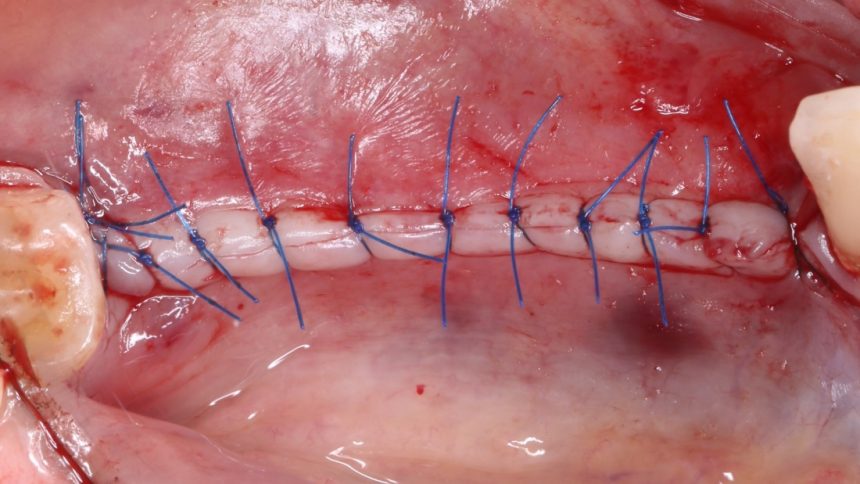
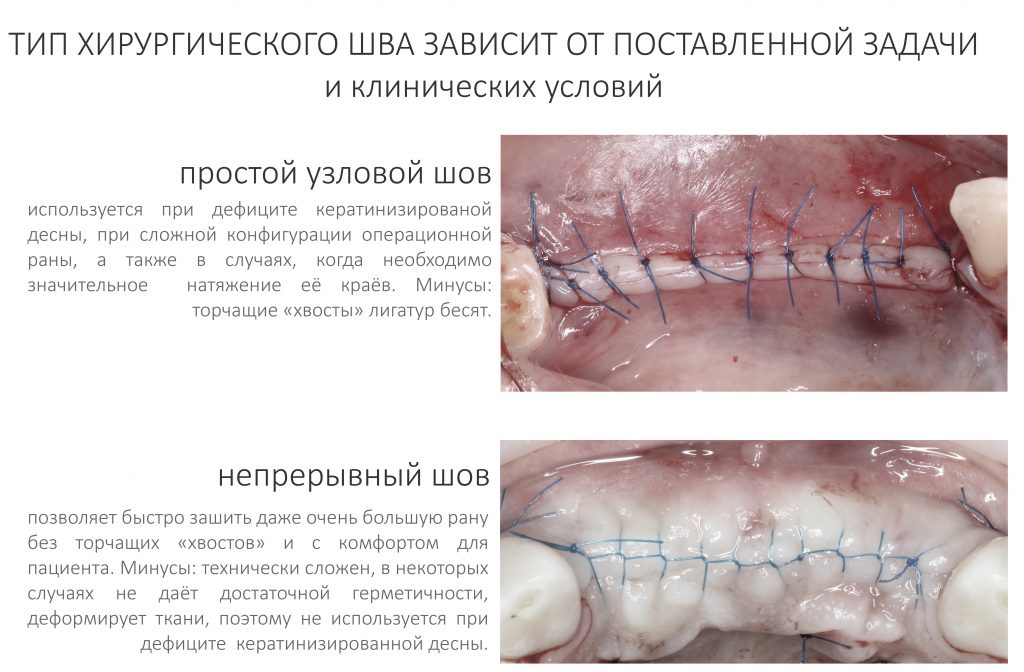
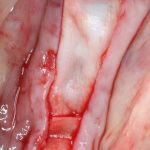
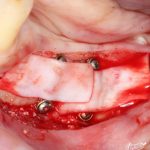
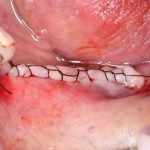
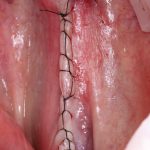
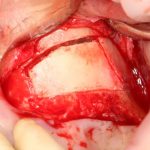
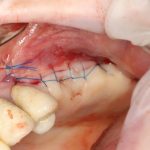
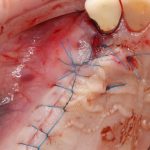
Если на этапе разреза и формирования раны всё сделано правильно, то наложение швов не вызывает особых трудностей. Периостотомия или послабляющие разрезы на периосте не требуются (ни практически никогда не требуются). А сами швы получаются аккуратными и герметичными:
 Обрати внимание, что все шовные лигатуры находятся в пределах кератинизированной десны. Это позволяет избежать деформации тканей и лишних рубцов. В наиболее уязвимых местах (около зубов) шовные лигатуры лучше продублировать.
Обрати внимание, что все шовные лигатуры находятся в пределах кератинизированной десны. Это позволяет избежать деформации тканей и лишних рубцов. В наиболее уязвимых местах (около зубов) шовные лигатуры лучше продублировать.
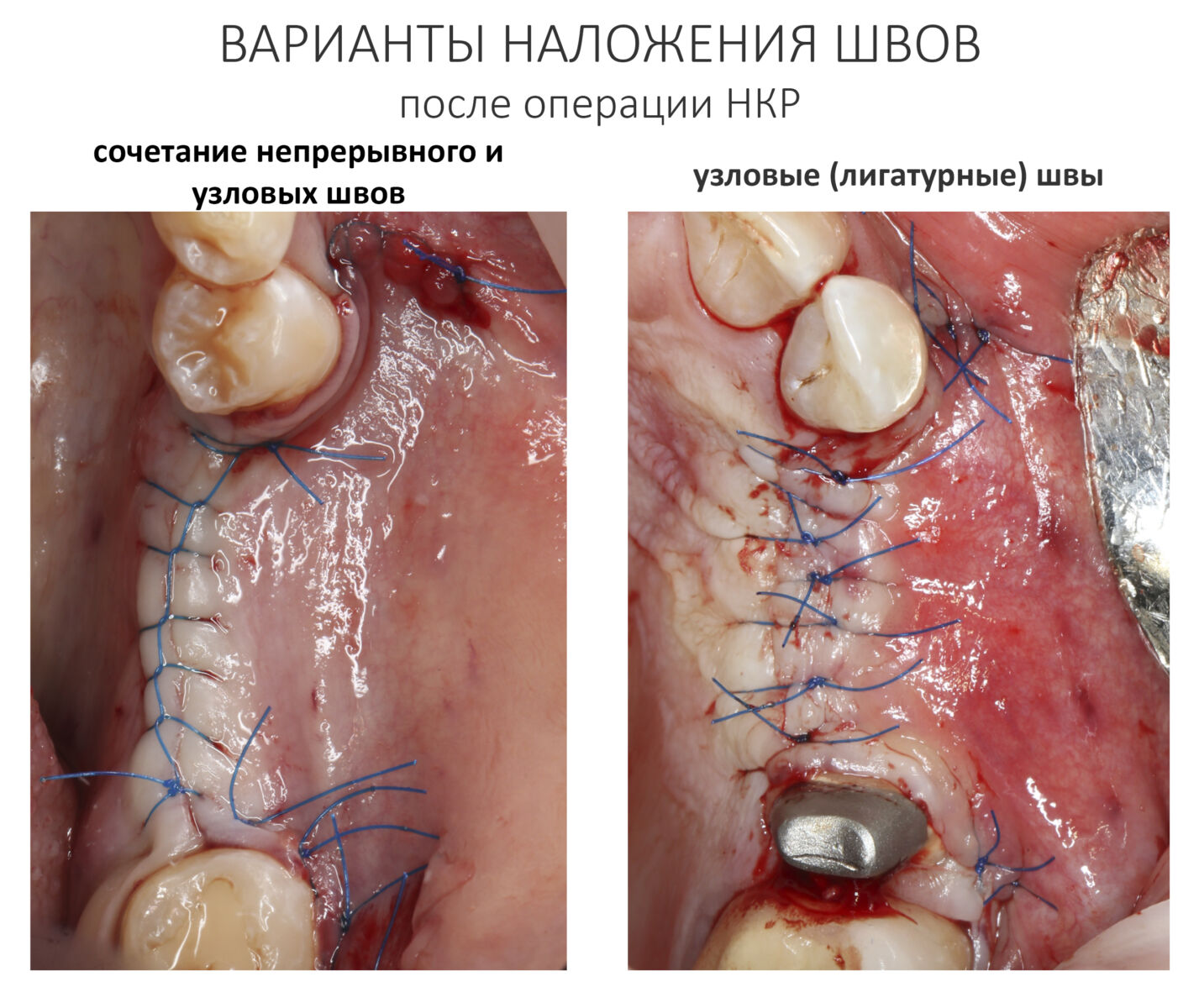
Если бы мне пришлось делать это сейчас, то я бы использовал непрерывный «матрацный» шов. Он удобнее, быстрее в наложении и комфортнее для пациента. Минус — если распускается, то распускается весь. К тому же, его очень неудобно снимать.
Несмотря на то, что уже тогда мы широко использовали непрерывные швы в подобных случаях, здесь я, во-первых, зассал (может распуститься), во-вторых, снятие швов предполагалось в поликлинике по месту жительства пациентки, и мне не хотелось, чтобы там при снятии швов начудили. Как выяснится позже — зря беспокоился.
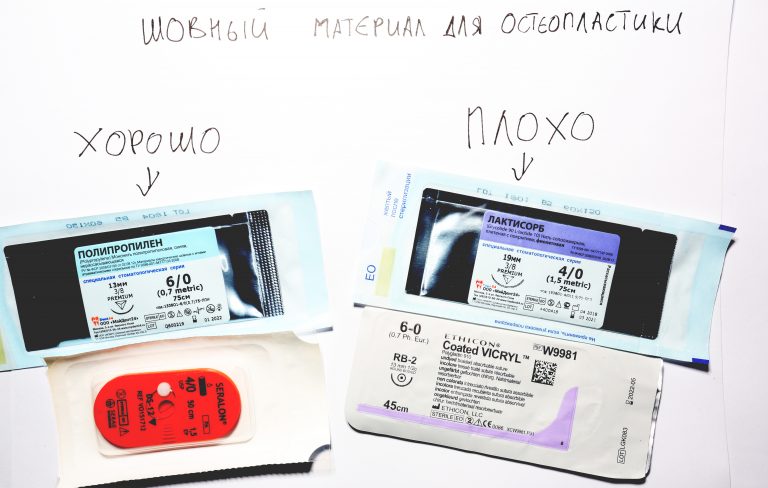
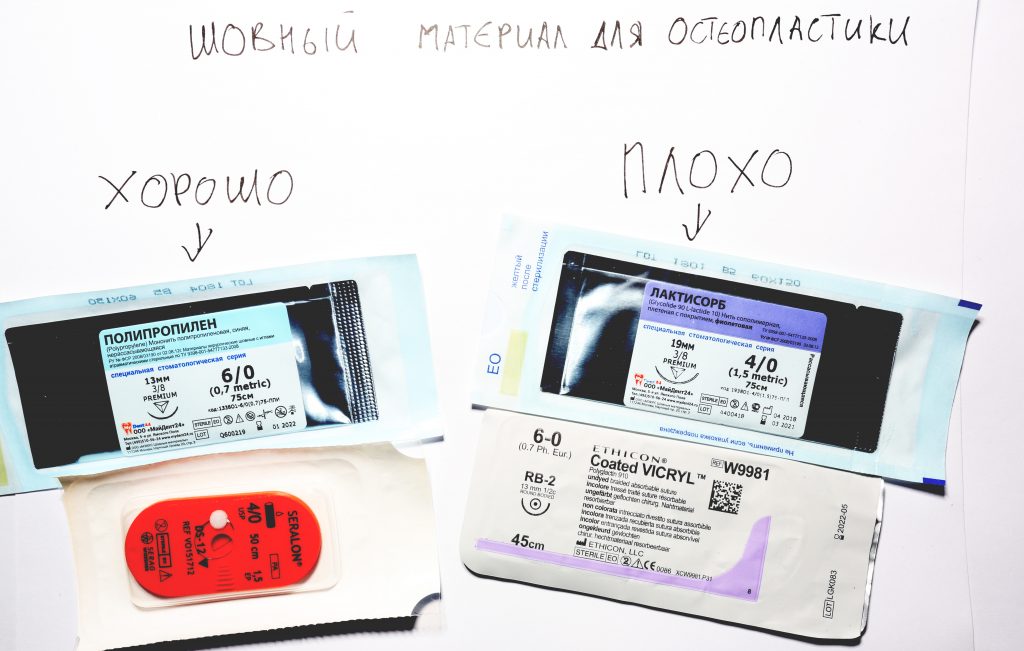
Неизменно одно — в таких операциях мы использовали и до сих пор используем нерезорбируемые монофиламентные шовные материалы, поскольку они наиболее гигиеничные. Чтобы острые концы нитей не беспокоили пациента, их можно оплавить нагретой гладилкой или гуттаперчевым плаггером.
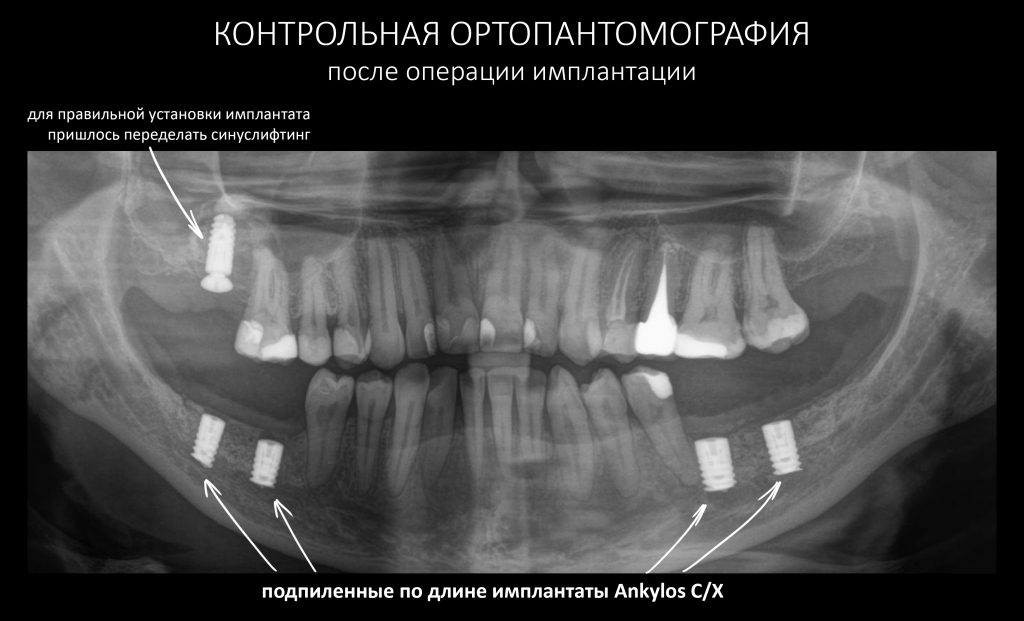
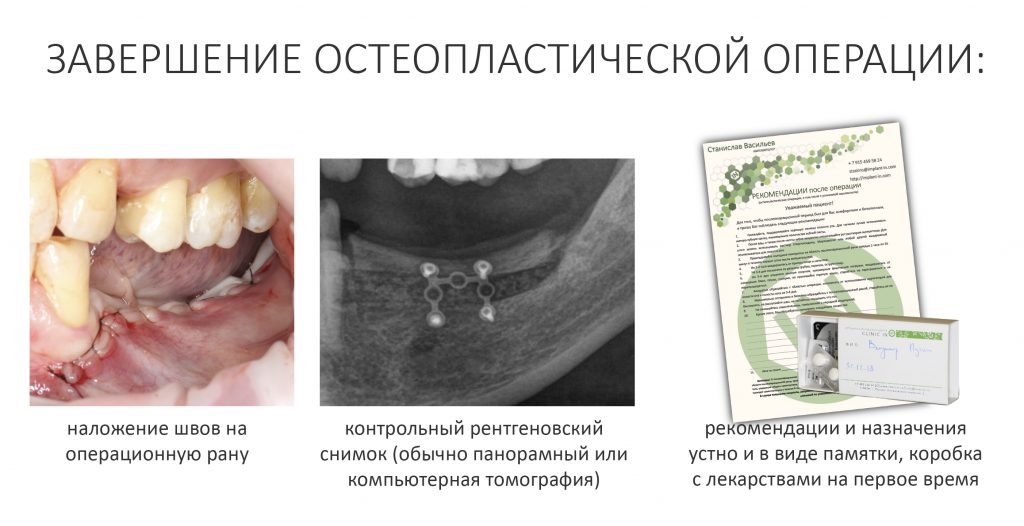
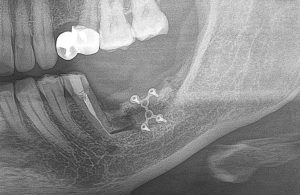
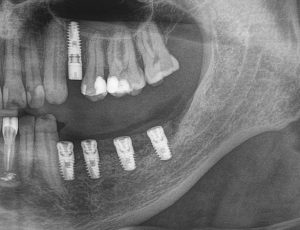
После операции:
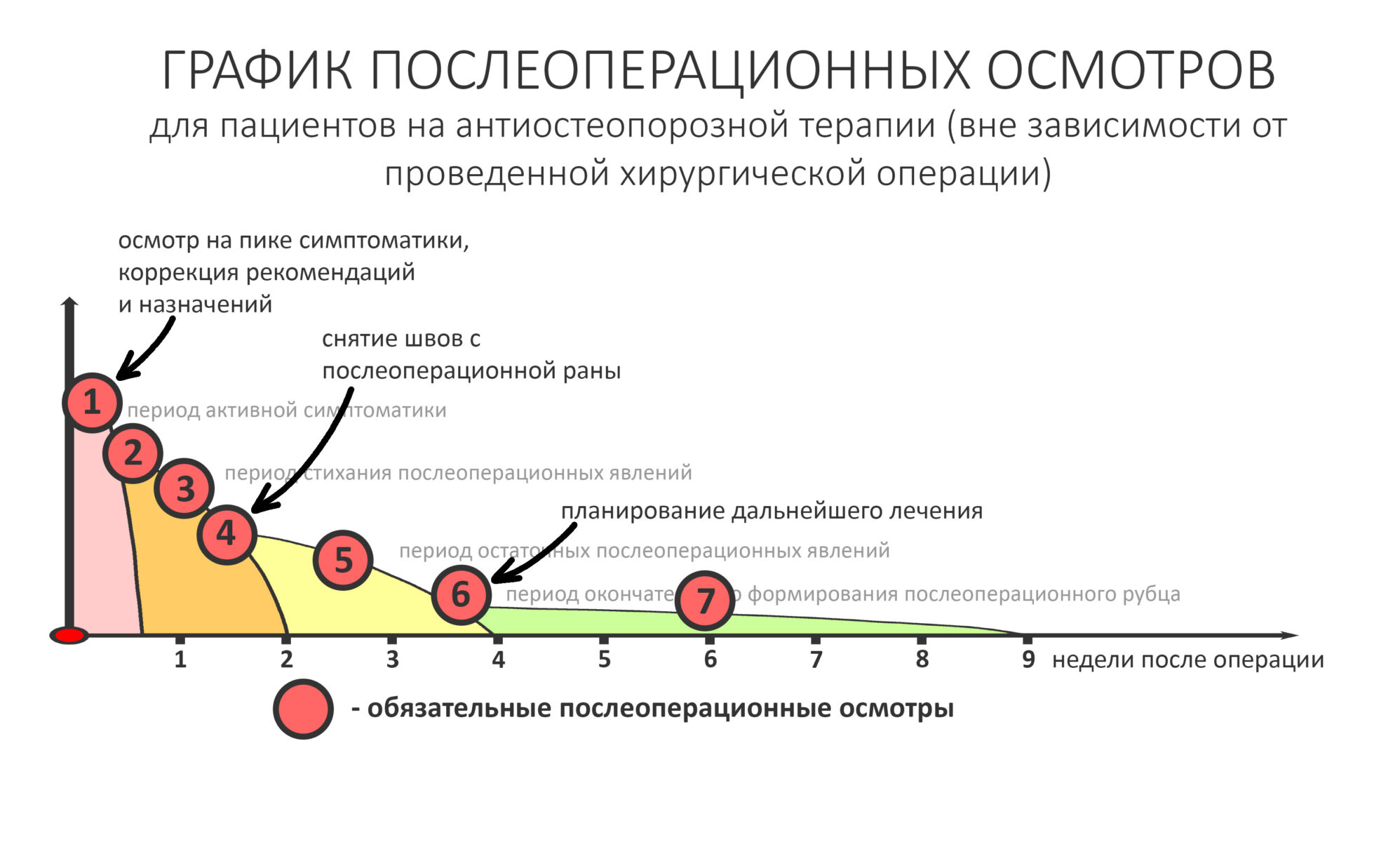
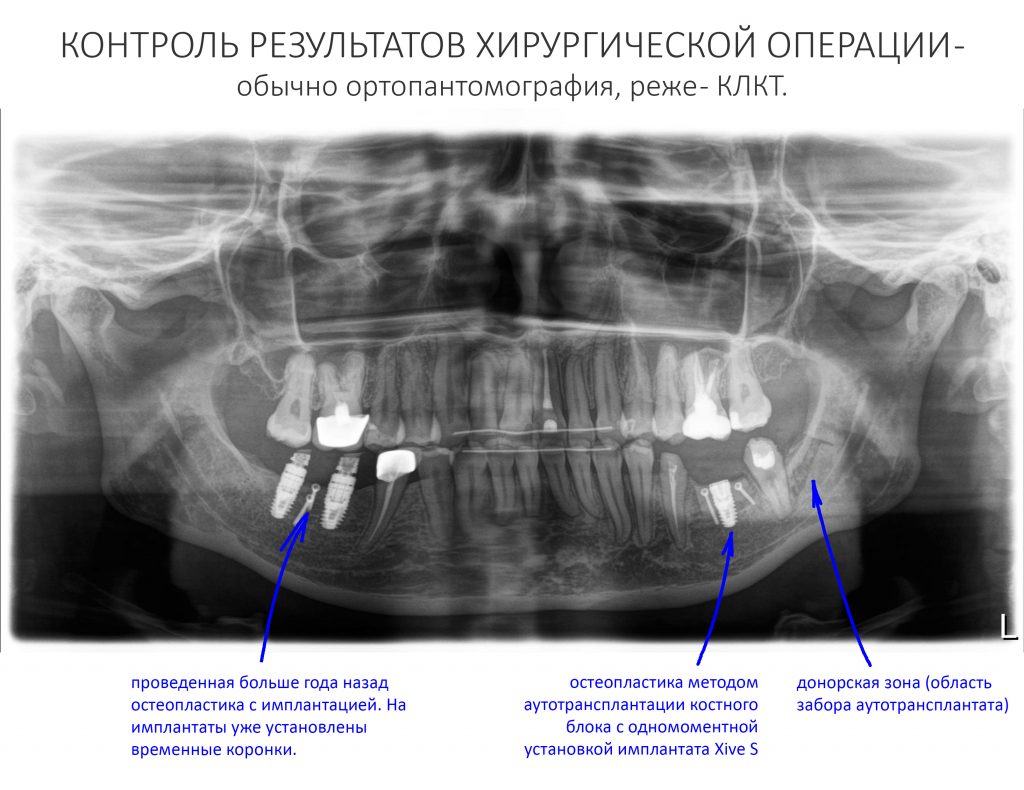
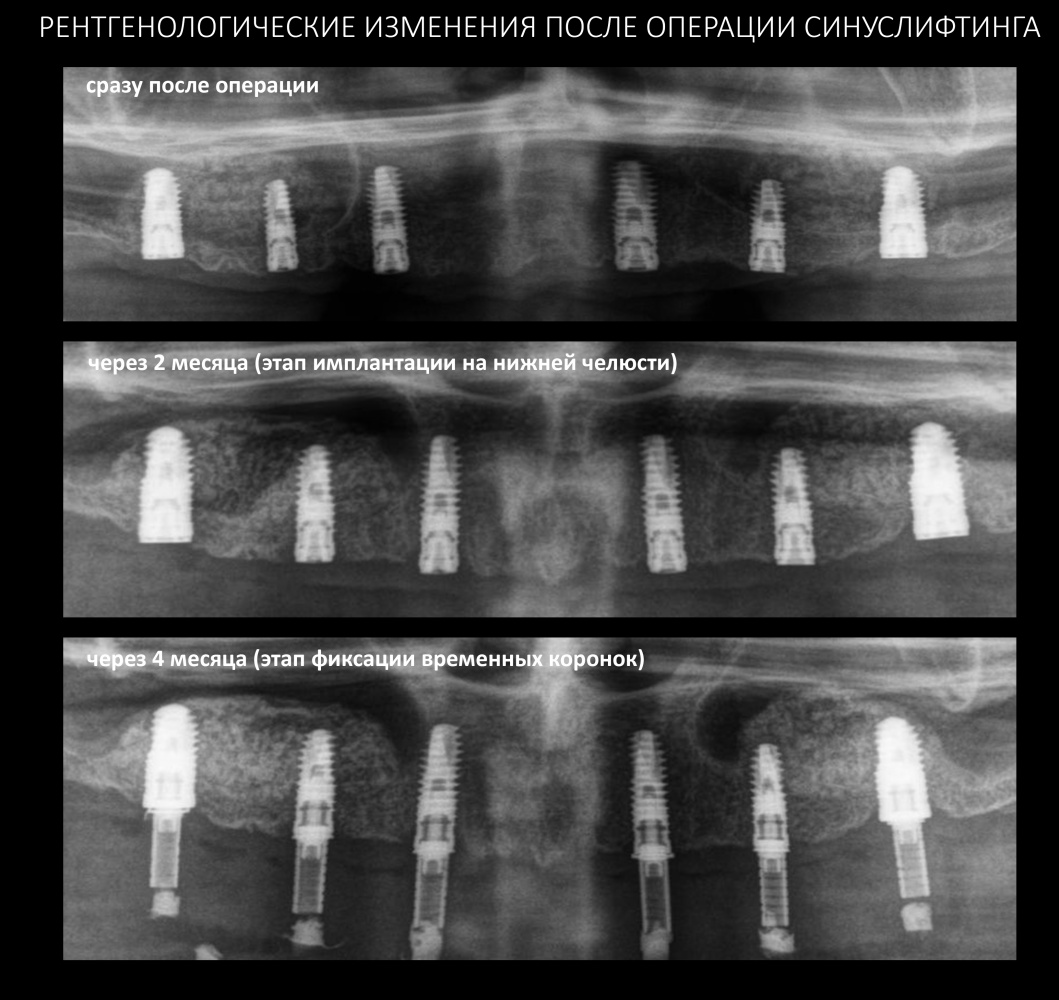
— контрольный снимок (раньше делали ОПТГ, сейчас — строго КЛКТ)
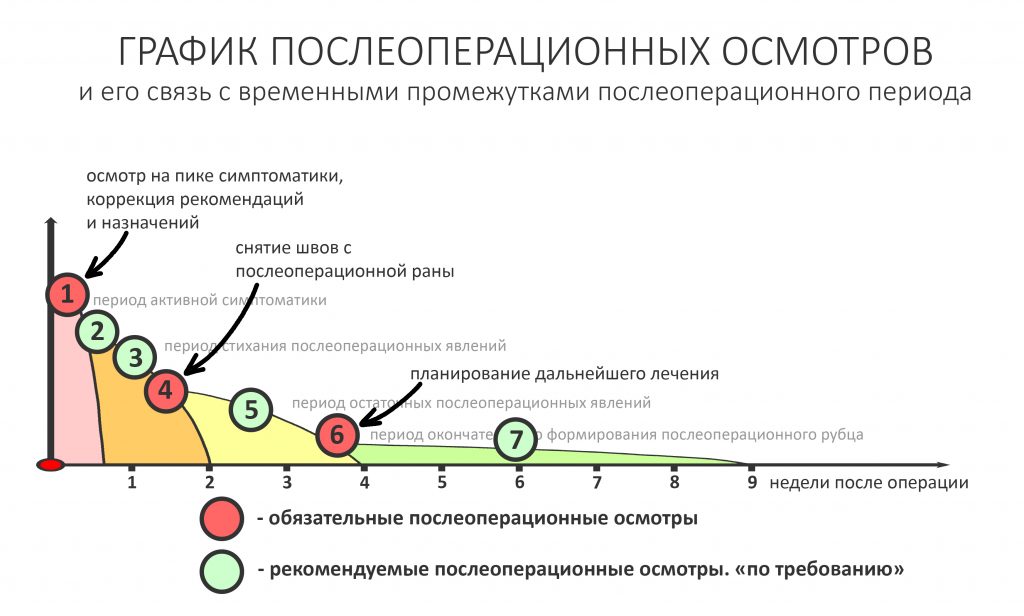
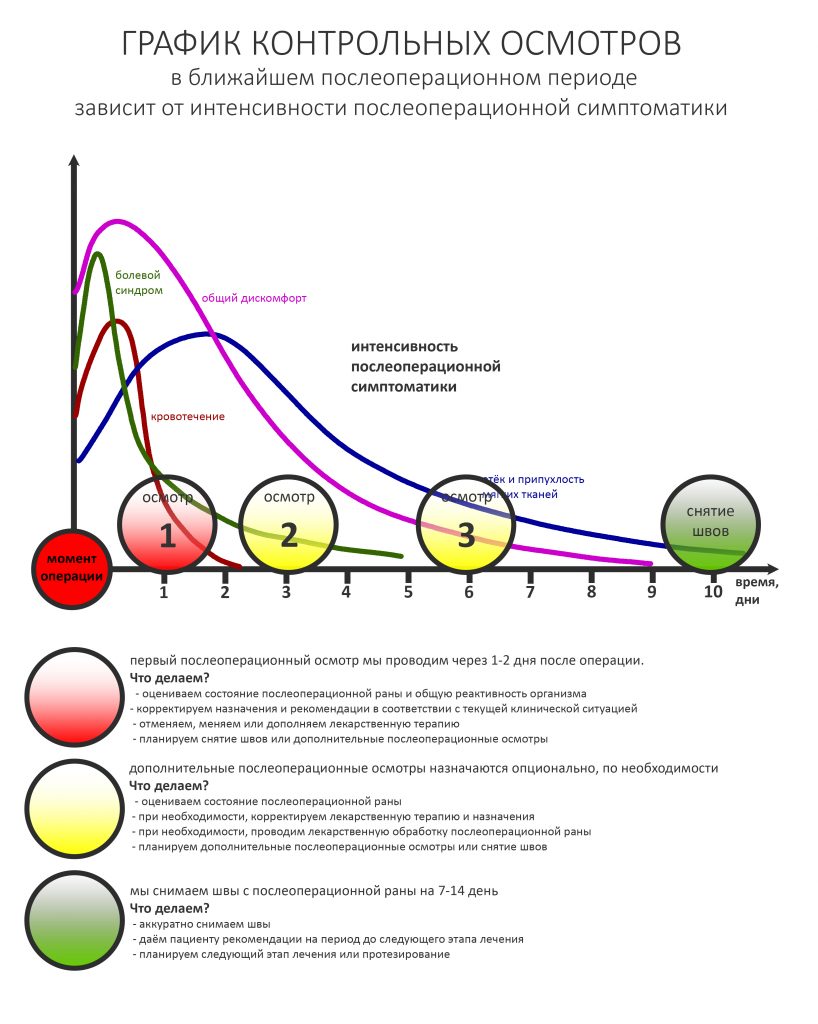
— рекомендации и назначения в письменном виде, которые мы всегда сопровождаем устными пояснениями. Их, кстати, можно найти на этой странице>>. Почитай, если интересно.
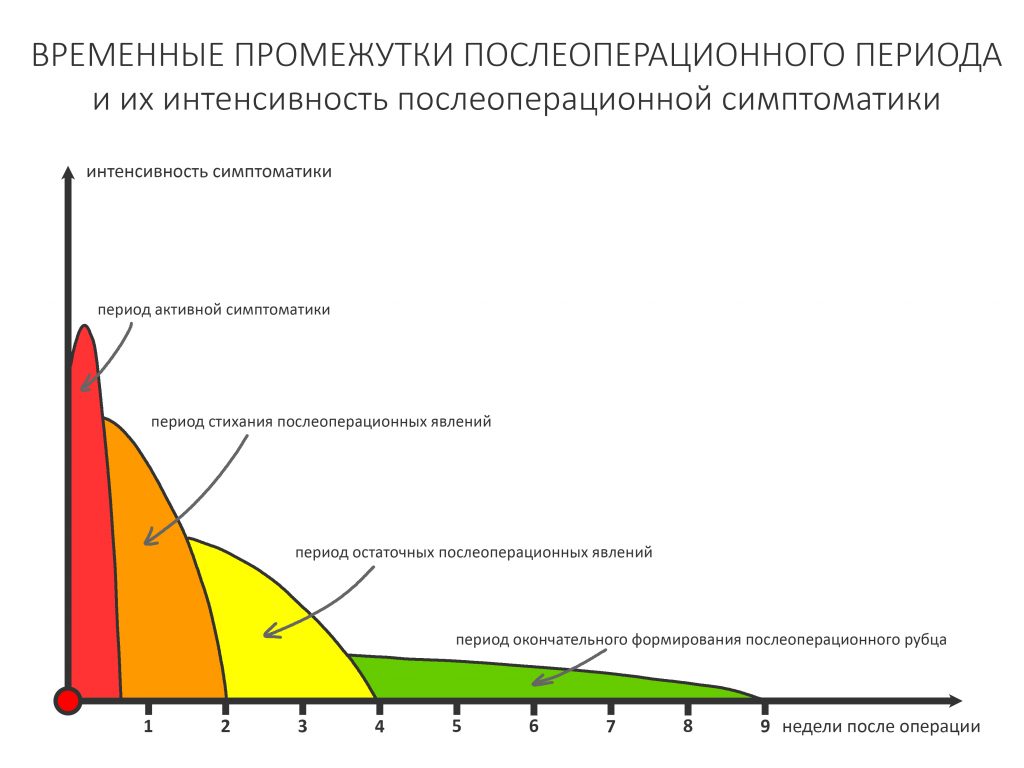
После операции
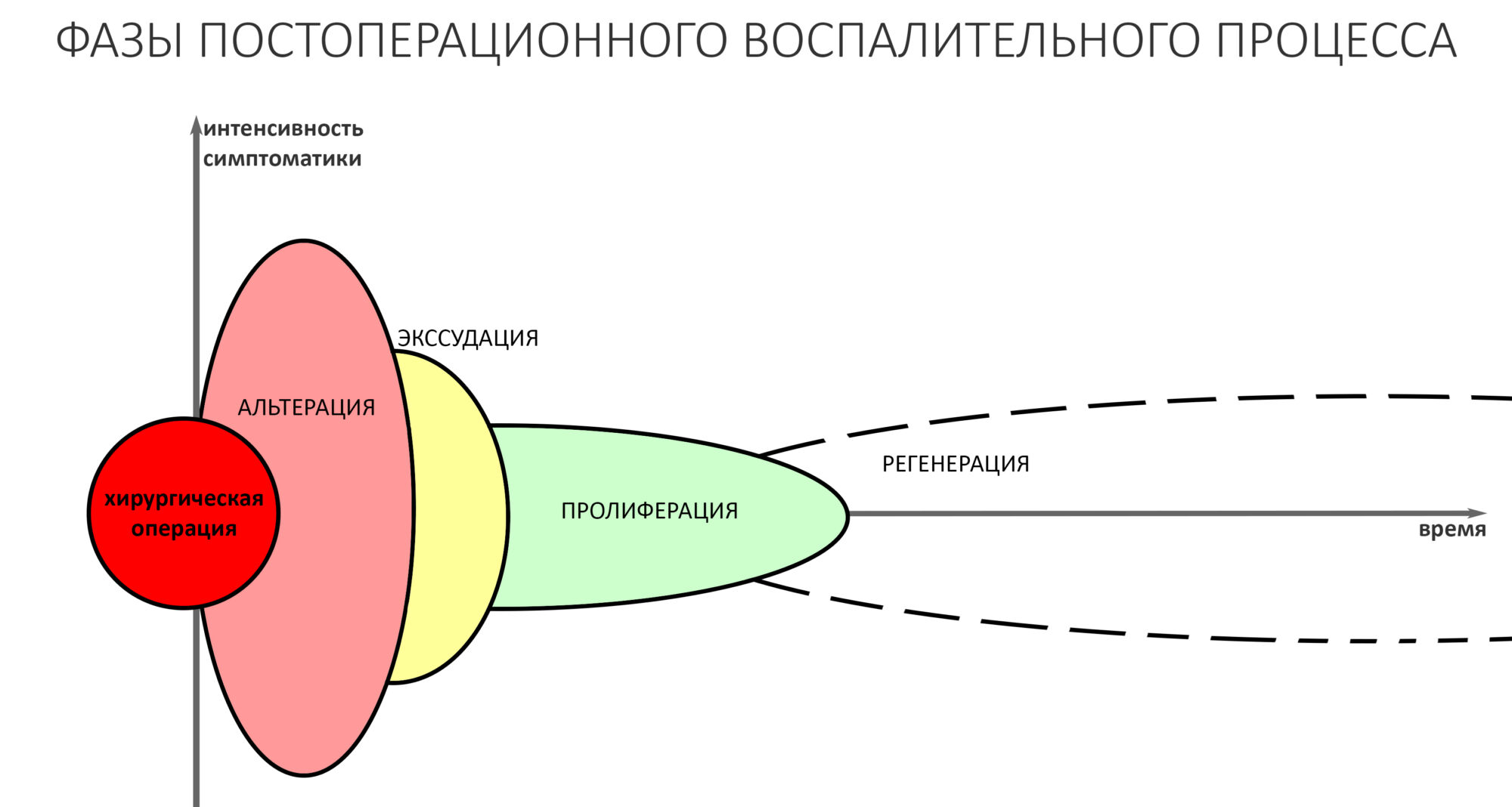
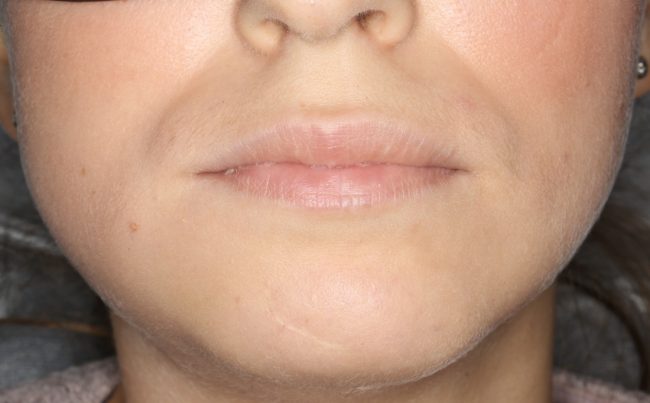
Через день мы встретились с Зинаидой, оценили симптоматику. Она вполне обычная для таких операций: болезненных ощущений практически нет, зато есть выраженный отек в пол-лица и синяк, на всю щеку, плавно переходящий на шею. От всего этого прекрасно спасала медицинская маска, и пациентка не сильно переживала. Вообще, мне нравился её позитивный настрой — на любую бабуйню, которую многие бы посчитали «ужасом-ужасом», она улыбалась и говорила: «Я думала, что будет хуже…»
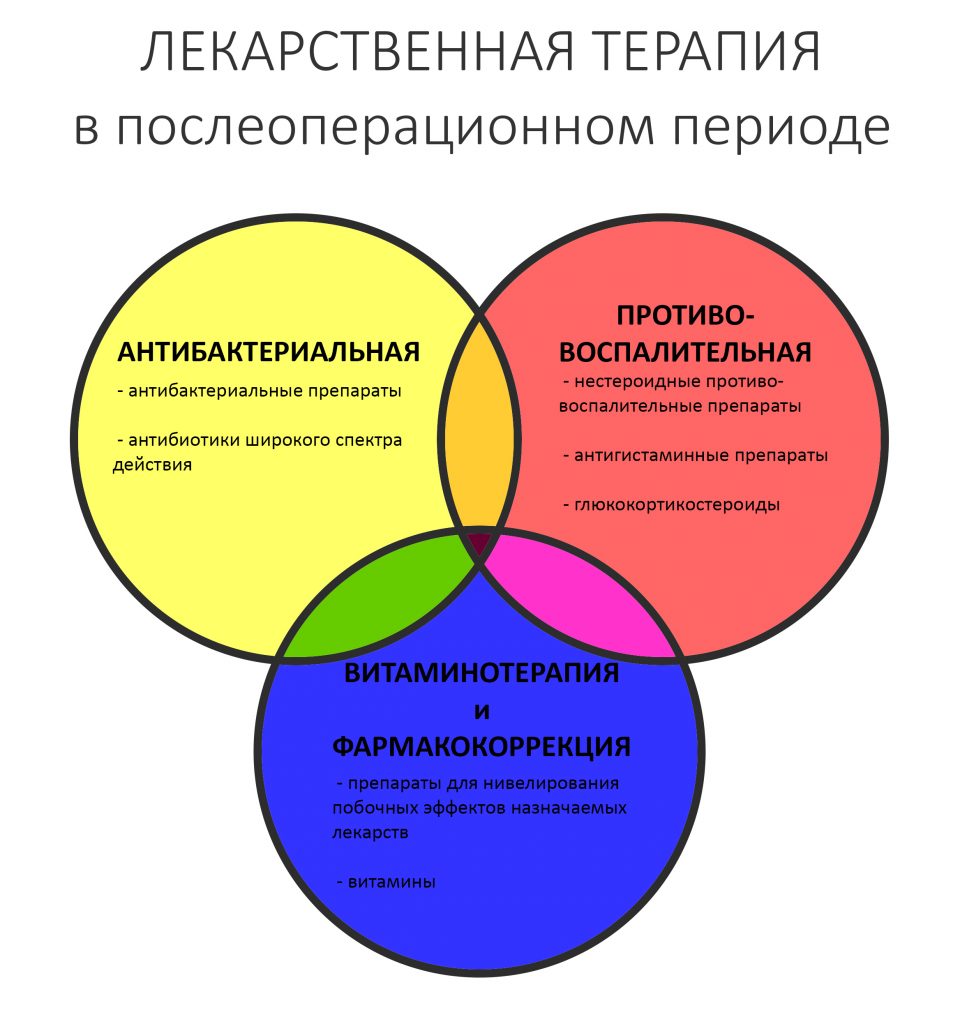
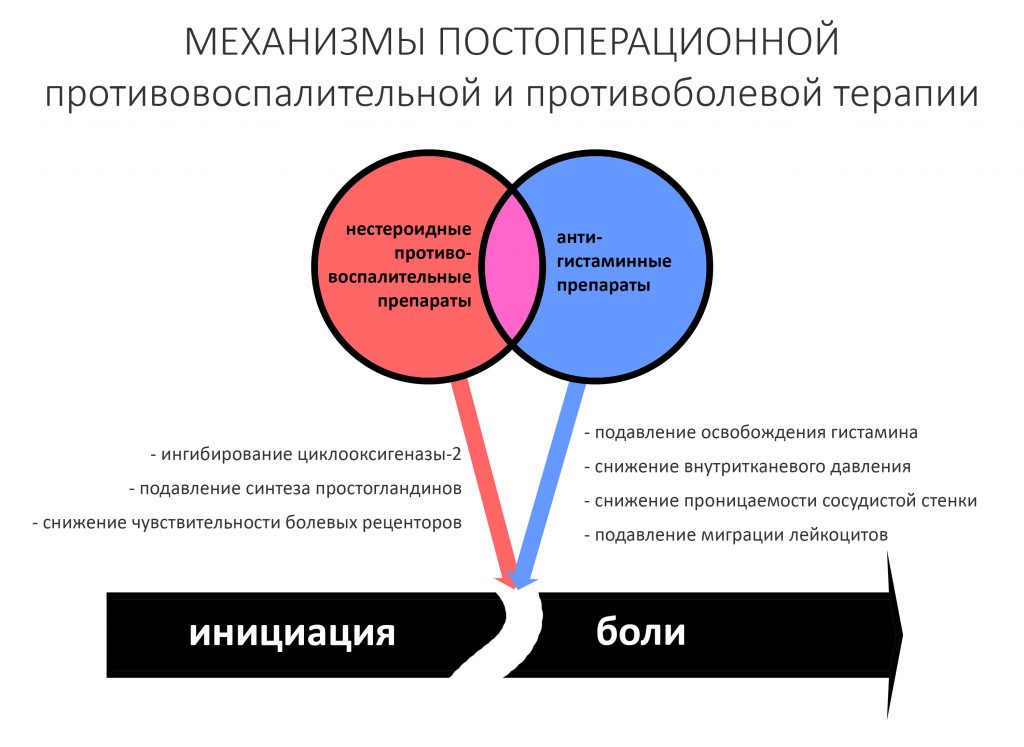
Коррекция назначений не потребовалась. Я рекомендовал держать обезболивающие (НПВС) в кармане и принимать только по необходимости. Антибактериальную терапию мы запланировали отменить через пару дней, в итоге срок приёма антибиотиков составил всего 4 дня, не считая дня операции.
Ремарка: В моих книгах подробно описаны схемы лекарственной терапии в хирургической стоматологии. Если кратко, то назначения не должны быть шаблонными, должны учитывать особенности здоровья и образа жизни пациента, быть легкими в применении и, при необходимости, корректироваться.
На следующий день после осмотра, Зинаида улетела домой, в солнечную среднеазиатскую страну.
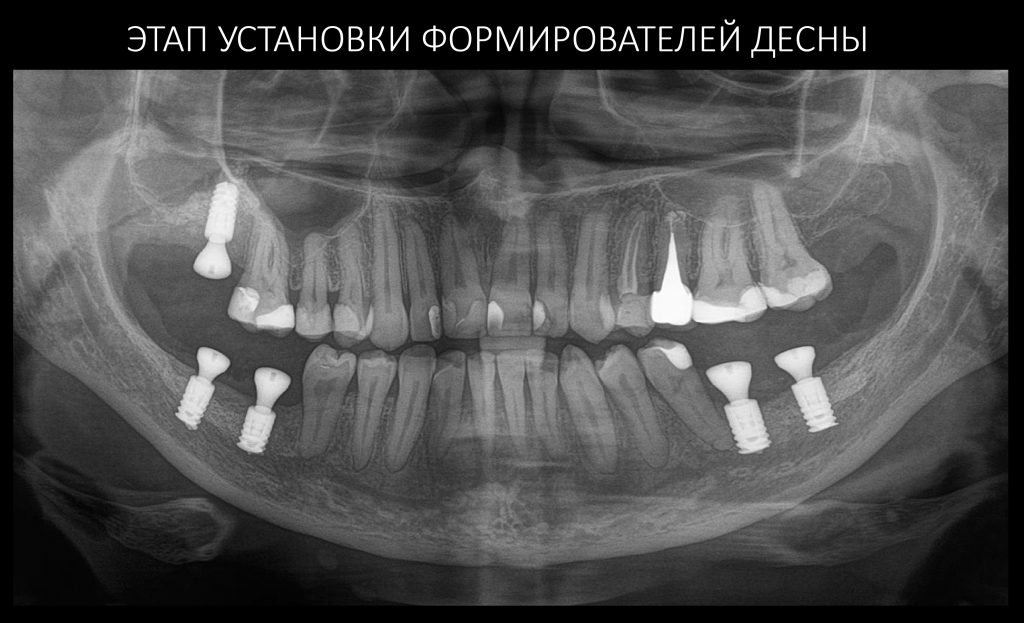
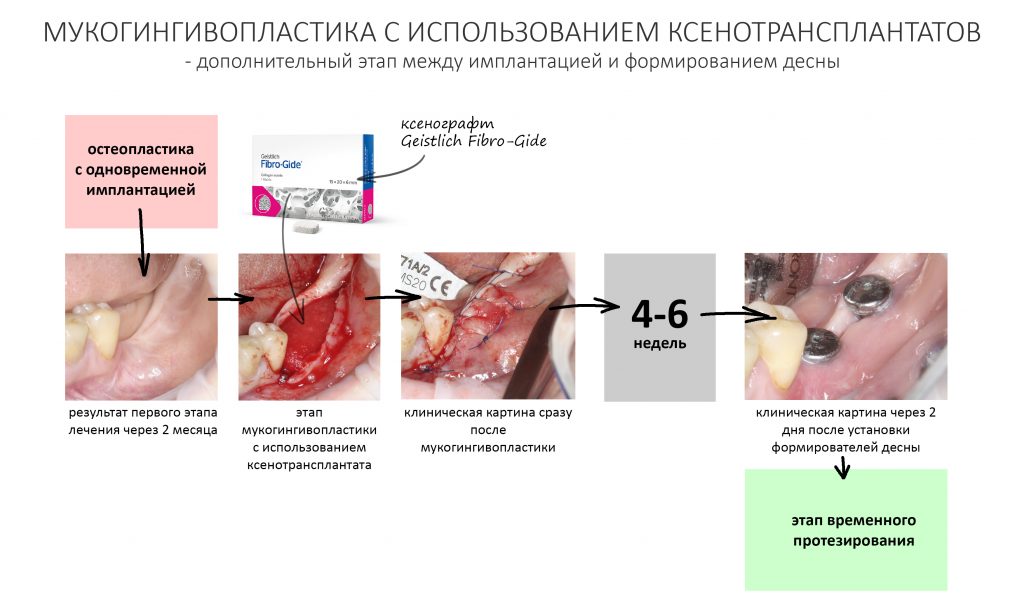
Этап установки формирователей десны
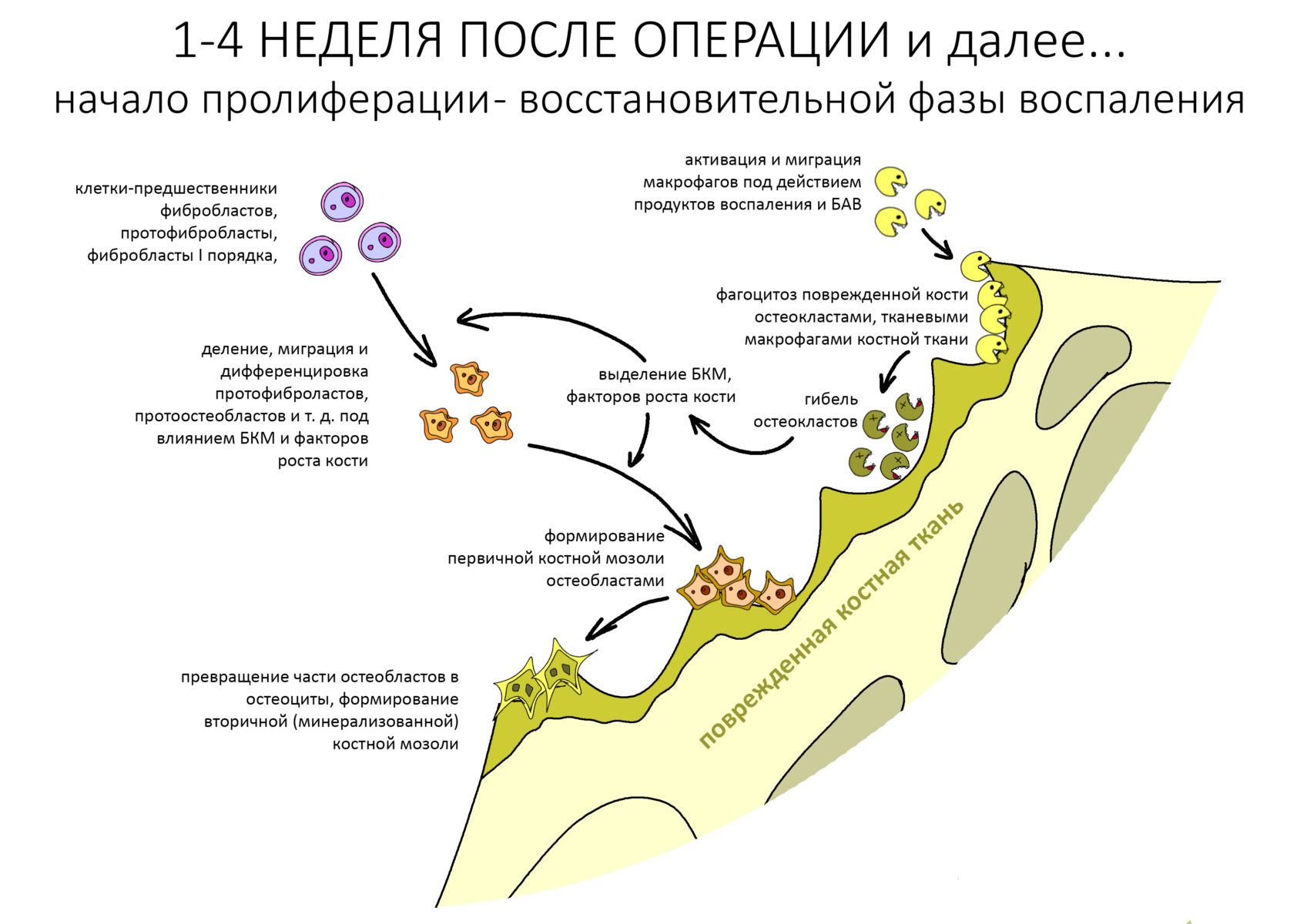
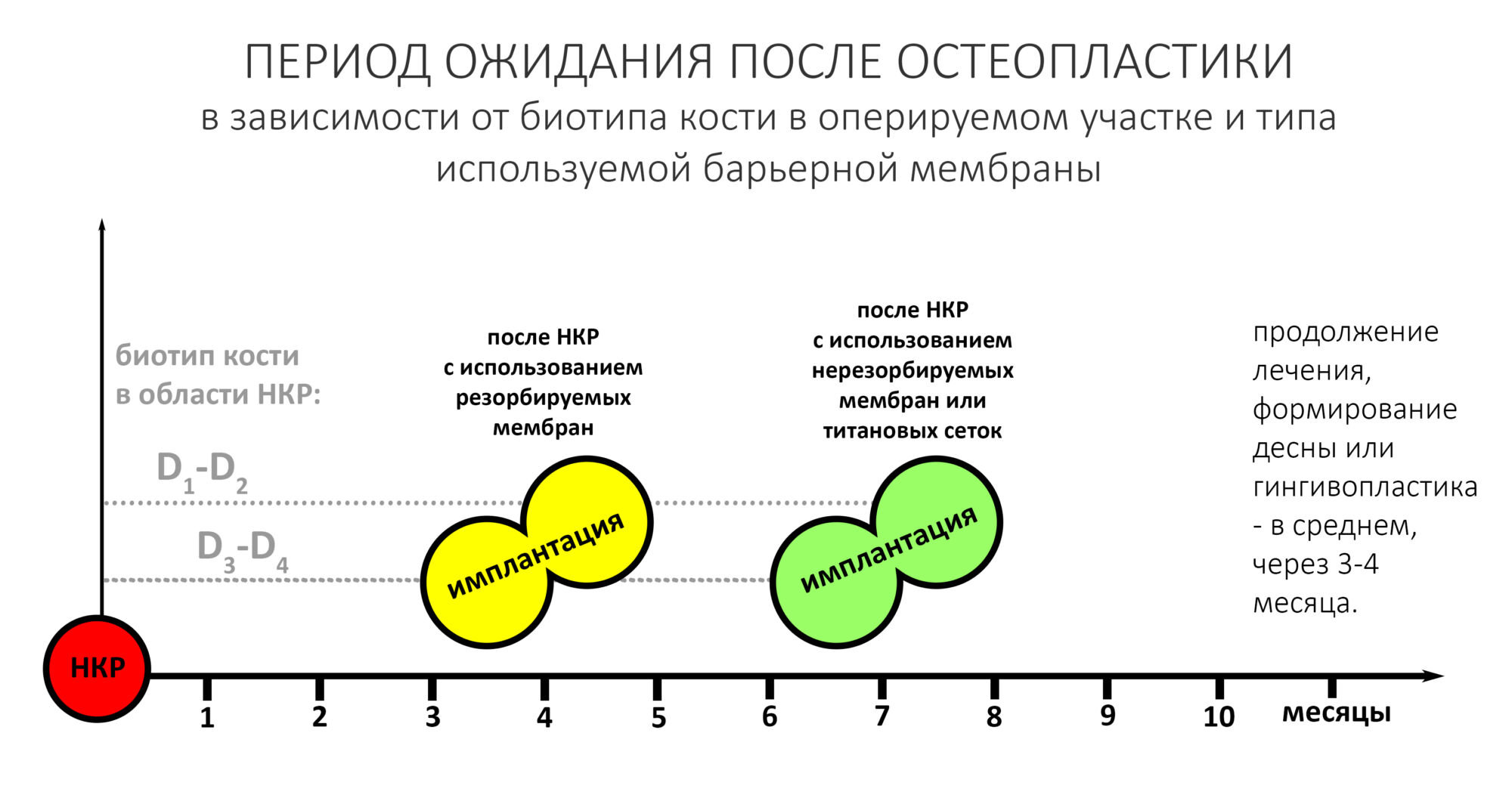
Прошло около четырех месяцев. Мы запланировали следующий этап лечения, формирование десневой манжеты (ФДМ).
Как и в прошлый раз, мы согласовали приезд Зинаиды заранее. Здесь возник целый ряд проблем:
— Сама по себе операция установки формирователей десны довольно простая и занимает, от силы, 15-30 минут. После неё редко бывают какие-нибудь осложнения, она не требует такого наблюдения, как, например, остеопластика или имплантация. По сути, пациентка едет к нам ради 15-минутной хирургической процедуры, стоимость которой в два раза ниже, чем билеты до Москвы и обратно.
— Следовательно, если и приезжать, то сразу на этапы протезирования. Но к ним возможно приступить только через несколько дней после установки формирователей десны, а само временное протезирование занимает, в среднем, около недели. Иными словами, Зинаиде лучше остаться в Москве дней на 10-12, и вернуться домой уже с новыми зубами. Чтобы максимально ускорить проведение протезирования, нам нужно заранее поставить все приёмы у стоматолога-ортопеда и забронировать зуботехническую лабораторию.
— Всегда есть риск, что что-то пойдет не так. Например, на этапе установки мы поймем, что остеопластика не удалась, или имплантат не интегрировался, или требуются какие-то дополнительные хирургические процедуры, вроде пластики десны. В этом случае план предстоящего лечения кардинально меняется, мы обламываем и пациента, и зуботехническую лабораторию. А у стоматолога-ортопеда пропадает ценное время. Объясняться со всеми и выяснять, кто кому что должен, весьма не просто.
Ремарка: вот поэтому я сделал специальную страницу для пациентов из других городов, регионов и стран, желающих лечиться в нашей клинике. И не очень одобряю стоматологический туризм "набегами", без должного контроля врачом по месту жительства и взаимодействием с лечащей клиникой.
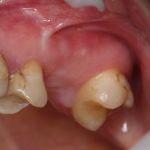
Итак, Зинаида на приеме.
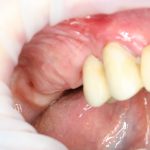
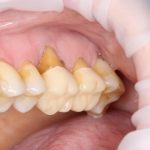
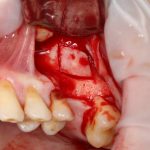
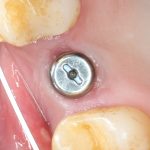
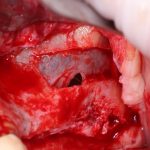
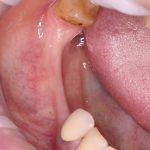
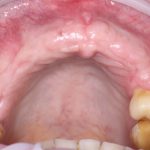
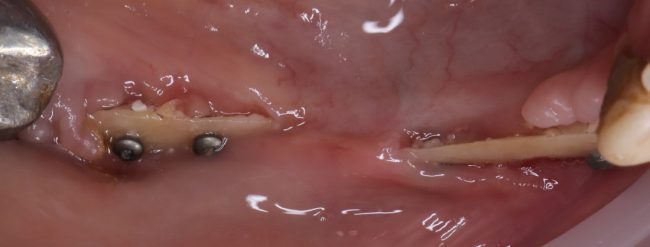
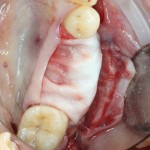
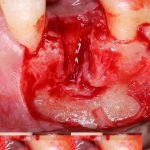
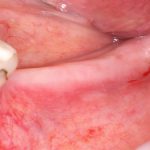
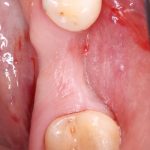
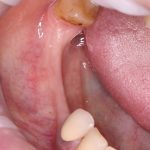
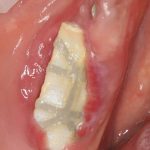
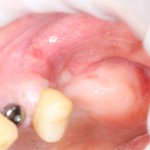
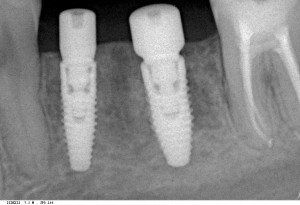
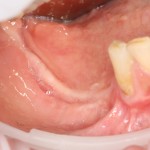
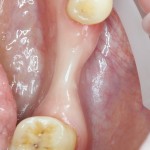
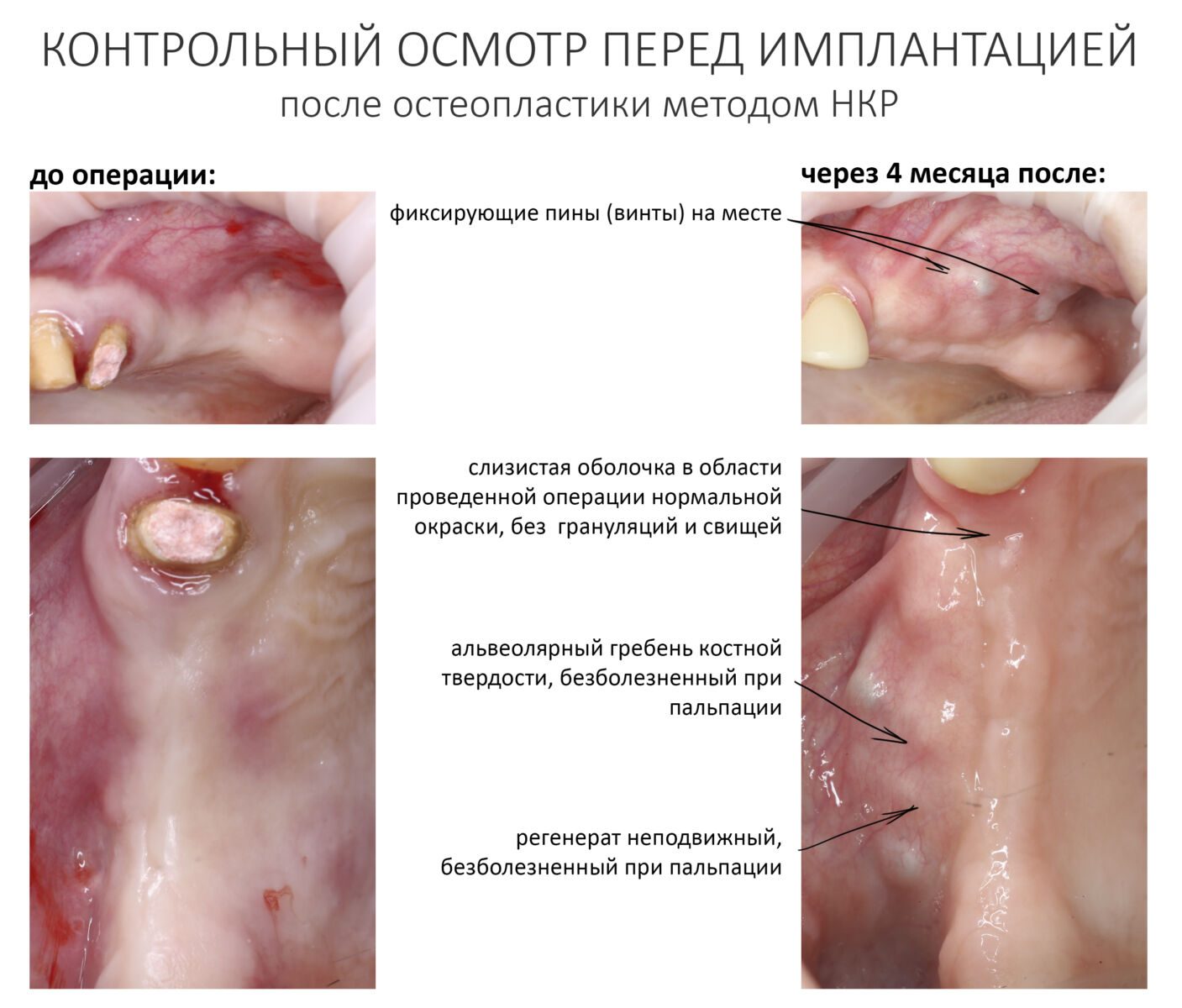
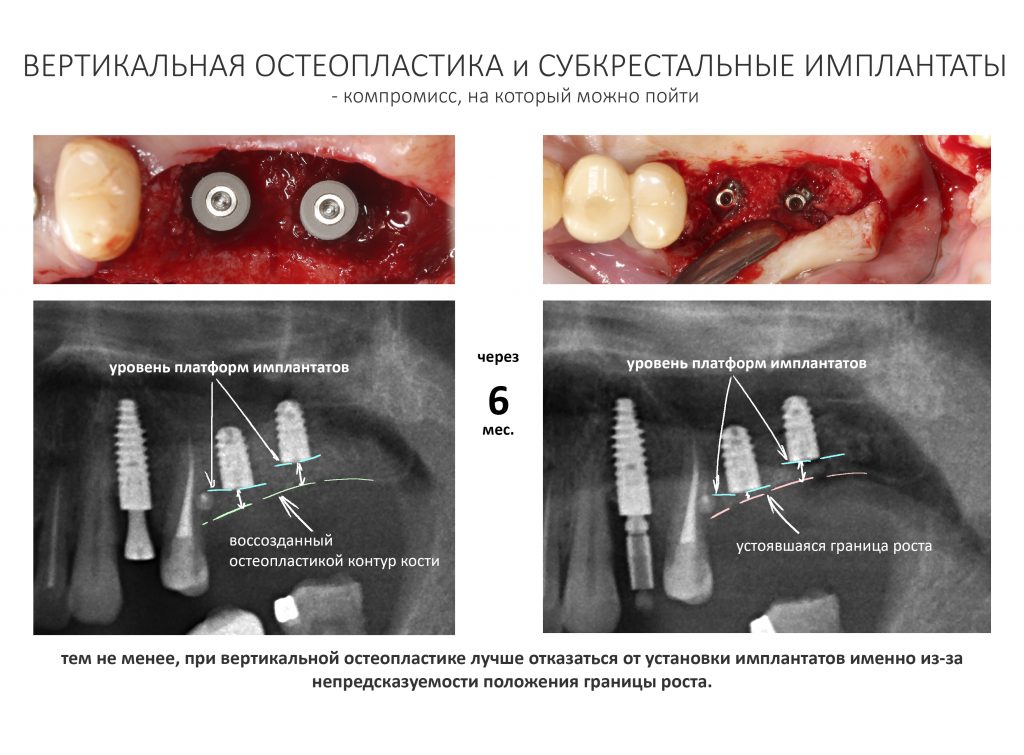
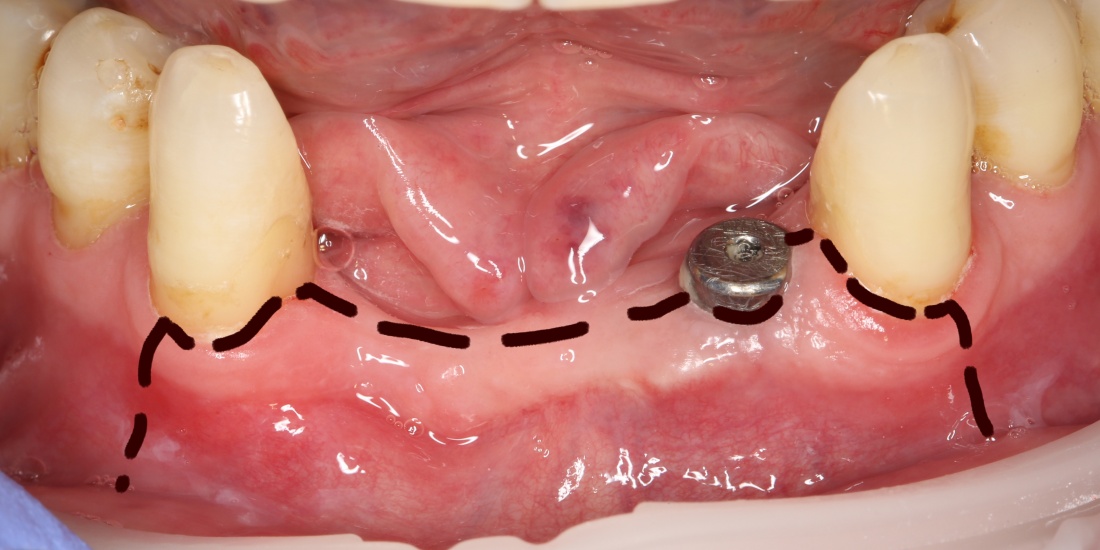
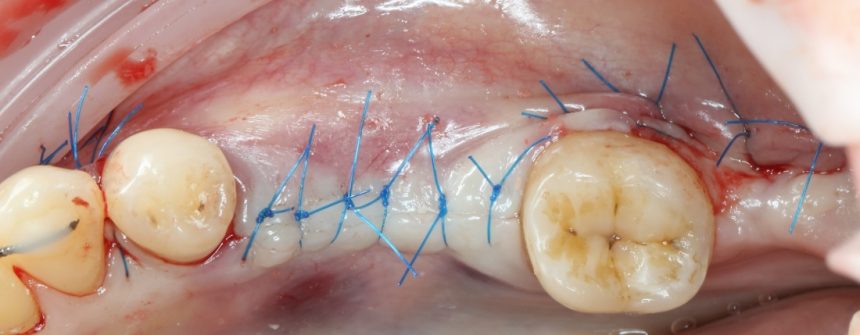
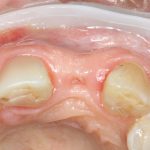
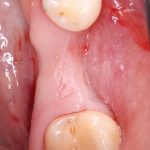
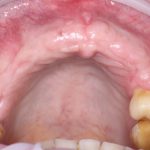
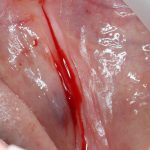
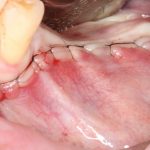
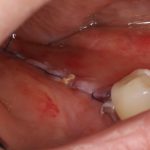
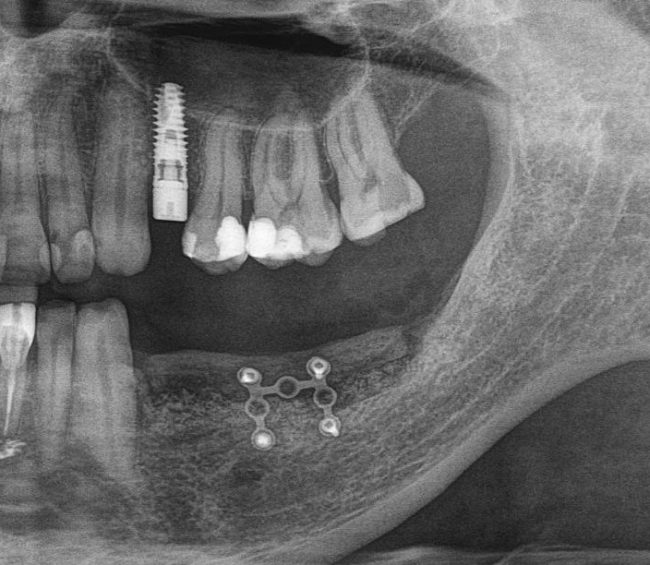
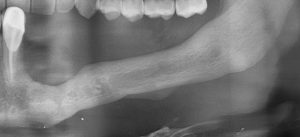
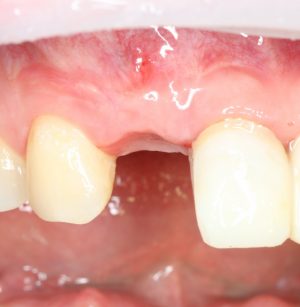
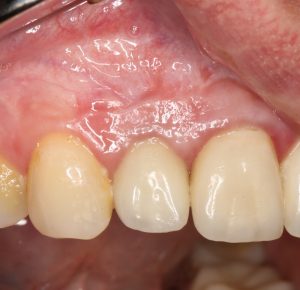
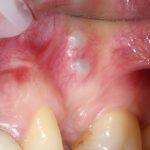
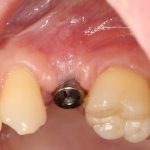
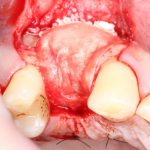
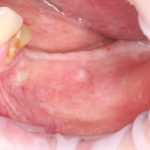
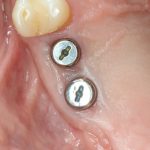
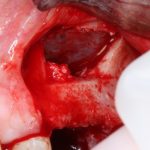
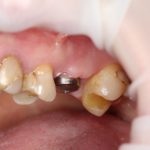
Вот клиническая картина через 4 месяца после ранее проведенной имплантации с остеопластикой:
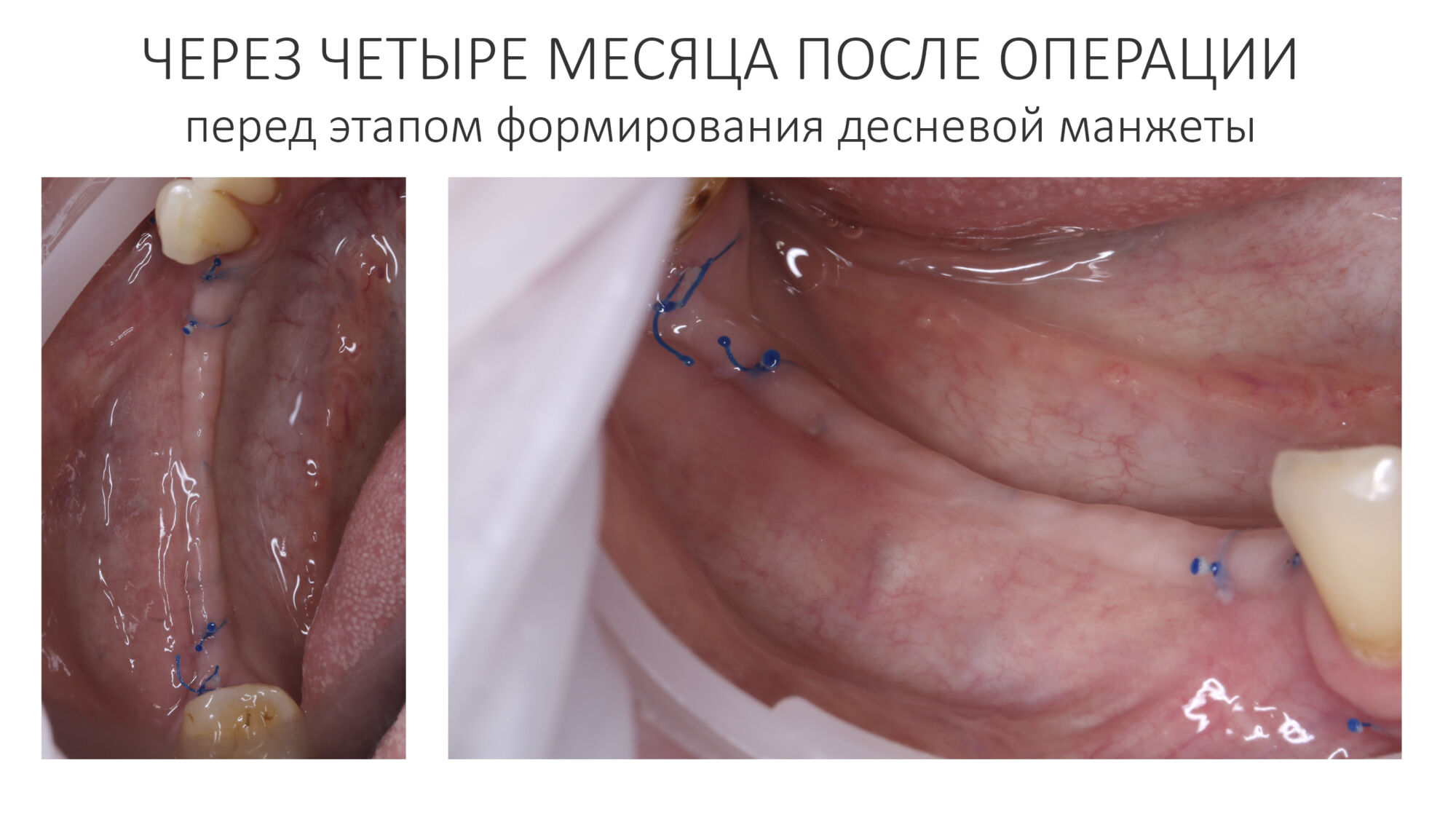 Как видишь, коллеги из недалекой дружественной страны не осилили снятие швов. Мне это не нравится, хотя и объясняет, почему люди готовы ехать за тыщи километров ради 20-минутной операции удаления зуба мудрости.
Как видишь, коллеги из недалекой дружественной страны не осилили снятие швов. Мне это не нравится, хотя и объясняет, почему люди готовы ехать за тыщи километров ради 20-минутной операции удаления зуба мудрости.
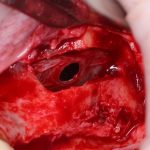
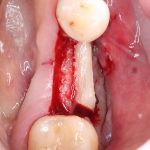
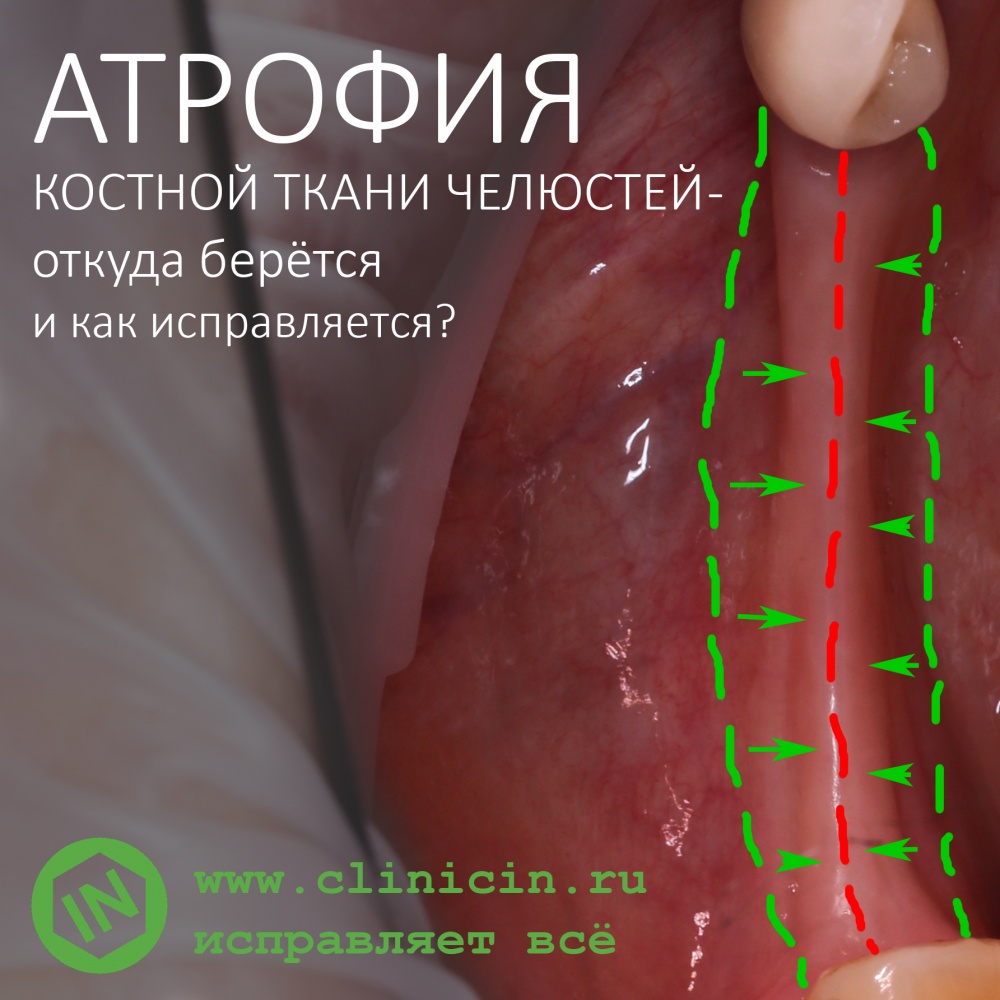
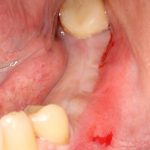
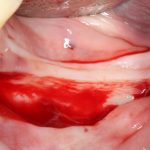
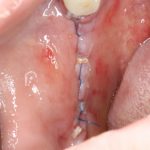
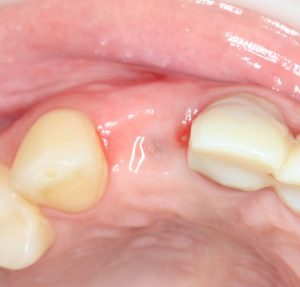
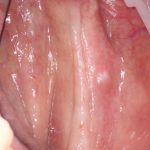
Ну хорошо. Швы сняли. Делаем разрез. Обрати внимание, что после всех проведенных операций у нас остается очень небольшой по ширине слой жевательной слизистой оболочки:
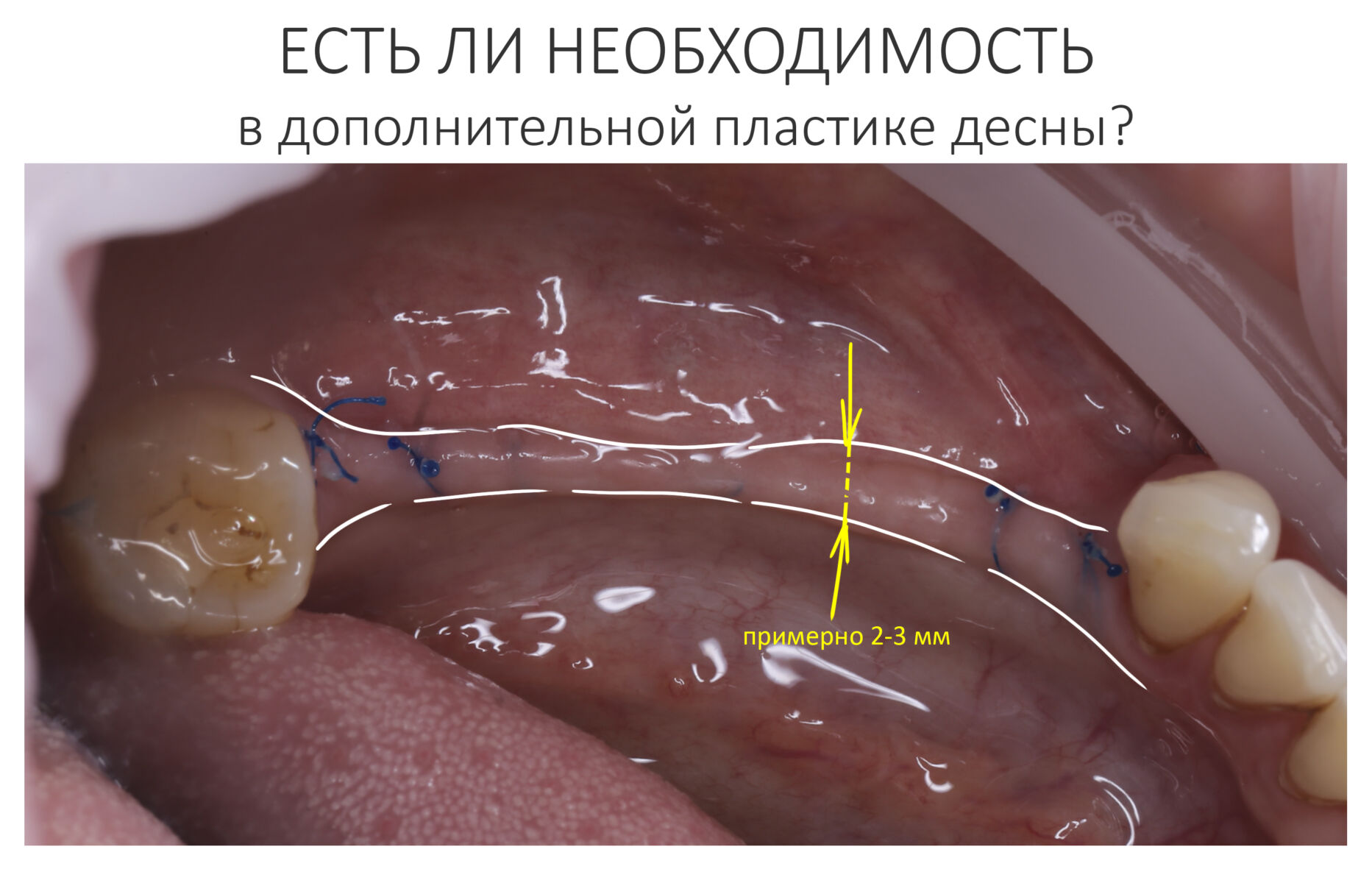 в связи с чем возникает резонный вопрос:
в связи с чем возникает резонный вопрос:
А нет ли здесь необходимости в дополнительной пластике десны?
Напомню, то был 2014 год. В те времена отношение моих коллег к пластике десны как к необходимому этапу имплантологического лечения сводилось к двум крайностям: от «нафиг не нужна» до «делаем всегда». Не все понимали её смысл, далеко не всегда доктора могли обосновать клинические показания для её проведения. Это сейчас мы такие умные и всё знаем. Провели сотни нужных и ненужных операций, написали кучу статей по этому поводу:
Сохранение и формирование десневого контура: от простого к сложному и наоборот.
ВОКРУГ ИМПЛАНТАТОВ: нулевая утрата кости, биологическая ширина десны и всё такое.
А тогда… тогда я решил обойтись без дополнительной хирургической процедуры. И вот, почему.
Во-первых, дополнительная хирургия сильно бы осложнила логистику лечебного процесса. Пациентке пришлось бы приезжать еще раз (издалека), а сам этап протезирования откладывался бы на несколько месяцев. Этого не хотели ни я, ни пациентка, ни стоматолог-ортопед.
Во-вторых, к тому моменту у меня были прекрасные результаты лечения и в более худших условиях по десне. В конце концов, нам ничто не помешает провести эту операцию и после протезирования, если что-то пойдет не так.
В-третьих… в третьих, лучшая операция — это та, которой удалось избежать. Вот мы и ведем дело… к лучшей операции.
Конечно, сейчас мы действуем значительно деликатнее. И не делаем такие разрезы без необходимости:
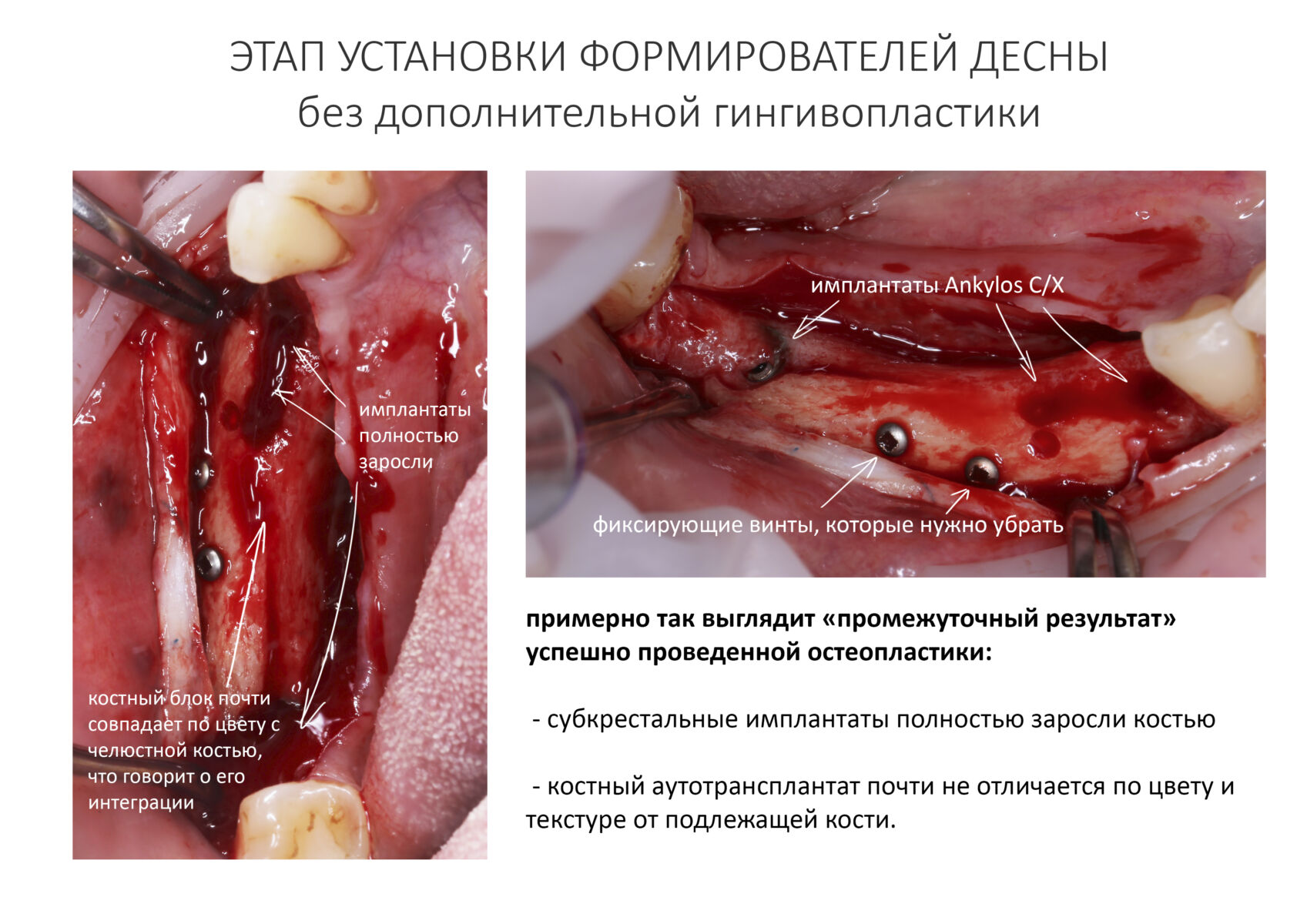 С другой стороны, если бы делали «как сейчас», ты не увидел бы ничего интересного.
С другой стороны, если бы делали «как сейчас», ты не увидел бы ничего интересного.
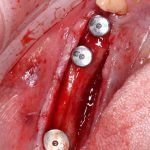
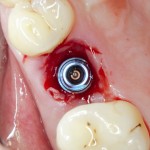
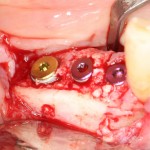
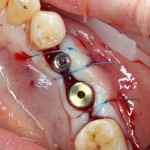
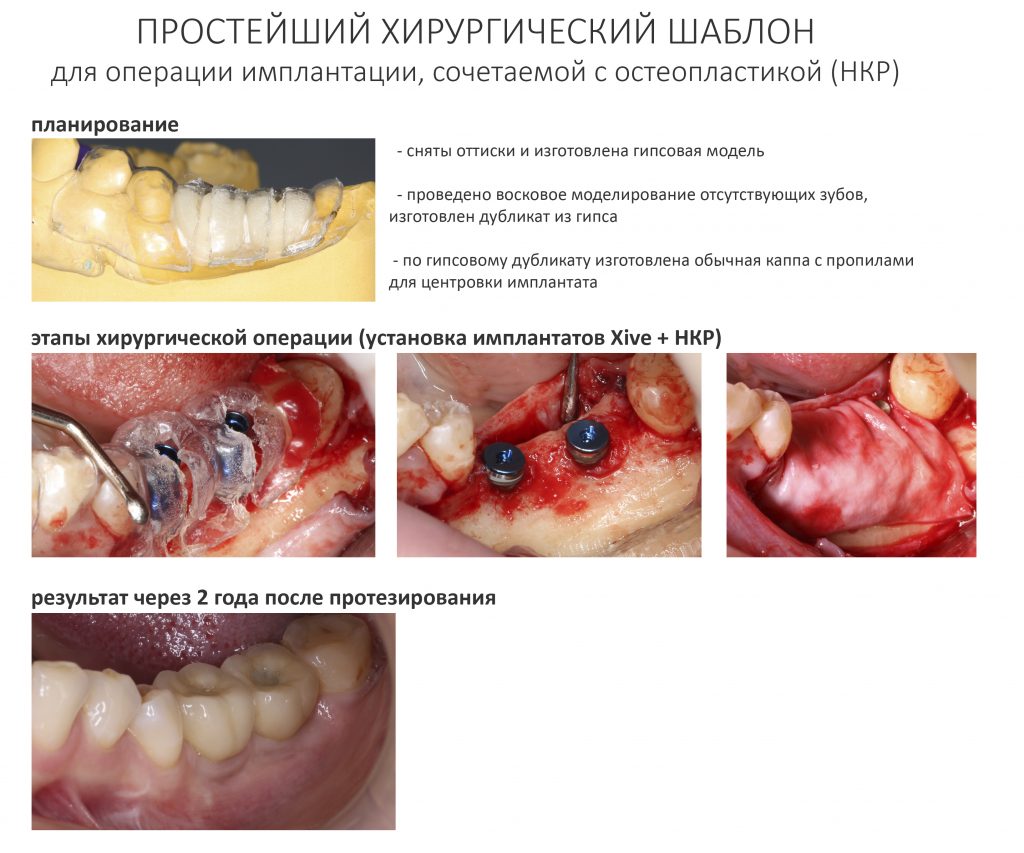
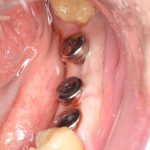
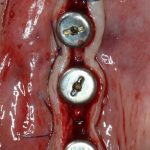
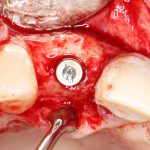
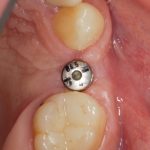
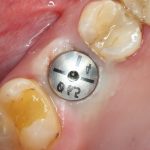
Устанавливаем формирователи десневой манжеты. Сегодня я называю эту процедуру не менее важной, чем любой другой этап имплантологического лечения:
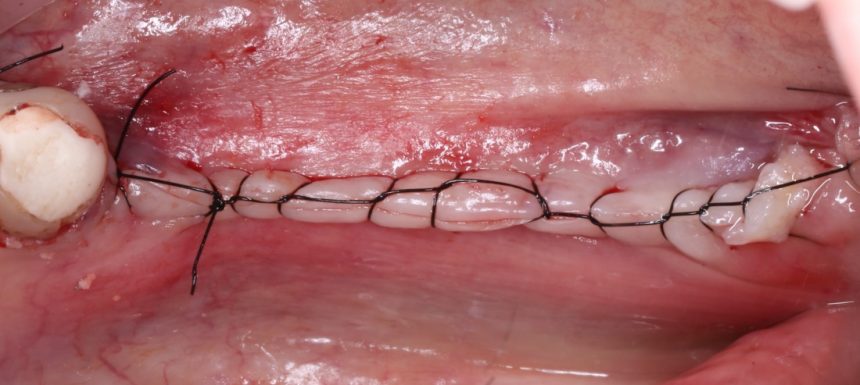
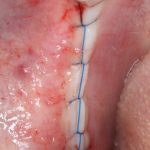
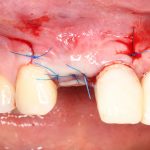
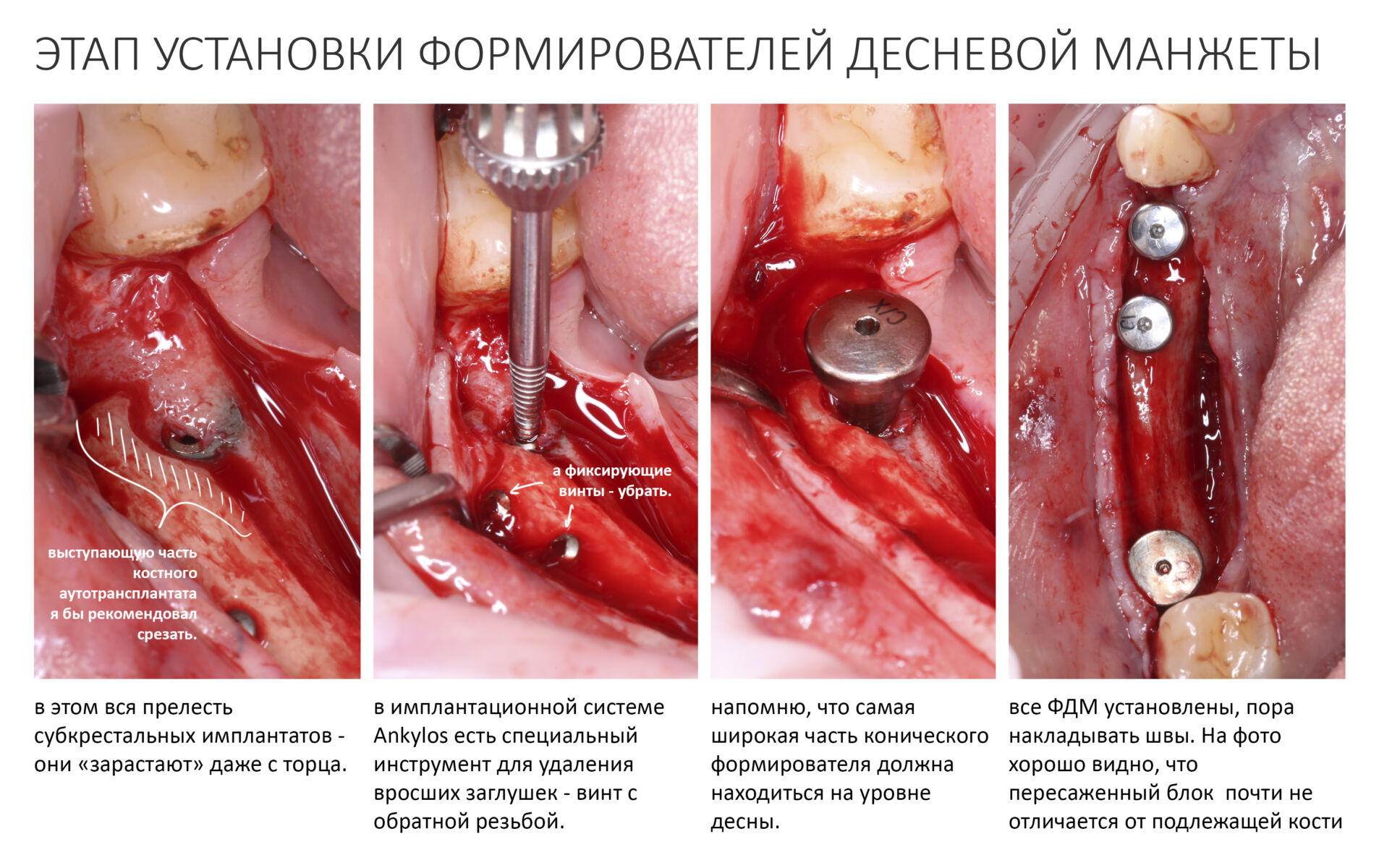 И швы. Просто швы. Никаких дополнительных процедур.
И швы. Просто швы. Никаких дополнительных процедур.
 Если честно, то сейчас бы я использовал другой шовный материал и другой тип швов. Одно неизменно, — и я об этом много раз говорил, — самая широкая часть формирователя десны должна находиться на уровне десны. Так, чтобы эффективно отрабатывать т. н. «биологическую ширину».
Если честно, то сейчас бы я использовал другой шовный материал и другой тип швов. Одно неизменно, — и я об этом много раз говорил, — самая широкая часть формирователя десны должна находиться на уровне десны. Так, чтобы эффективно отрабатывать т. н. «биологическую ширину».
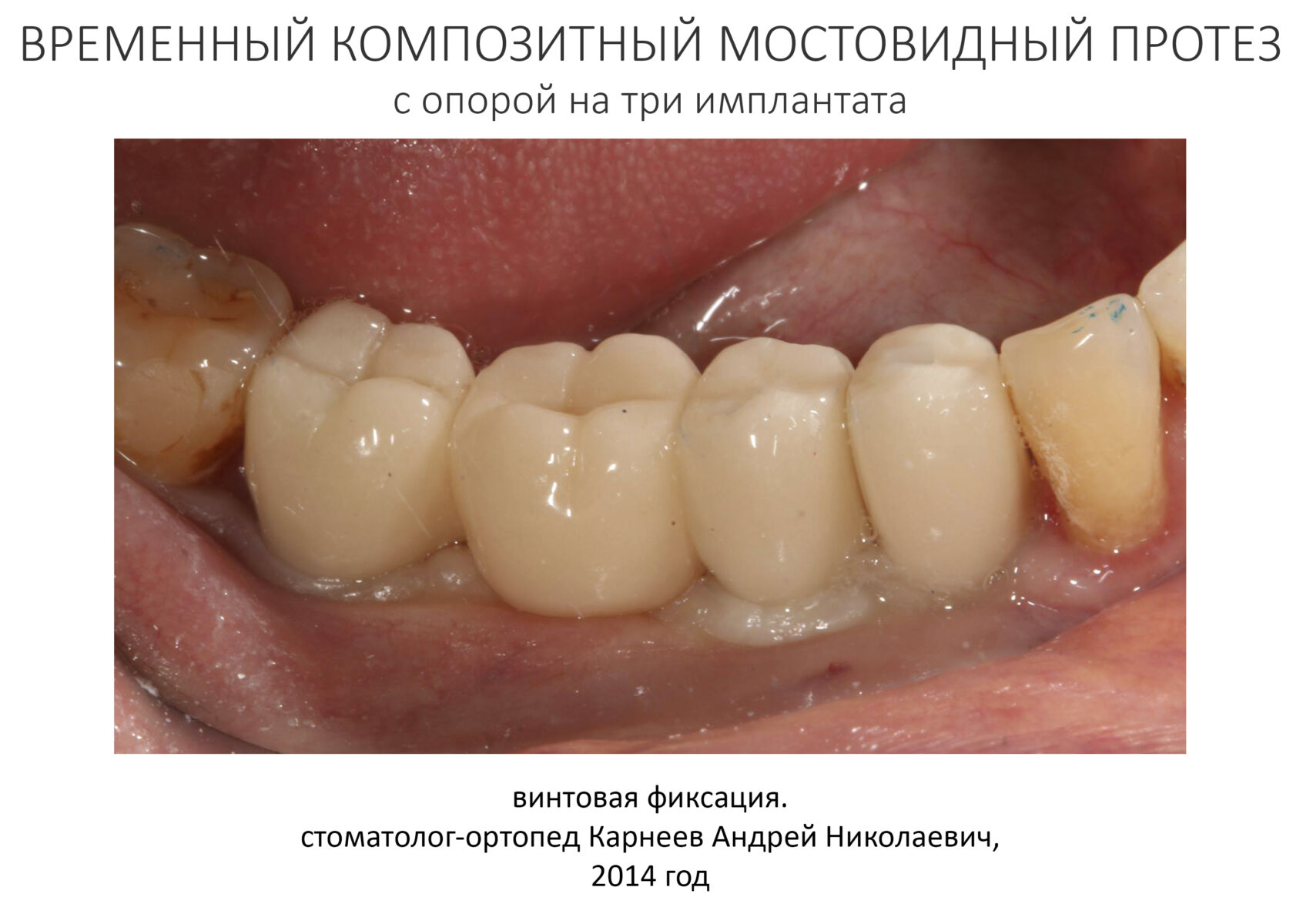
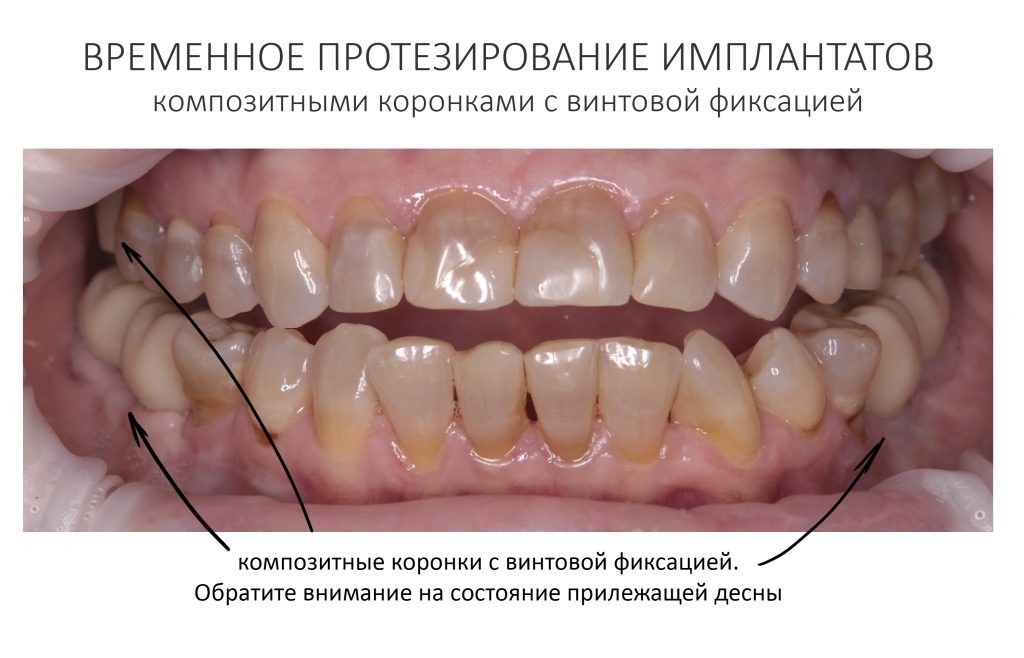
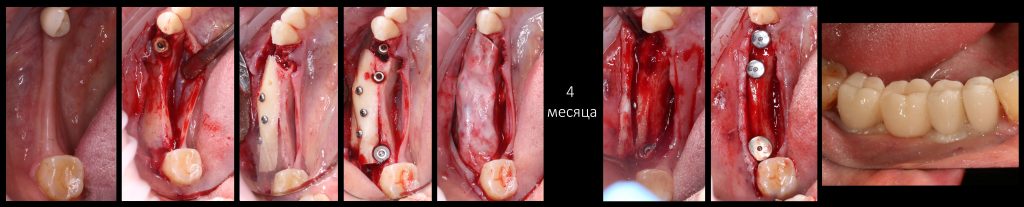
Через неделю я снял швы, а мой коллега Андрей Карнеев (дело было еще в НИЦ) приступил к изготовлению протезов. На это ушло полторы недели:
Ремарка: Во всех случаях "сложной" имплантации первым делом изготавливаются временные коронки на срок до 12 месяцев. Здесь мы провели остеопластику одновременно с имплантацией - и это вполне катит за "сложную" имплантацию и требует изготовления временных коронок на минимальный срок 6 месяцев.
«Ого, какие классные зубы!» — сказала тогда Зинаида, после чего мы попрощались и договорились встретиться через полгода-год для замены временного протеза на постоянный керамический. Зинаида вернулась домой, в дружественную среднеазиатскую страну.
Ежу понятно, что ни через полгода, ни через год мы не встретились…
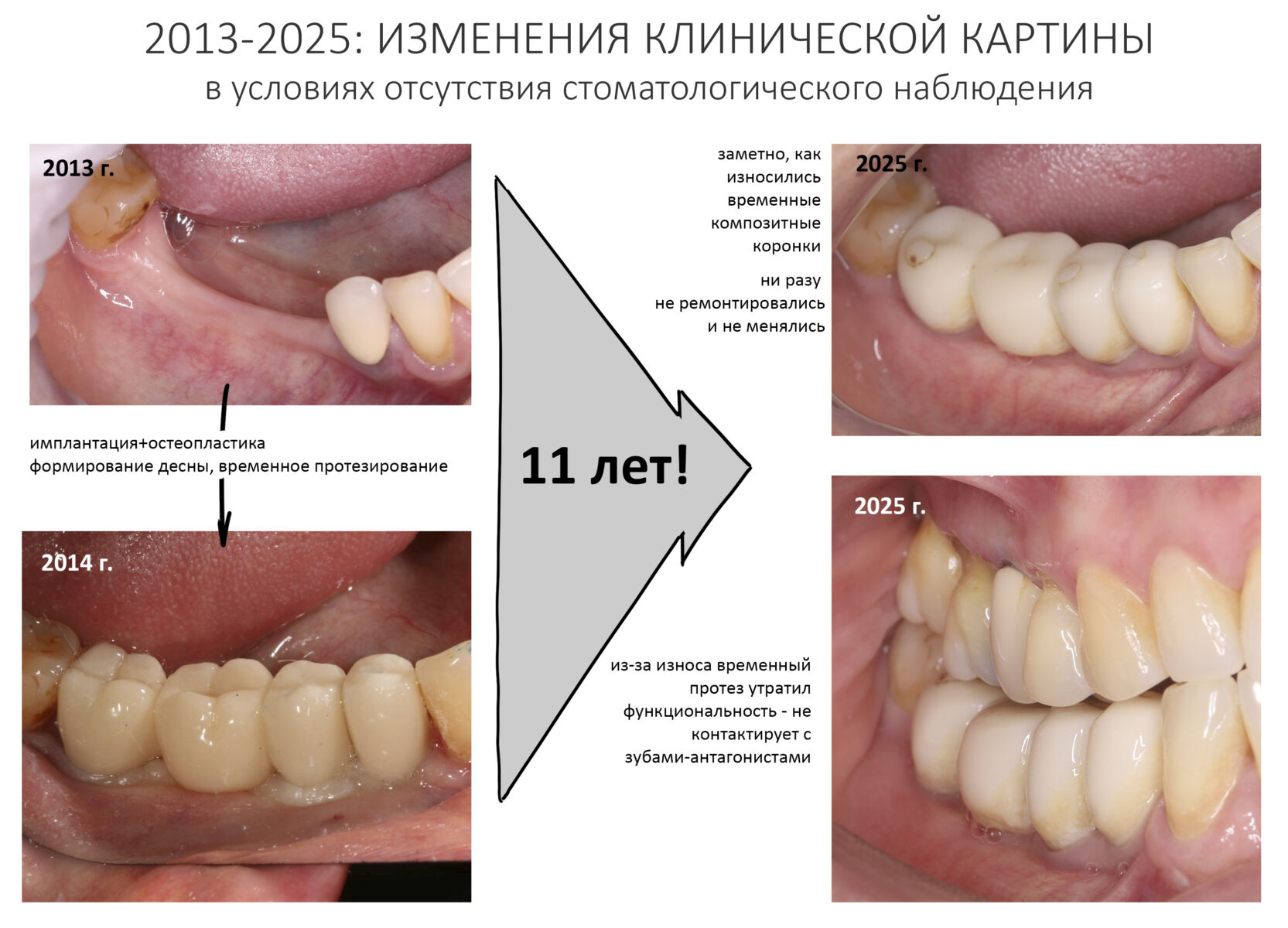
2025 год, наши дни.
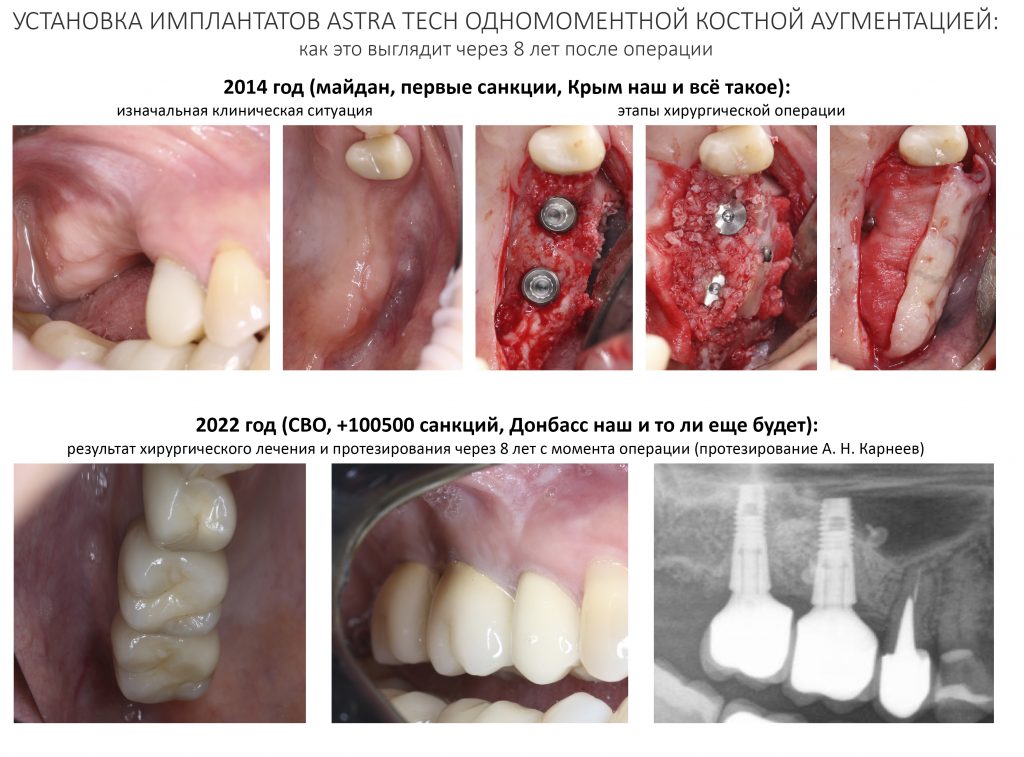
Стоит ли говорить, как много событий произошло с момента последней нашей встречи? Произошел госпереворот на Украине (2014), после которого Крым стал нашим, и против нашей страны были введены первые санкции. в 2020 году эпидемия COVID-19 наглядно показала, как ОРВИ может вырубить экономику целых регионов, и как легко можно управлять людьми и миром. Про 2022 год я вообще молчу — СВО и конфликт на Украине (прямое следствие госпереворота-2014) четко поделили общество на своих и чужих, наглядно показали, кто есть кто.
С момента проведенного лечения прошло 11 лет. Честно говоря, я подумал, что никогда больше не увижу Зинаиду, и что постоянное протезирование ей провели местные среднеазиатские доктора.
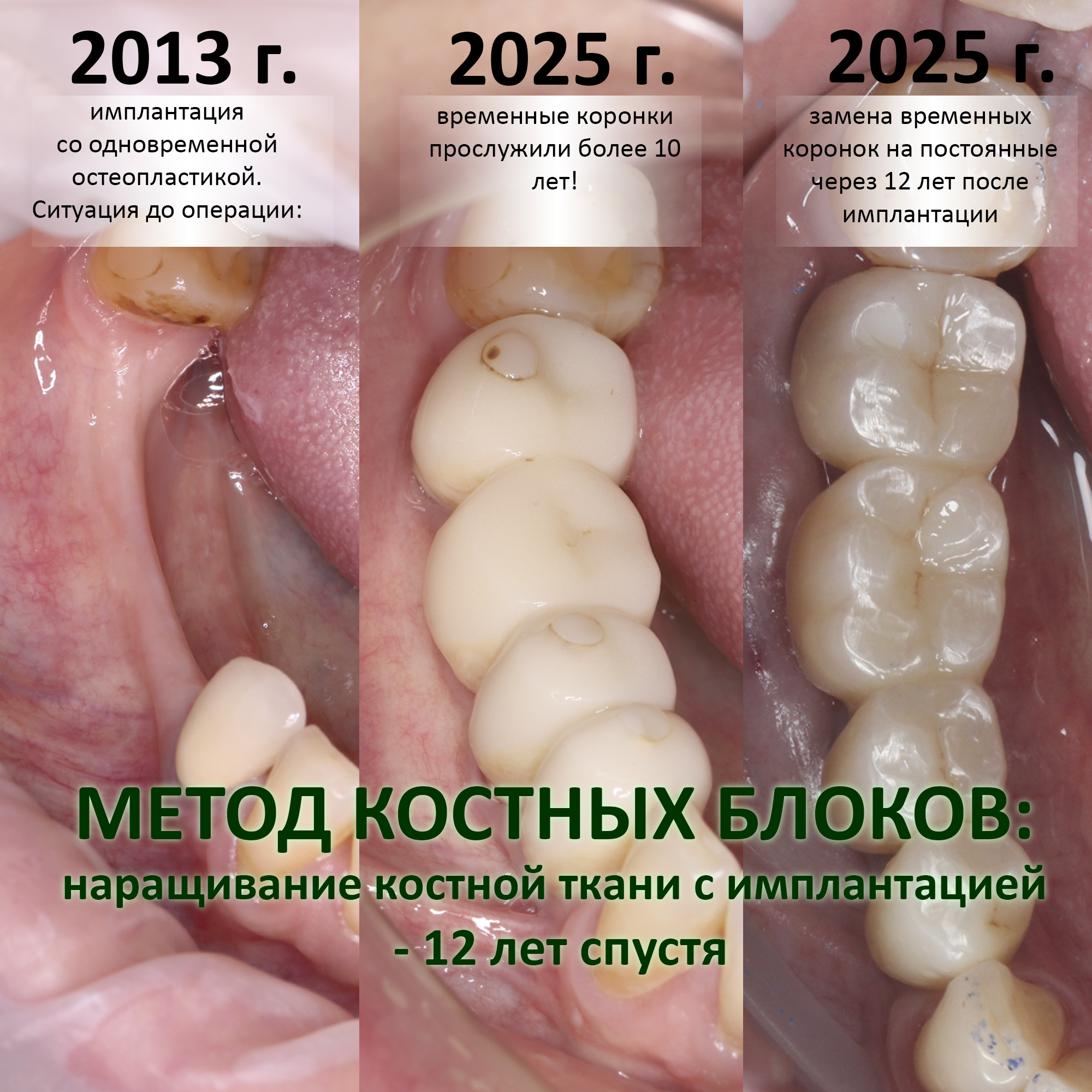
Но… в начале 2025 года я получаю от Зинаиды письмо, в котором она просит закончить лечение. Я с ужасом ожидал каких-нибудь жалоб и проблем (всё же, 11 лет без наблюдения стоматолога), но оказалось, что Зинаида просит поменять износившиеся временные коронки на постоянные. Да-да, ты не ослышался! Она 11 лет пользовалась временными коронками, и всё, что её беспокоит — это износ временных коронок!. Это абсолютный рекорд, я считаю.
К счастью, страна, где проживает Зинаида, осталась дружественной и после 2022 года. Более того, сохранила прямые рейсы с Москвой. Мы легко договорились о встрече и продолжении лечения. По тем же правилам, что и в прошлый раз.
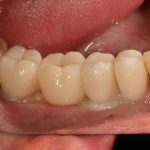
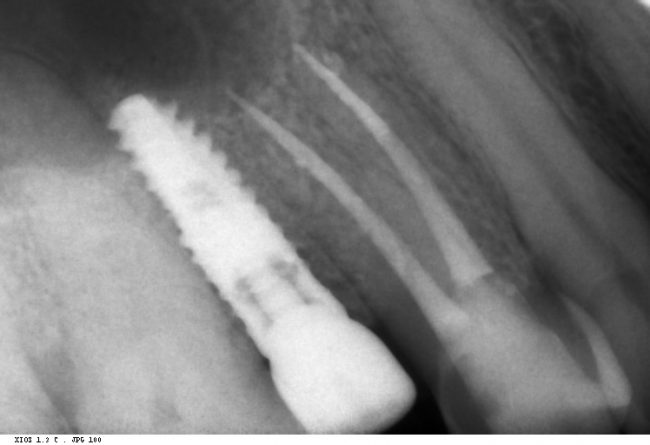
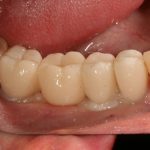
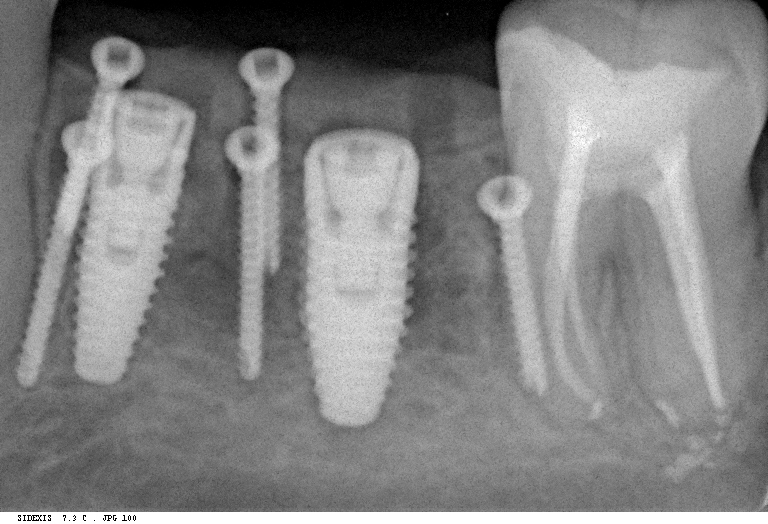
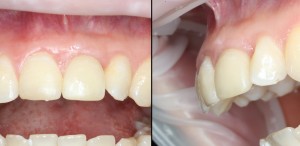
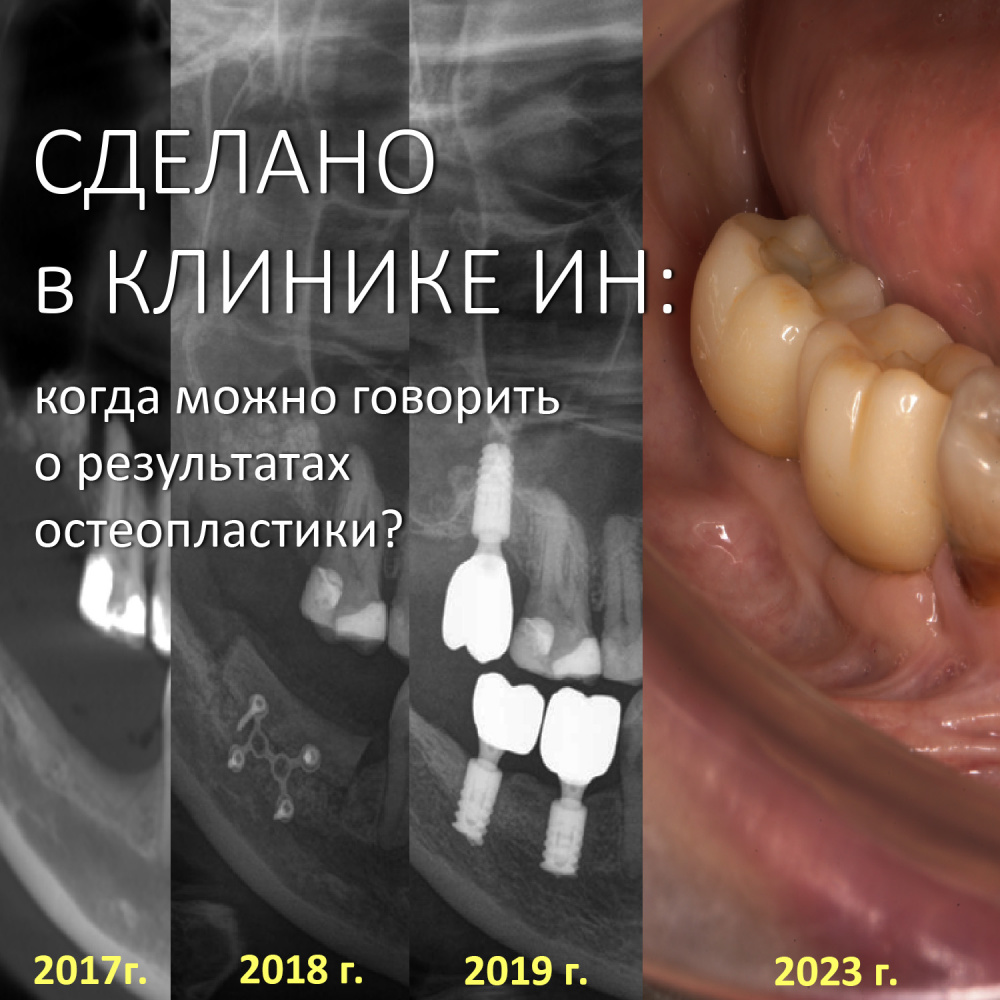
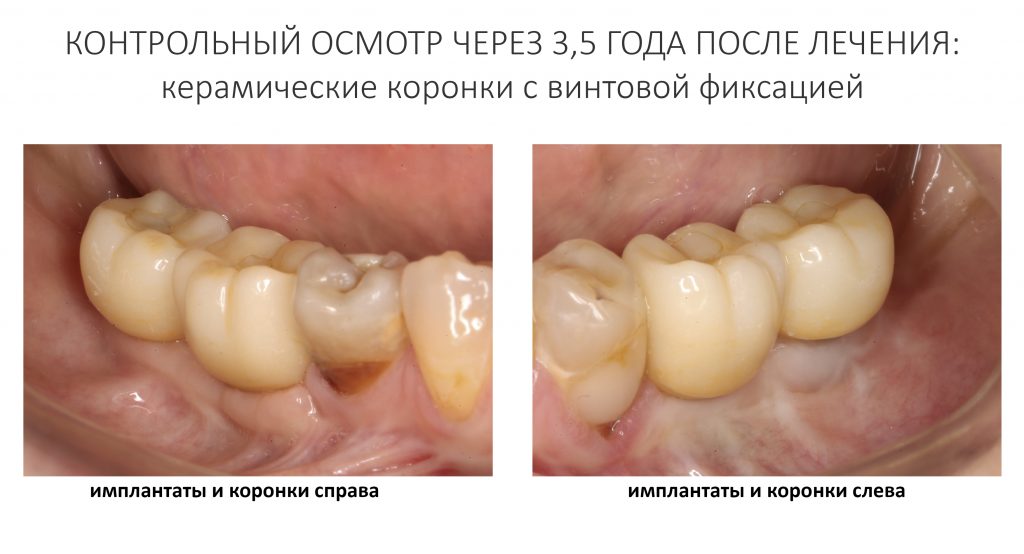
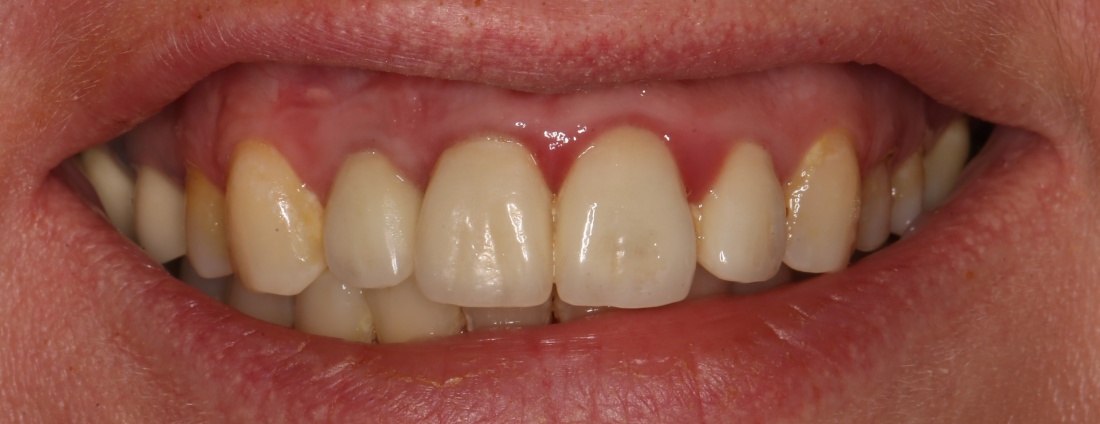
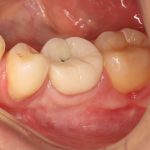
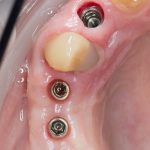
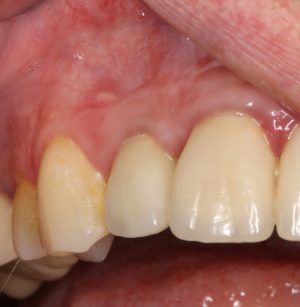
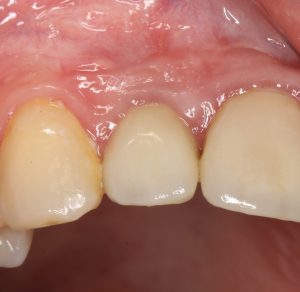
Мы встретились как старые друзья. Честно признаюсь, я очень переживал. Я ожидал увидеть какую-нибудь жуть, утраченную кость, периимплантит, разрушенный вхлам протез и всё такое. Но… всё оказалось не так плохо:
Но фиг с ними, с протезами. Это временные композитные коронки, их не так уж сложно заменить. Меня волнует другой вопрос:
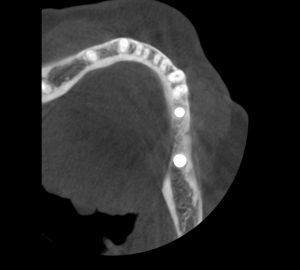
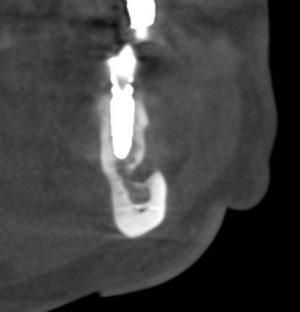
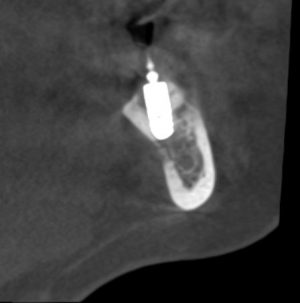
— что там с имплантатами и костной тканью?
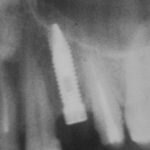
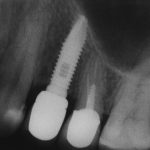
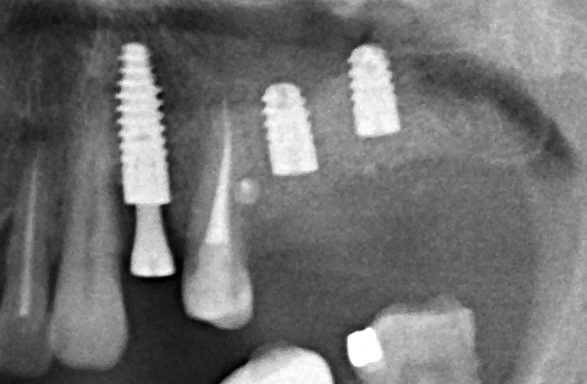
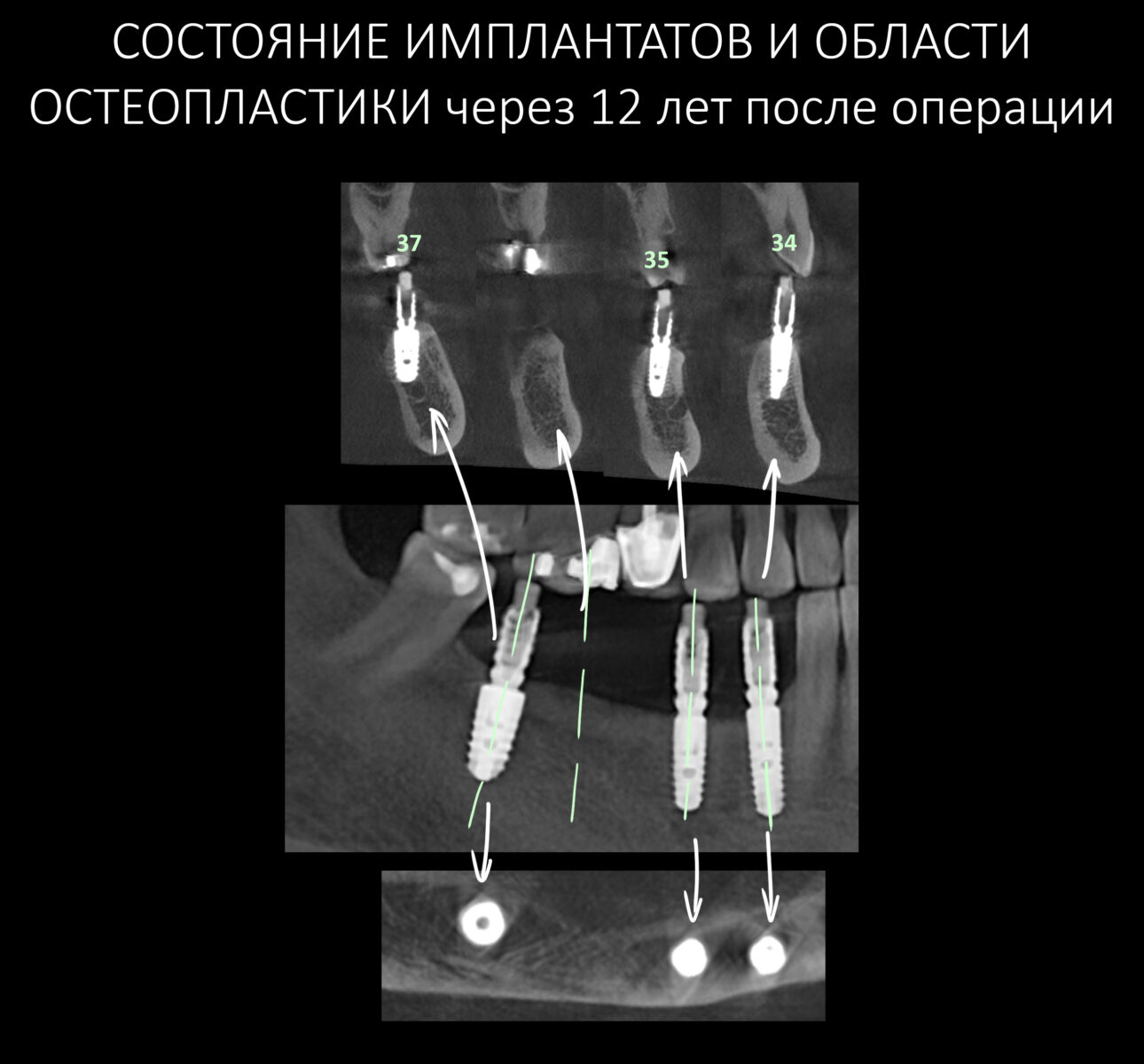
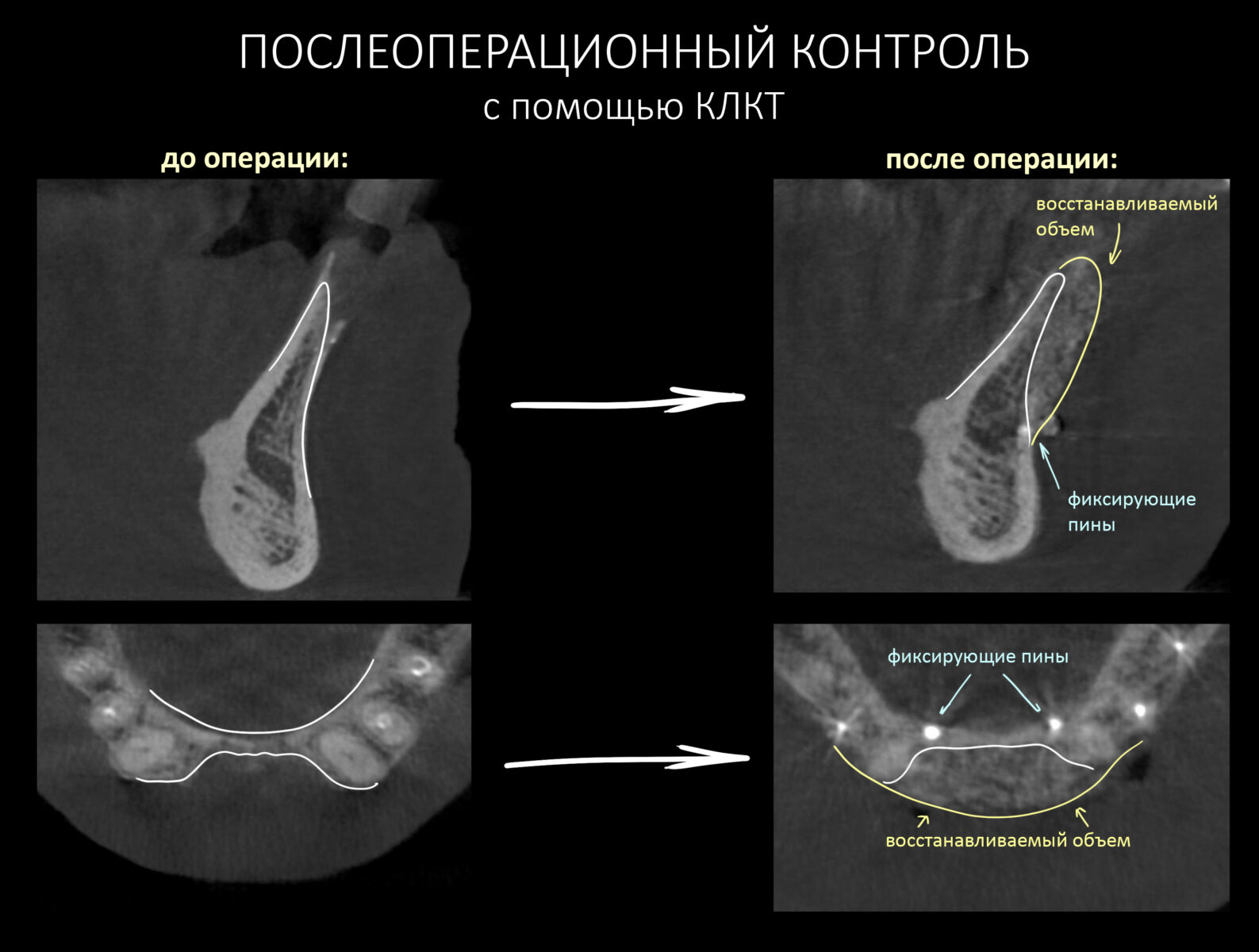
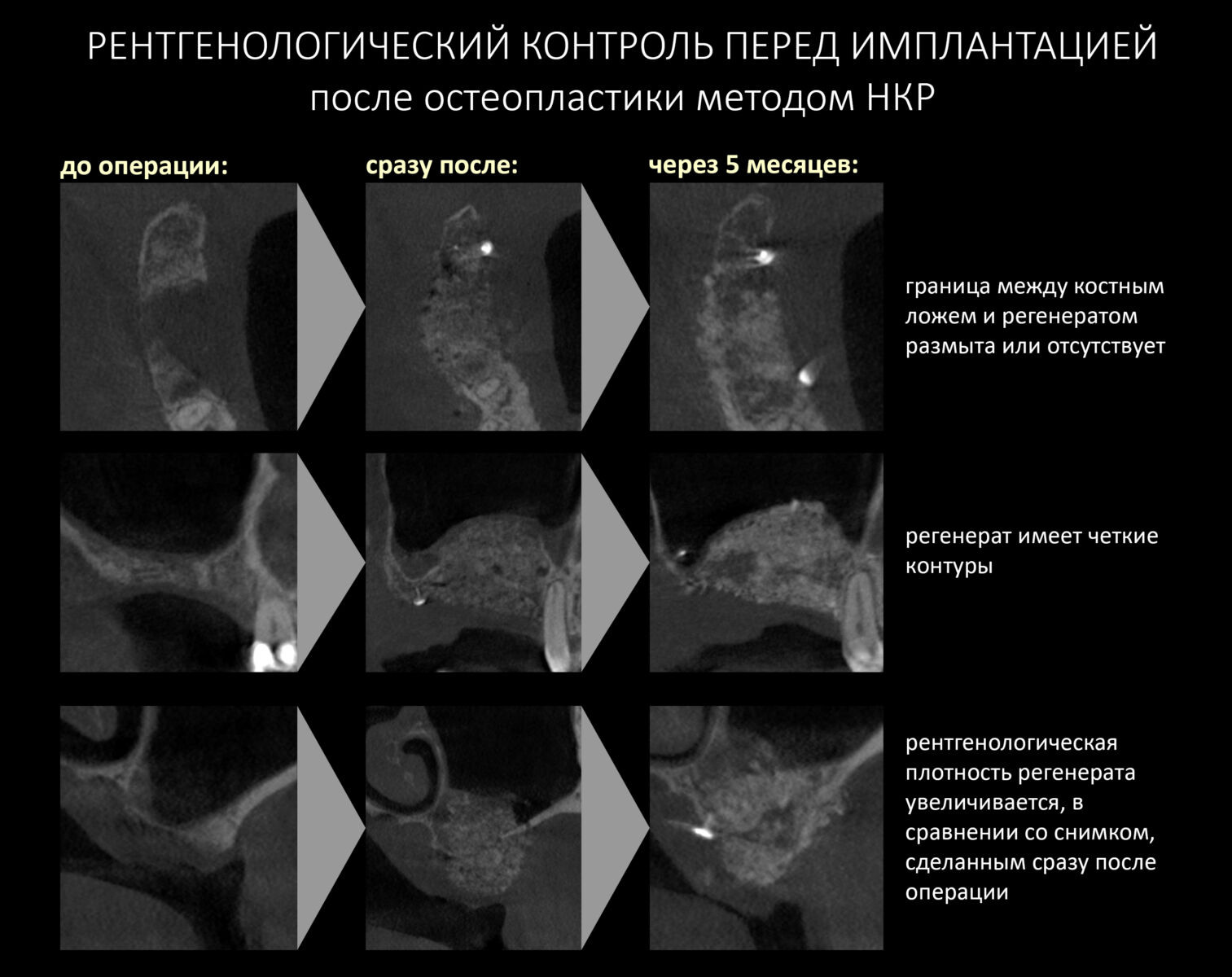
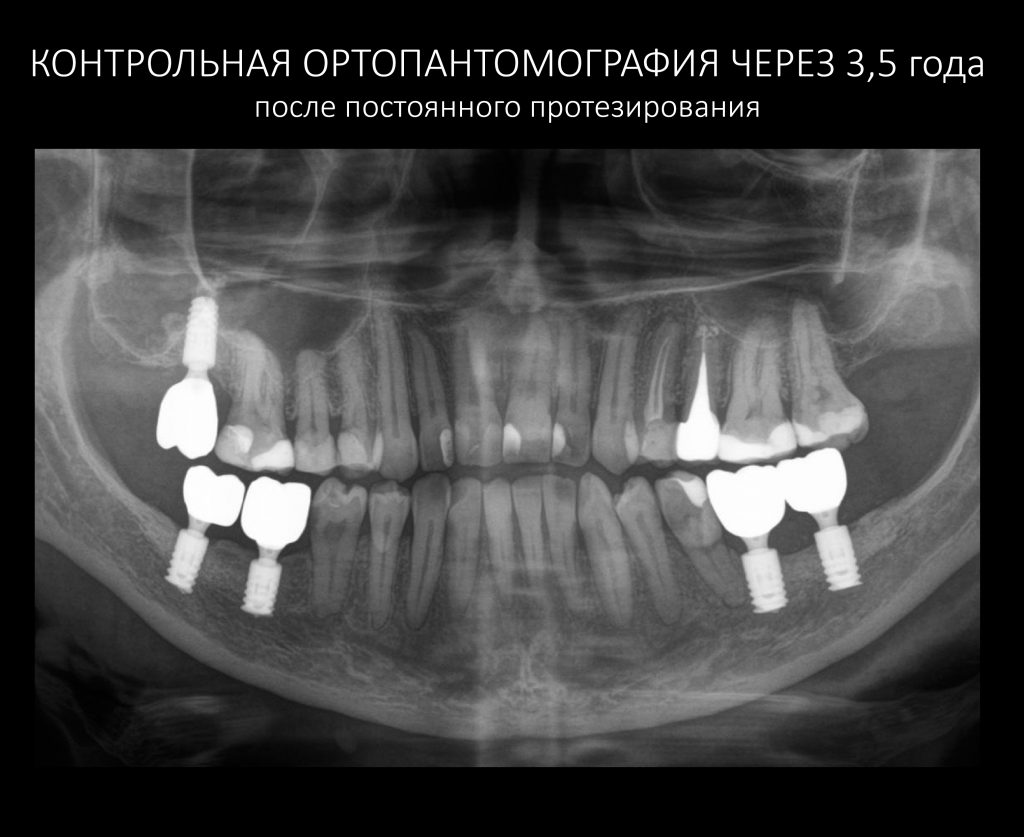
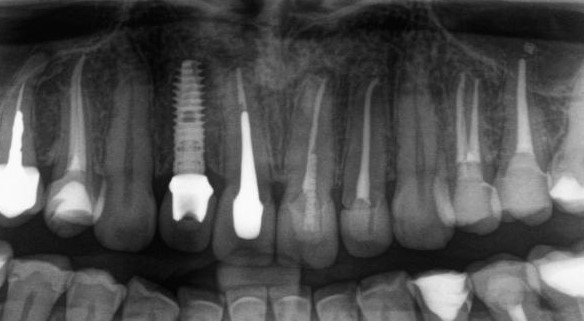
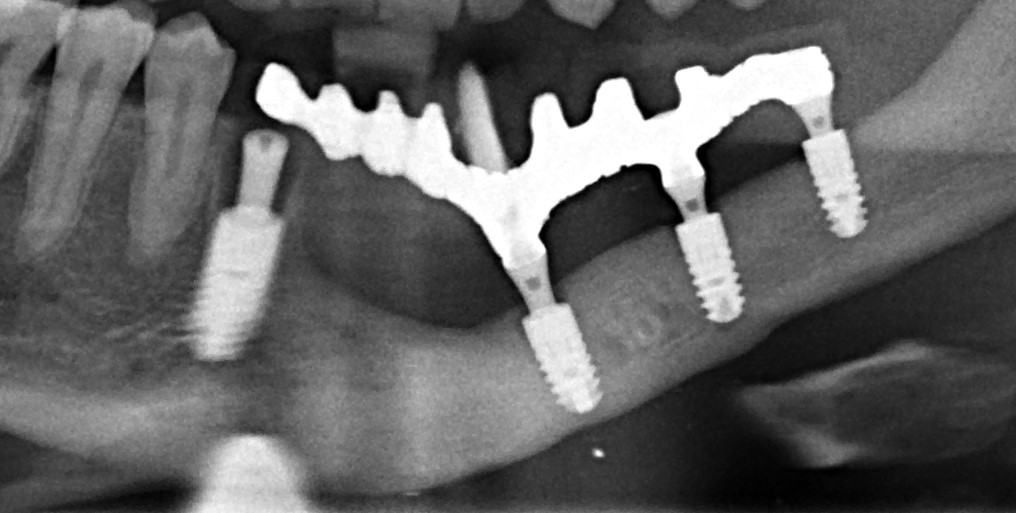
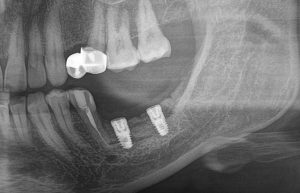
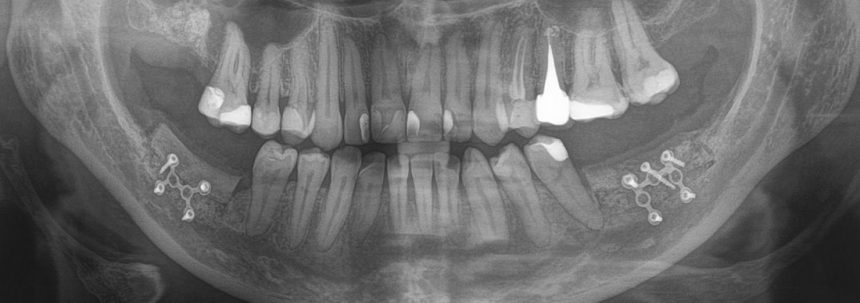
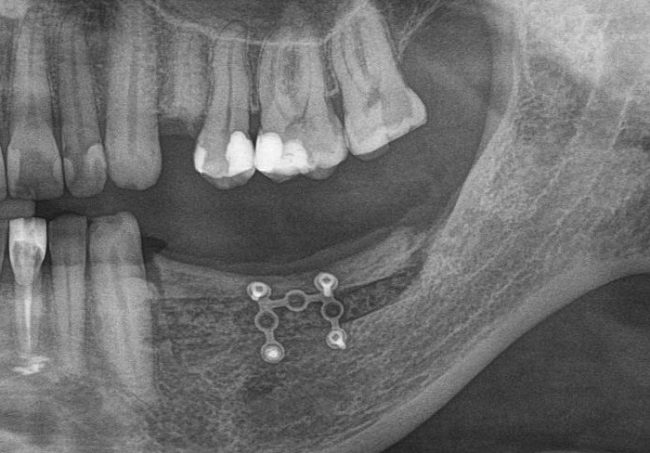
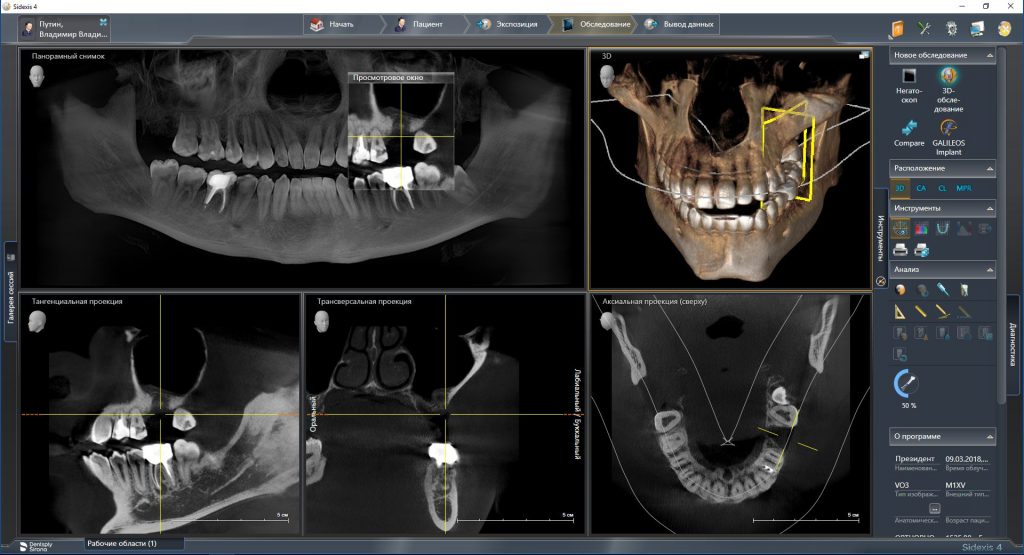
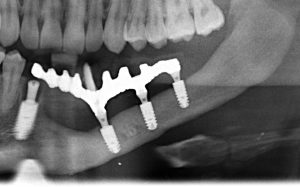
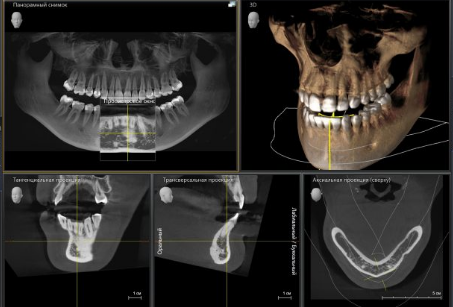
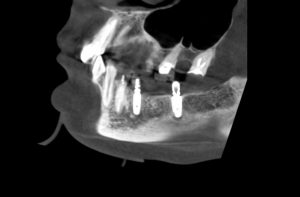
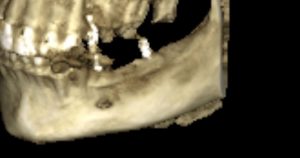
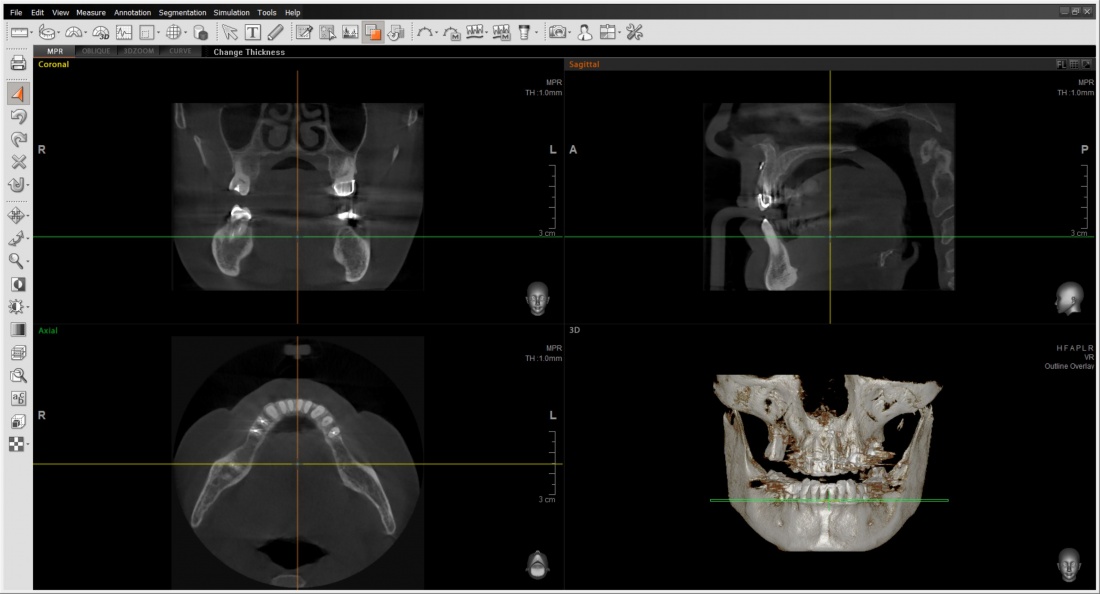
Для этого мы сделали КЛКТ:
И КЛКТ показала нам, что с имплантатами и окружающей костью всё зашибись. Через 12 лет после операции, отсутствия наблюдения, пофигизма в замене временных коронок! Нужны ли тебе еще какие-нибудь доводы в пользу долгосрочной эффективности метода?
Что дальше?
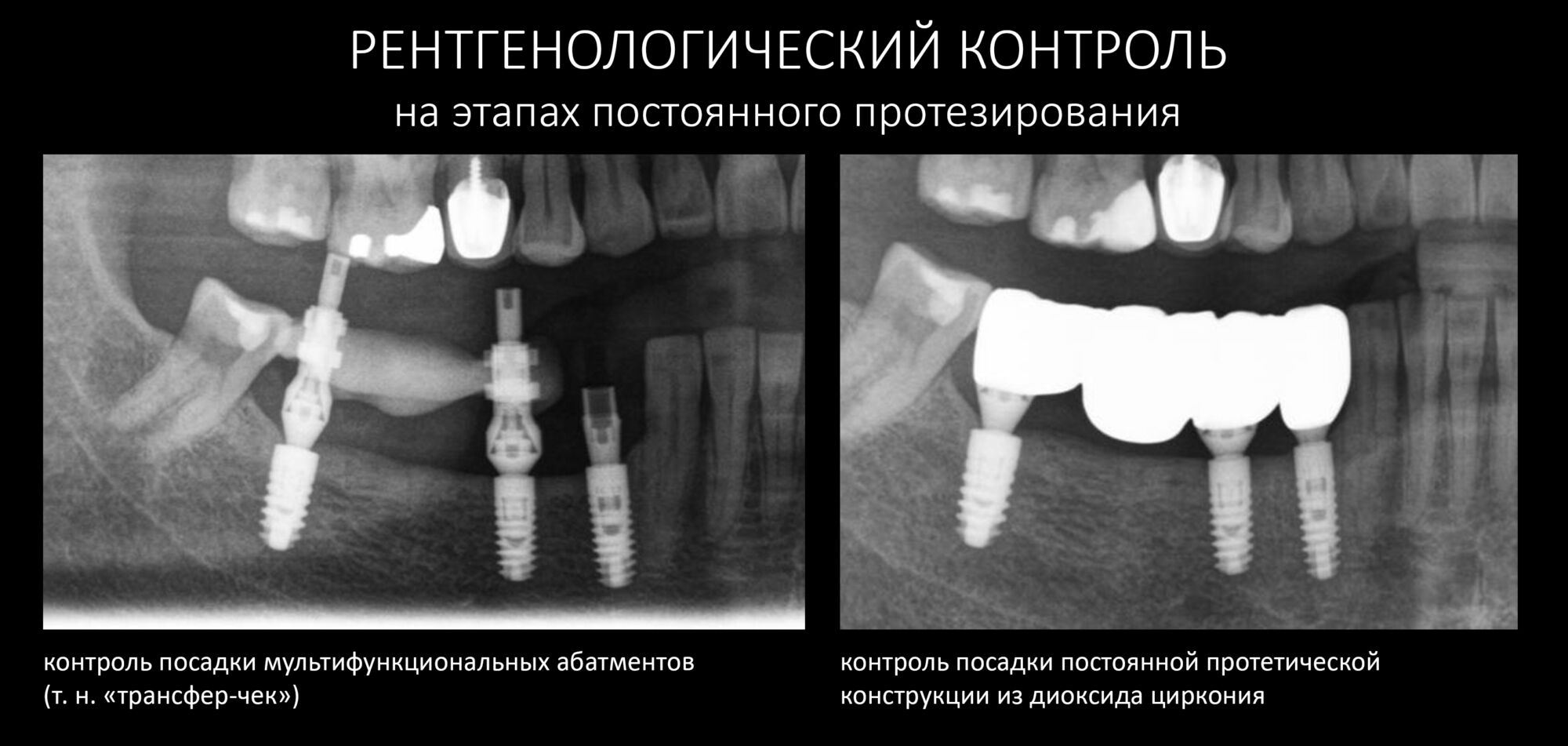
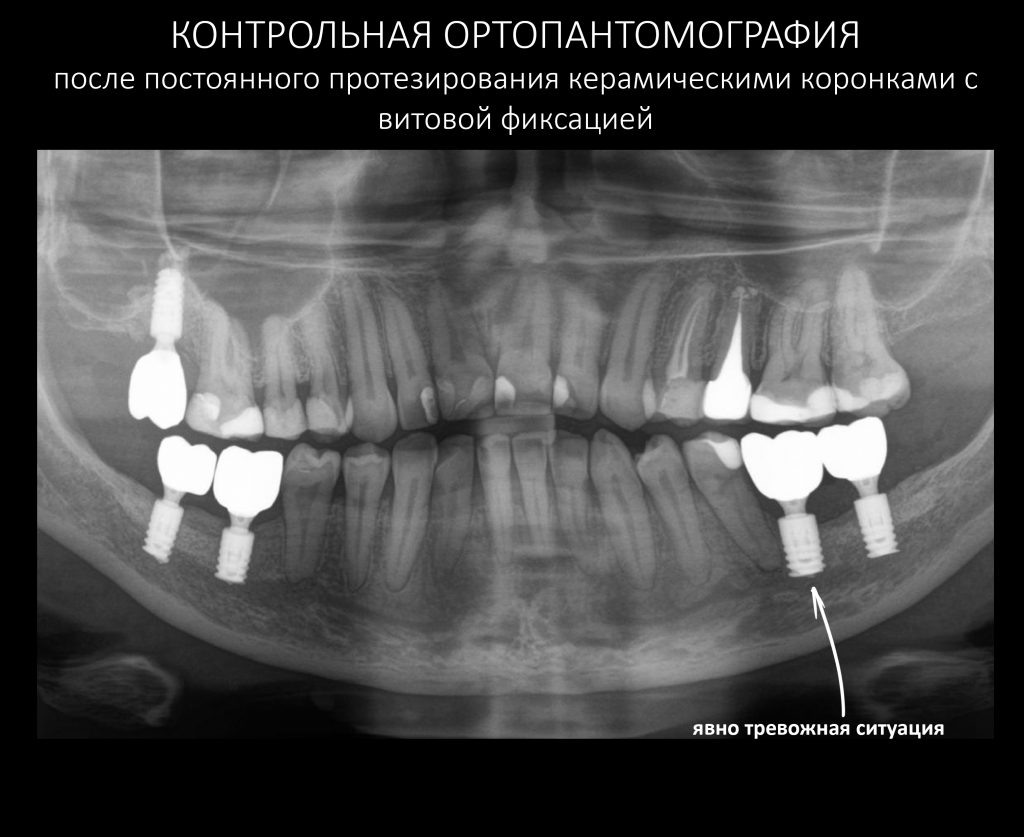
А дальше всё просто. Я попросил своего коллегу Ивана Алгазина заменить износившиеся временные коронки на постоянные керамические — но с учётом современных реалий и требований:
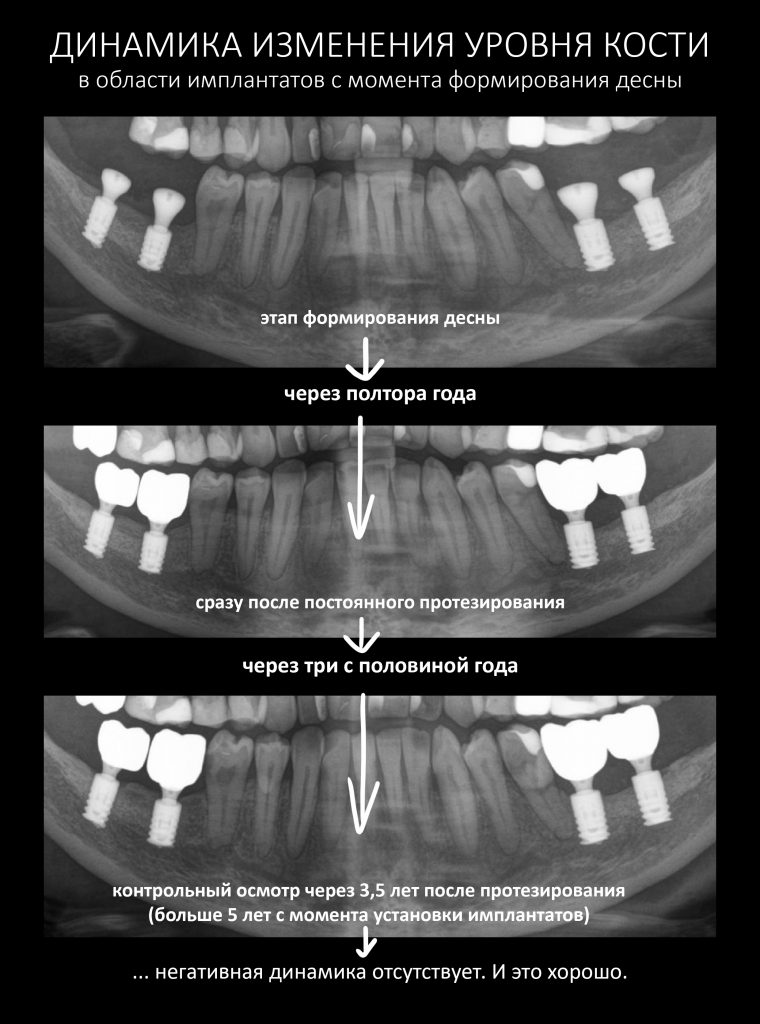
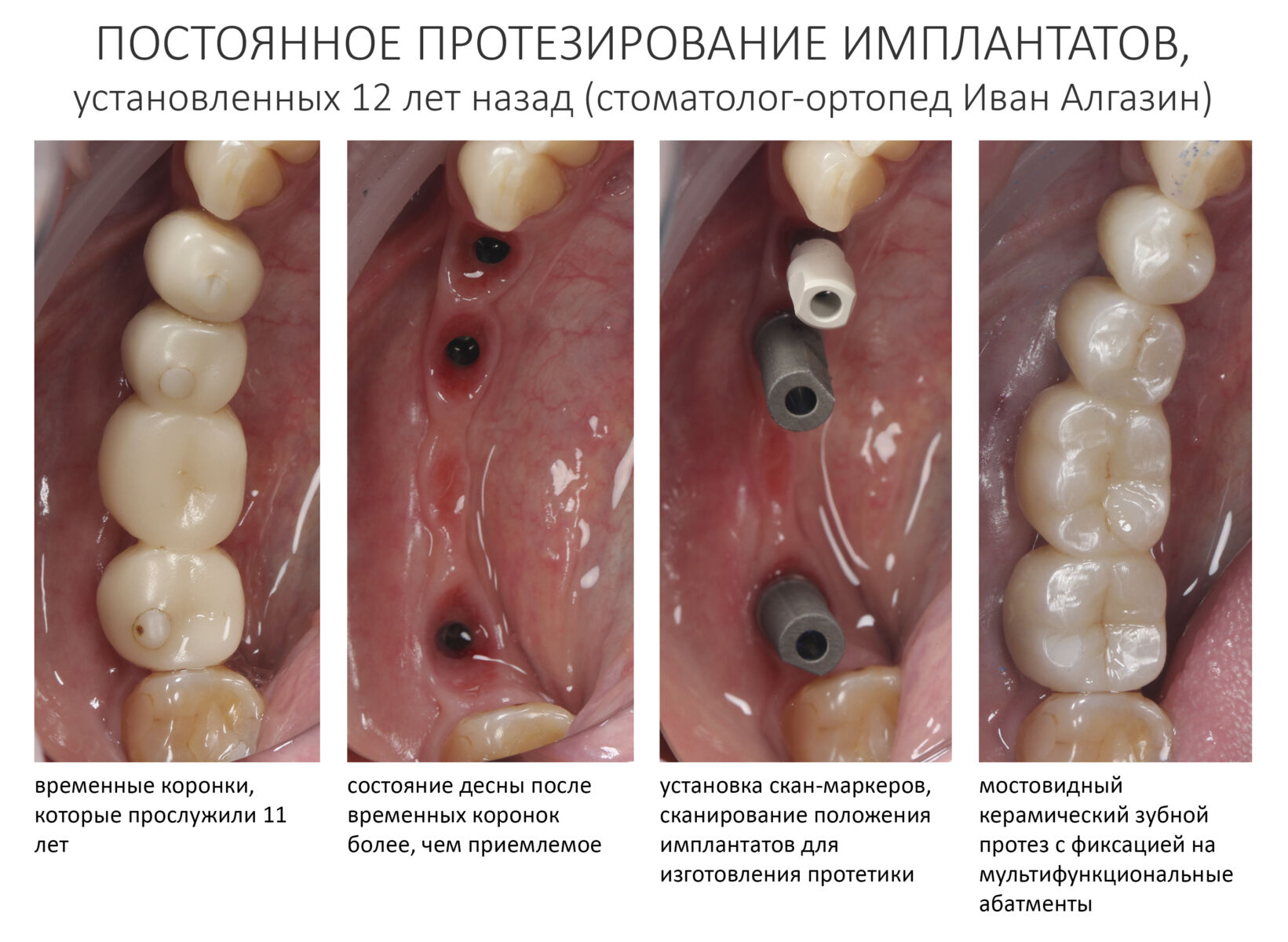 Серия контрольных снимков на этапах:
Серия контрольных снимков на этапах:
Вот так закончилась 12-летняя эпопея Зинаиды с восстановлением зубов на нижней челюсти. Через пару дней она уехала на экскурсию в Санкт-Петербург (на всякий случай, мы попросили задержаться в России, вдруг потребуется коррекция), а оттуда — домой, в дружественную страну. Судя по тому, что она нам пишет — у неё всё прекрасно и хорошо. Зинаида обещает не пропускать профилактические осмотры и наблюдаться у стоматолога по месту жительства.
Надеюсь, так оно и будет.
* * *
Описанный здесь хирургический этап был давно, 12 лет назад — ежу понятно, он отличается от того, что мы делаем сейчас. Наверное, не было бы повода рассказывать об этом клиническом случае так подробно, если бы не ванги.
Ванги
Вангами я называю любителей заглядывать в будущее и предсказывать. Эдаких провидцев на минималках. Это та самая разновидность диванных экспертов с минимальным опытом и поверхностными знаниями, для которых умение прогнозировать является синонимом «экспертности». Такие ванги есть везде, в любой группе, паблике или в любом сообществе. Ты их встречал, и не один раз. Их прогнозы, в основном пессимистичны и выглядят как «всё развалится…», «будет только хуже…», «ничего не получится!..», » не взлетит…» и т. п. Как они приходят к таким прогнозам — хрен его знает. Почему они хотят всем об этом рассказать — объяснения нет даже у самих ванг. Они не заморачиваются глубоким анализом, не знакомы с методологией научного прогнозирования, ибо для этого нужен мозг, а у них его нет. У современной ванги вместо мозга — ChatGPT. Каждый их коммент — не поиск истины, а стремление самоутвердиться. Даже когда ванга задает вопрос — ей не нужен твой ответ, ей нужно чтобы ты выслушал её невероятно ценное «проффесиональное» мнение.
Примерно в 2015 году, когда этот клинический случай, условно говоря, был завершен, в стоматологическом сообществе одной вражеской социальной сети разгорелась дискуссия об эффективности методов остеопластики, плавно переходящая в срач. Несмотря на то, что уже тогда я не питал никаких иллюзий в отношении профессиональных пабликов и тех, кто в них зависает, я решил выложить комикс-обзор на основе этого случая в обсуждении эффективности методов наращивания костной ткани.
 Я бы привел ссылку на свой коммент, но, во-первых, эта вражеская социальная сеть, принадлежащая террористической организации, заблокирована на территории нашей страны, а, во-вторых, мне лень.
Я бы привел ссылку на свой коммент, но, во-первых, эта вражеская социальная сеть, принадлежащая террористической организации, заблокирована на территории нашей страны, а, во-вторых, мне лень.
Стоило мне нажать «Отправить», как на мой комикс сразу набежали ванги, их общий посыл выглядел так:
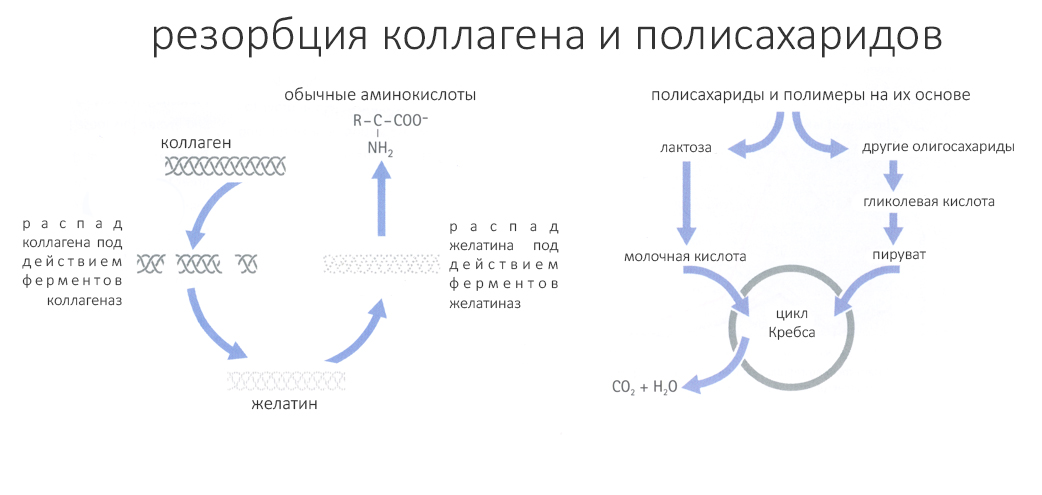
«Всё херня/всё развалится/костные блоки уйдут/надо было делать НКР/импланты выпадут/метод неэффективный, всё резорбируется/бла-бла-бла…./Урбан сказал/Кури сказал/Массирони сказал…»
В итоге, ванги были посланы нахер, а я — заблокирован в стоматологическом паблике за оскорбление уважаемых людей. Да, среди ванг встречаются деятели, обвешанные свистелками-перделками аки новогодняя ёлка. Они всерьез считают, что за это их нужно уважать. Ога, канешн.
Но, не суть. С момента описанной хирургической операции прошло 12 лет. С момента моего комикса в паблике и обсуждения эффективности методов остеопластики- примерно десять лет.
Наверное, сегодня я могу обратиться ко всем вангам во всех стоматологических пабликах:
Предсказания — это не признак «экспертности». Стремление всюду и всему давать прогнозы — признак недалекого ума и отсутствия опыта.
Это если вежливо.
А если нет, то
Лососните тунца, предсказатели херовы!
Да-да, именно так ты можешь сказать всем вангам, если повстречаешь их на своём профессиональном пути.
По идее, нужно закончить мой рассказ какими-то выводами и моралью.
Начну с морали:
Мораль.
Наука, какой бы они ни была, изучает причинно-следственные взаимосвязи. Причина — в прошлом, Следствие — в настоящем. У науки нет возможности изучать будущее. Поэтому наука никогда не смотрит вперед. Она смотрит назад и по сторонам. Как только наука начинает рассказывать о будущем, делать прогнозы и давать предсказания — она перестает быть наукой.
Прогнозы в медицине — дело крайне не благодарное. Если не сказать, что зловредное. Всё, что у нас есть в медицине в настоящий момент — это прошлое. У нас есть статистика, но это статистика прошлого. У нас есть опыт, но это всегда опыт прошлого. Сто офигенно результативных операций никак не гарантируют, что следующая, сто первая операция пройдет хорошо. В медицине мы можем говорить только об осторожных предположениях, но никак не о прогнозах.
Для того, чтобы сделать осторожное предположение, нужно намного больше данных, чем есть у любого комментатора в интернетах. По сути, предполагать могут лишь доктор и его пациент. Те, кто планировал, обосновывал и принимал решения, проводил лечение, наблюдал за развитием ситуации и т. д. Остальные не имеют никаких моральных и этических прав на прогнозы, поэтому идут нахер. Это утверждение превращает любое интернет-обсуждение клинических случаев в пустую трату времени. Дискуссии в профессиональных пабликах контрпродуктивны. Они не дают знаний, не несут никакой практической пользы и ставят целью самоутверждение и повышение чувства собственной важности.
Если ты хочешь чему-то научиться — читай книжки (не обязательно мои) и общайся с реальными докторами в реальной жизни. Лучший вариант — сначала встать за спиной, а затем и рядом со своим более опытным коллегой. Доктора так всегда учились. Я так учился. Это единственный проверенный способ стать настоящим хирургом. Других вариантов нет. Кстати, об этом я говорил во время разговора со студентами.
Выводы.
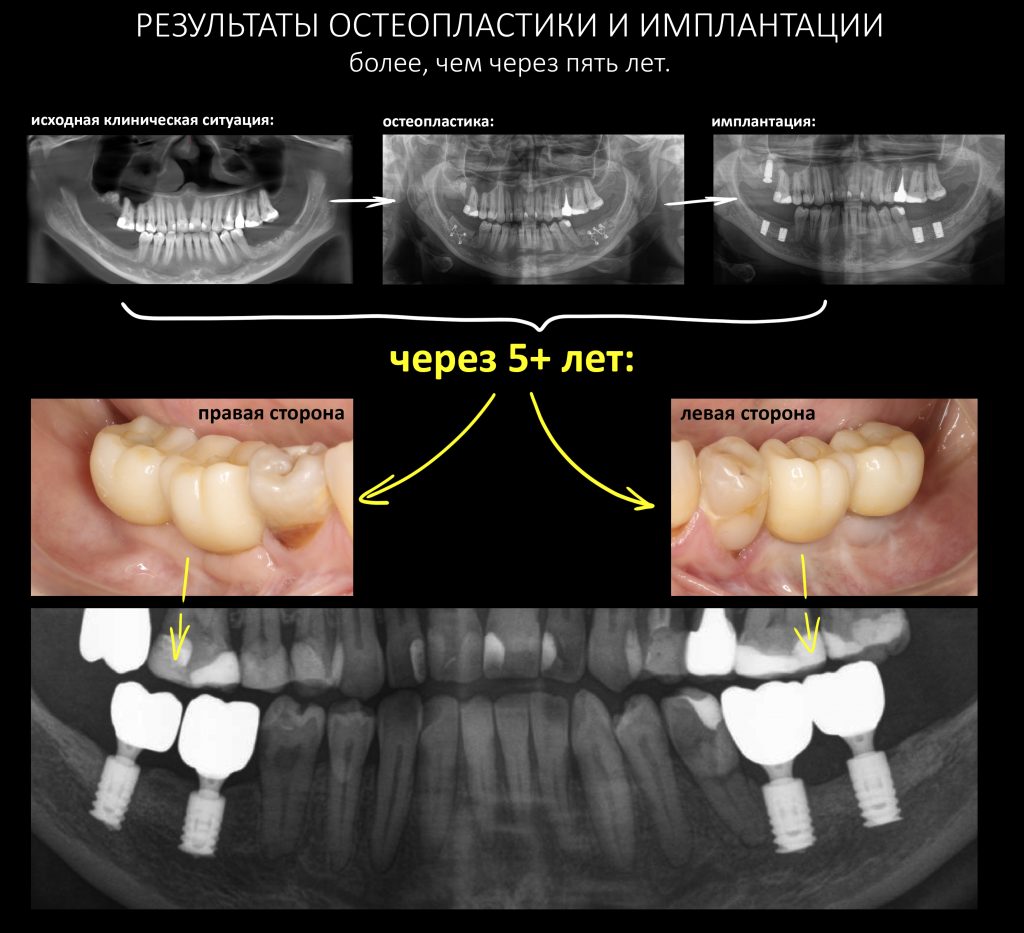
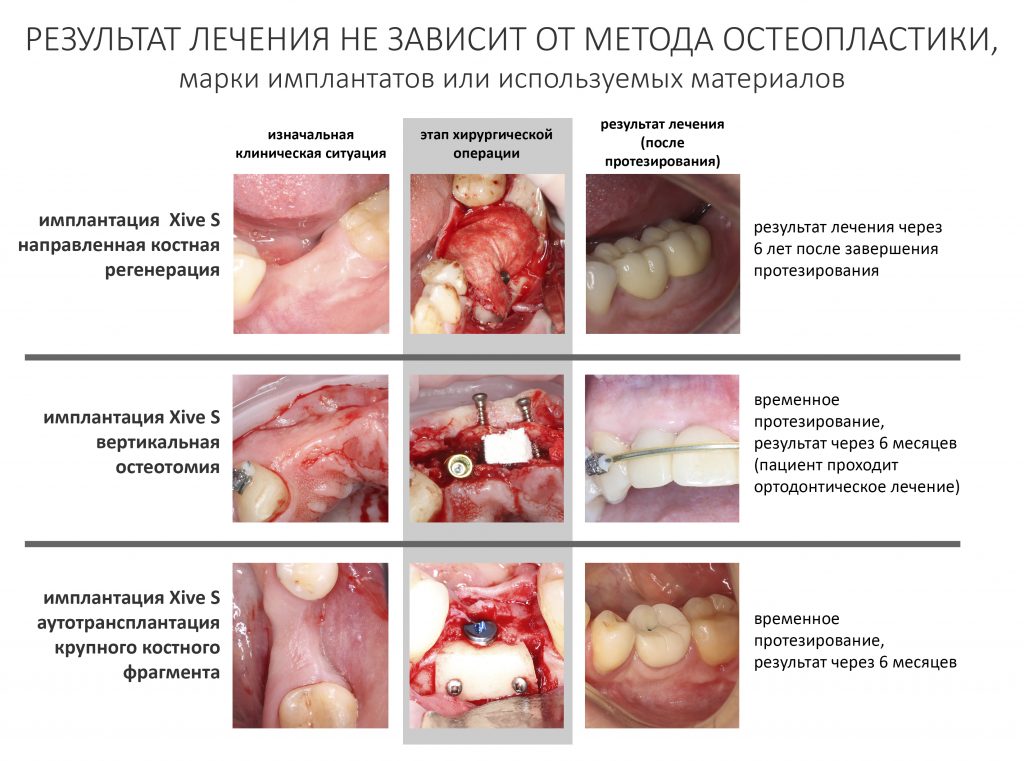
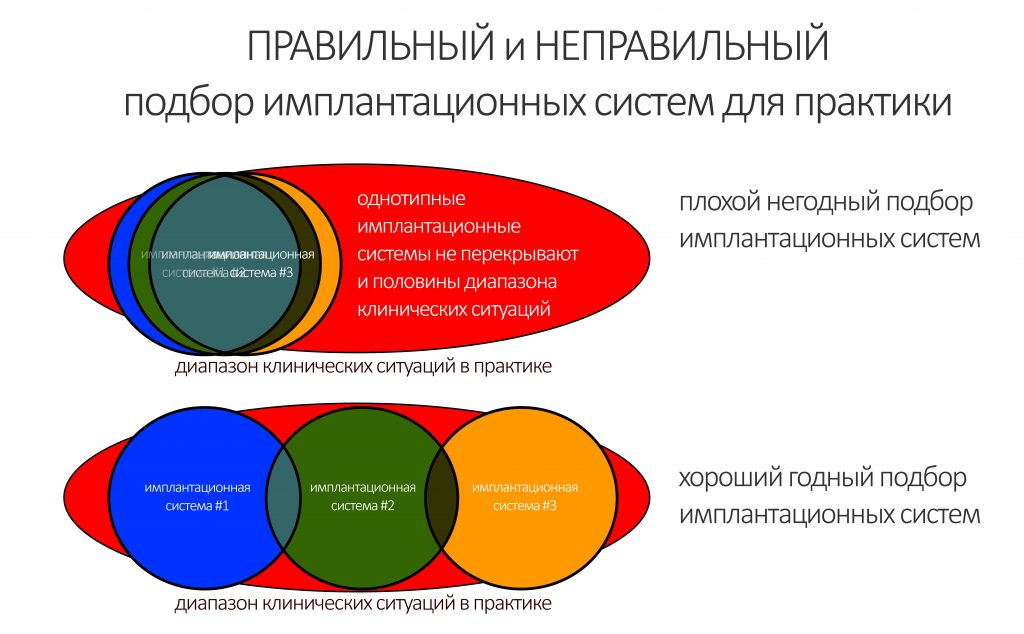
Нет никакой разницы в эффективности различных методов остеопластики. Вообще никакой. Все методы наращивания костной ткани одинаково результативны при условии, что правильно спланированы и реализованы.
Нельзя противопоставлять различные способы остеопластики. НКР никак не противоречит остеотомии, а она, в свою очередь, никогда не заменит АТККФ там, где это нужно. Профессионализм стоматолога-хирурга состоит не столько в правильной реализации методов наращивания кости, сколько в умении правильно выбирать подходящий метод для имеющихся клинических условий.
Наконец, никакая операция не может быть сложнее, чем ее планирование (с). Если во время или после операции с твоим пациентом начинается какая-то бабуйня — значит, ты что-то упустил при планировании.
Помни об этом. Еще на забудь подписаться на нашу новую группу в Телеграм, где есть раздел для врачей.
И всё у тебя получится!
Спасибо, что дочитал до конца. Как всегда, я готов ответить на любые твои вопросы. Пиши в комментах прямо здесь.
С уважением, Станислав Васильев, стоматолог-хирург, КЛИНИКА ИН.









































































 В эпоху раннего Средневековья, точнее в 13-14 вв. н. э., в английской деревне Оккам (Ockham) жил чувак по имени Уильям.
В эпоху раннего Средневековья, точнее в 13-14 вв. н. э., в английской деревне Оккам (Ockham) жил чувак по имени Уильям.














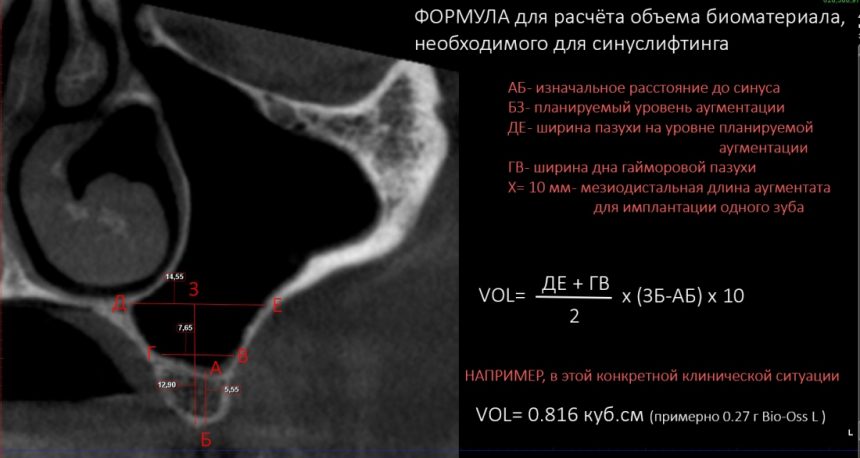
 Признаюсь, не совсем понимаю необходимости назначения консультации ЛОР-врача всем пациентам поголовно. Скажем, если у пациента нет жалоб со стороны носовой полости, нет вазомоторного или аллергического ринита, на КЛКТ все носовые пазухи воздушные и чистые, их сообщение с носовой полостью не нарушено — каков смысл гонять пациента к ринологу?
Признаюсь, не совсем понимаю необходимости назначения консультации ЛОР-врача всем пациентам поголовно. Скажем, если у пациента нет жалоб со стороны носовой полости, нет вазомоторного или аллергического ринита, на КЛКТ все носовые пазухи воздушные и чистые, их сообщение с носовой полостью не нарушено — каков смысл гонять пациента к ринологу?